О. уравнотежење једначина омогућава нам да подударамо број атома присутних у хемијској једначини тако да она постане тачна и представља хемијску реакцију.
Користите питања у наставку да бисте тестирали своје знање и проверили одговоре коментарисане након повратних информација да бисте одговорили на своја питања.
Питање 1
(Мацкензие-СП)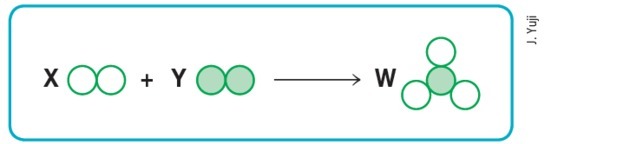
Под претпоставком да празни и испуњени кругови значе различите атоме, онда шема горе представљаће уравнотежену хемијску реакцију ако слова Кс, И и В заменимо са вредности:
а) 1, 2 и 3.
б) 1, 2 и 2.
в) 2, 1 и 3.
г) 3, 1 и 2.
д) 3, 2 и 2.
Алтернатива г) 3, 1 и 2.
1. корак: Додељујемо слова како бисмо олакшали разумевање једначине.
2. корак: збрајамо индексе да бисмо сазнали ко има највише атома у једначини.
| ТХЕ | |
| Б. |
А и Б се појављују само једном у сваком члану једначине. Међутим, ако додамо индексе, видимо да А има највећу вредност. Стога смо започели балансирање за њега.
3. корак: Избалансирамо елемент А транспонујући индексе и претварајући их у коефицијенте.
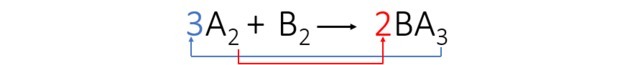
Приметили смо да је елемент Б аутоматски уравнотежен, а коефицијенти једначине су: 3, 1 и 2.
питање 2
(Уницамп-СП) Прочитајте следећу реченицу и трансформишите је у (уравнотежену) хемијску једначину, користећи симболе и формуле: „молекул гасовитог азота, који садржи два атома азот по молекулу, реагује са три молекула двоатомног, гасовитог водоника, производећи два молекула гасовитог амонијака, који се састоји од три атома водоника и једног од азот ".
Одговорити:
Представљајући атоме описане у питању, можемо схватити да се реакција одвија на следећи начин:
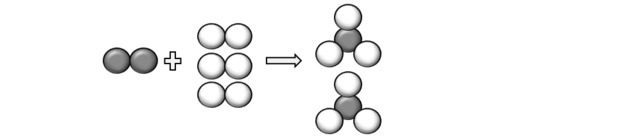
Дакле, долазимо до једначине:
питање 3
Водоник-пероксид је хемијско једињење које се може разградити, формирајући воду и кисеоник, у складу са хемијском једначином доле.
Што се тиче ове реакције, правилно уравнотежена једначина је:
Ах2О.2 → Тхе2 + Х2О.
б) 2х2О.2 → Тхе2 + 2Х2О.
ц) Х.2О.2 → 2О2 + Х2О.
д) 2х2О.2 → 2О2 + 2Х2О.
Тачна алтернатива: б) 2Х2О.2 → Тхе2 + 2Х2О.
Имајте на уму да је водоник-пероксид хемикалија која се састоји од атома два хемијска елемента: водоника и кисеоника.
Након реакције разградње морате имати исти број атома два елемента и у реактантима и у производима. За ово морамо уравнотежити једначину.
Имајте на уму да у реактанту имамо 2 атома водоника (Х2О.2) и два атома у производу (Х.2О). Међутим, кисеоник има два атома у реактанту (Х2О.2) и три атома у производима (Х.2О и О.2).
Ако коефицијент 2 ставимо испред водоник-пероксида, удвостручујемо број атома елемената.
Имајте на уму да ако ставимо исти коефицијент заједно са формулом за воду, имамо исту количину атома на обе стране.
Стога је правилно уравнотежена хемијска једначина 2Х2О.2 → Тхе2 + 2Х2О.
питање 4
(УФПЕ) Размотрите хемијске реакције у наставку.
Можемо рећи да:
а) сви су уравнотежени.
б) 2, 3 и 4 су уравнотежени.
в) уравнотежена су само 2 и 4.
г) само 1 је неуравнотежен.
е) ниједна није правилно уравнотежена, јер су физичка стања реактаната и производа различита.
Алтернатива б) 2, 3 и 4 су уравнотежене.
Алтернативе 1 и 5 су нетачне јер:
- Једначина 1 је неуравнотежена, исправан биланс би био:
- Једначина 5 је нетачна јер би једињење настало у реакцији било Х2САМО3.
Да би се формирао Х.2САМО4 треба укључити у једначину оксидација СО2.
питање 5
(Мацкензие-СП) Загрејан на 800 ° Ц, калцијум-карбонат се разлаже на калцијум-оксид (девичански креч) и угљен-диоксид. Тачно уравнотежена једначина, која одговара описаном феномену, је:
(Дато: Ца - земноалкални метал.)
Алтернатива ц)
Калцијум је земноалкални метал и за стабилност калцијуму су потребна 2 електрона (Ца2+), што је набој кисеоника (О2-).
Дакле, атом калцијума се везује за атом кисеоника и настало једињење је ЦаО, које је живо вапно.
Други производ је угљен-диоксид (ЦО2). Обе се формирају калцијум-карбонатом (ЦаЦО3).
Стављајући га у једначину:
Примећујемо да су количине атома већ тачне и да их није потребно уравнотежити.
питање 6
(УФМГ) Једначина није уравнотежен. Избалансирајући га са најмањим могућим бројевима, збир стехиометријских коефицијената биће:
а) 4
б) 7
ц) 10
д) 11
е) 12
Алтернатива д) 12
Користећи пробну методу, редослед уравнотежења биће:
1. корак: Како је елемент који се појављује само једном у сваком члану и има највећи индекс калцијум, почели смо да балансирамо за њега.
2. корак: Пратимо балансирање радикалног ПО43-, који се такође појављује само једном.
3. корак: уравнотежујемо водоник.
Овим примећујемо да је аутоматски прилагођена количина кисеоника и равнотежа једначине је:
Имајући на уму да када је коефицијент 1 не треба да га записујете у једначину.
Сабирањем коефицијената које имамо:
питање 7
Сагоревање је врста хемијске реакције у којој се енергија ослобађа у облику топлоте.
У потпуном сагоревању супстанце коју чине угљеник и водоник, настају угљен-диоксид и вода.
Посматрајте реакције сагоревања угљоводоника и одговорите која од једначина у наставку није правилно уравнотежена:
а) ЦХ4 + 2О2 → ЦО2 + 2Х2О.
пре нове ере3Х.8 +502 → 3ЦО2 + 4Х2О.
ц) Ц.4Х.10 + 13 / 3О2 → 4ЦО2 + 5х2О.
д) Ц.2Х.6 + 7 / 2О2 → 2ЦО2 + 3Х2О.
Нетачан одговор: в) Ц.4Х.10 + 13 / 3О2 → 4ЦО2 + 5х2О.
Да бисмо уравнотежили хемијске једначине, погледајмо прво који се елемент појављује само једном у сваком члану једначине.
Имајте на уму да угљеник и водоник чине само један реагенс и један производ у свакој приказаној једначини.
Па кренимо са балансирањем са водоником, јер он има већи број атома.
Стога ће редослед уравнотежења бити:
- Водоник
- Угљеник
- Кисеоник
Водоник
Како производ има 2 атома водоника, убацујемо број као коефицијент који помножен са 2 даје резултат број атома водоника реактанта.
а) ЦХ4 + О.2 → ЦО2 + 2Х.2О.
пре нове ере3Х.8 + О.2 → ЦО2 + 4Х.2О.
ц) Ц.4Х.10 + О.2 → ЦО2 + 5Х.2О.
д) Ц.2Х.6 + О.2 → ЦО2 + 3Х.2О.
Угљеник
Балансирање се врши транспоновањем индекса угљеника у реактанту и његовим коришћењем као коефицијента на производу који има атоме овог елемента.
а) ЦХ4 + О.2 → 1ЦО2 + 2Х2О.
пре нове ере3Х.8 + О.2 → 3ЦО2 + 4Х2О.
ц) Ц.4Х.10 + О.2 → 4ЦО2 + 5х2О.
д) Ц.2Х.6 + О.2 → 2ЦО2 + 3Х2О.
Кисеоник
Сабирањем броја атома кисеоника у насталим производима проналазимо број атома елемента који мора да реагује.
За то морамо као коефицијент ставити број који помножен са 2 резултира бројем атома кисеоника у производима.
а) ЦХ4 + О.2 → 1ЦО2 + 2Х2О.
2к = 2 + 2
2к = 4
к = 2
Дакле, тачна једначина је: ЦХ4 + 2О.2 → 1ЦО2 + 2Х2О.
пре нове ере3Х.8 + О.2 → 3ЦО2 + 4Х2О.
2к = 6 + 4
2к = 10
к = 5
Дакле, тачна једначина је: Ц.3Х.8 + 5О.2 → 3ЦО2 + 4Х2О.
ц) Ц.4Х.10 + О.2 → 4ЦО2 + 5х2О.
2к = 8 + 5
2к = 13
к = 13/2
Дакле, тачна једначина је: Ц.4Х.10 + 13/2О.2 → 4ЦО2+ 5х2О.
д) Ц.2Х.6 + О.2 → 2ЦО2 + 3Х2О.
2к = 4 + 3
2к = 7
к = 7/2
Дакле, тачна једначина је: Ц.2Х.6 + 7/2О.2 → 2ЦО2 + 3Х2О.
Тачно уравнотежене једначине су:
а) ЦХ4 + 2О2 → ЦО2 + 2Х2О.
пре нове ере3Х.8 +502 → 3ЦО2 + 4Х2О.
ц) Ц.4Х.10 + 13 / 2О2 → 4ЦО2 + 5х2О.
д) Ц.2Х.6 + 7 / 2О2 → 2ЦО2 + 3Х2О.
Дакле, алтернатива в) Ц.4Х.10 + 13 / 3О2 → 4ЦО2 + 5х2Ствар је у томе што нема правилан биланс.
питање 8
(Енем 2015) Кречњаци су материјали састављени од калцијум-карбоната, који могу деловати као сорбенти за сумпор-диоксид (СО2), важан загађивач ваздуха. Реакције укључене у процес су активација кречњака, калцинацијом, и фиксација СО2 са формирањем калцијумове соли, што илуструју поједностављене хемијске једначине.
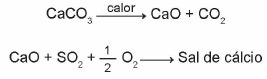
Узимајући у обзир реакције укључене у овај процес одсумпоравања, хемијска формула калцијумове соли одговара:
Алтернатива б)
Како је реакција уравнотежена, атоми садржани у реактантима морају бити у истој количини у производима. Тако,
Настала сол састоји се од:
1 атом калцијума = Ца
1 атом сумпора = С.
4 атома кисеоника = О.4
Према томе, хемијска формула калцијумове соли одговара ЦаСО4.
питање 9
(УФПИ) Реакција Кс са И приказана је у наставку. Одредите која једначина најбоље представља уравнотежену хемијску једначину.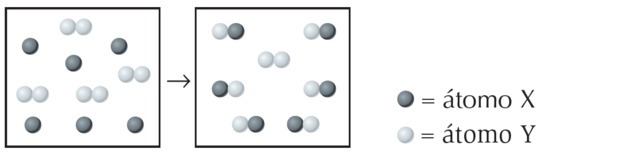
Алтернатива а)
На слици уочавамо да је врста Кс један атом док је И двоатомна, односно настаје спајањем 2 атома. Дакле, Кс реагује са И.2.
Настали производ је представљен са КСИ, при чему је једначина неуравнотежена:
Једначину уравнотежујемо на следећи начин:
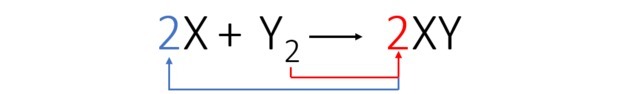
Према уравнотеженој једначини, доња слика показује нам како долази до реакције и њен удео.
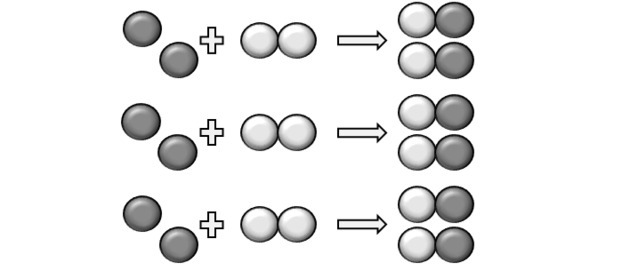
Да би се реакција догодила мора постојати фиксни однос и због тога неко једињење можда неће реаговати. То приказује слика, јер у производу видимо да је И2 није реаговао.
питање 10
(Енем 2010) Мобилизације за промоцију боље планете за будуће генерације су све чешће. Већина средстава масовног транспорта тренутно се напаја фосилним горивом. Као пример терета који ова пракса проузрокује, довољно је знати да аутомобил у просеку произведе око 200 г угљен-диоксида по пређеном километру.
Часопис за глобално загревање. Година 2, 8. Публикација Институто Брасилеиро де Цултура Лтда.
Један од главних састојака бензина је октан (Ц8Х.18). Кроз сагоревање октанске енергије је могуће, омогућавајући аутомобилу да се креће. Једначина која представља хемијску реакцију овог процеса показује да:
а) при томе се ослобађа кисеоник, у облику О.2.
б) стехиометријски коефицијент за воду је 8 до 1 октан.
в) у том процесу долази до потрошње воде, тако да се енергија ослобађа.
г) стехиометријски коефицијент за кисеоник је 12,5 до 1 октан.
д) стехиометријски коефицијент за угљен-диоксид је 9 до 1 октан
Алтернатива г) стехиометријски коефицијент за кисеоник је 12,5 до 1 октан.
Када балансирамо једначину, проналазимо следеће коефицијенте:
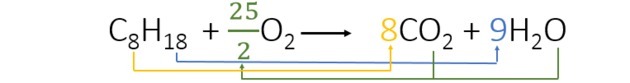
- Започели смо балансирање водоником који се појављује само једном у сваком члану и има већи индекс. С обзиром на то да у реакционом атому има 18 атома водоника, у производу их има 2, па морамо додати број који помножен са 2 даје 18. Дакле 9 је коефицијент.
- Затим додамо коефицијент 8 испред ЦО2 да има 8 угљеника у сваком члану једначине.
- На крају, само додајте количину кисеоника у производ и пронађите вредност која помножена са 2 даје 25 атома кисеоника. Па смо изабрали 25/2 или 12.5.
Дакле, за сагоревање 1 октана троши се 12,5 кисеоника.
питање 11
(Фатец-СП) Основна карактеристика ђубрива је њихова растворљивост у води. Стога индустрија ђубрива трансформише калцијум-фосфат, чија је растворљивост у води врло мала, у много растворљивије једињење, које је калцијум-суперфосфат. Овај процес је представљен једначином:
где су вредности к, и и з, респективно:
а) 4, 2 и 2.
б) 3, 6 и 3.
в) 2, 2 и 2.
г) 5, 2 и 3.
д) 3, 2 и 2.
Алтернатива д) 3, 2 и 2.
Користећи алгебарску методу, формирамо једначине за сваки елемент и изједначавамо број атома у реактанту са бројем атома у производу. Стога:
Уравнотежена једначина:
питање 12
Измерите доње једначине користећи пробну методу.
Одговорити:
Једначину чине елементи водоник и хлор. Елементе уравнотежујемо додавањем коефицијента 2 испред производа.
Једначину није требало уравнотежити, јер су количине атома већ прилагођене.
Фосфор има два атома у реактантима, па за уравнотежење овог елемента подешавамо количину фосфорне киселине у производу на 2Х3ДУСТ4.
Након тога, приметили смо да водоник има 6 атома у производу, уравнотежили смо количину овог елемента додајући коефицијент 3 реактанту који га садржи.
Са претходним корацима, количина кисеоника је била фиксна.
Гледајући једначину видимо да су количине водоника и брома у производима двоструко веће ако их има у реагенсима, па ХБр додајемо коефицијент 2 да бисмо уравнотежили ова два елементи.
Хлор има 3 атома у производима и само 1 у реактантима, тако да балансирамо стављајући коефицијент 3 пре ХЦл.
Водоник је имао 3 атома у реактантима и 2 атома у производима. Да бисмо прилагодили величине, трансформишемо индекс Х.2 у коефицијенту множимо са 3 која је већ била у ХЦл и добијамо резултат 6ХЦл.
Количине хлора у производима прилагођавамо тако да имају и 6 атома и добијамо 2АлЦл3.
Алуминијум је имао 2 атома у производима, прилагодили смо количину у реактантима на 2Ал.
Избалансирамо количину водоника у производу на 3Х2 и уклапамо количину од 6 атома тог елемента у сваки члан једначине.
У једначини је нитратни радикал (НО3-) има индекс 2 у производу, трансформишемо индекс у коефицијент у реактанту за 2АгНО3.
Требало је прилагодити количину сребра, јер сада има 2 атома у реагенсима, тако да у производу имамо 2Аг.
У реактантима имамо 4 атома водоника и за уравнотежење овог елемента додајемо коефицијент 2 у производ ХЦл.
Хлор сада има 4 атома у производима, тако да количину у реагенсу прилагођавамо на 2Цл2.
У реактантима имамо 6 атома водоника и за уравнотежење овог елемента прилагођавамо количину воде на 3Х2О.
У реактантима имамо 2 атома угљеника и за уравнотежење овог елемента подешавамо количину угљен-диоксида на 2ЦО2.
Кисеоник мора да има 7 атома у реактантима и да бисмо уравнотежили овај елемент, прилагодимо количину молекуларног кисеоника на 3О2.
Гледајући једначину, нитратни радикал (НО3-) има индекс 2 у производу. Индекс претварамо у коефицијент 2 у реагенсу АгНО3.
У реактантима имамо 2 атома сребра и да бисмо уравнотежили овај елемент, количину сребрног хлорида у производу прилагођавамо на 2АгЦл.
У производу имамо 3 атома калцијума и за уравнотежење овог елемента подешавамо количину калцијум нитрата у реагенсу на 3Ца (НЕ3)2.
Тада нам остаје 6 НО радикала3- у реактантима и да бисмо уравнотежили овај радикал, количину азотне киселине у производима прилагођавамо на 6ХНО3.
Сада у производима имамо 6 атома водоника и да бисмо уравнотежили овај елемент, прилагодимо количину фосфорне киселине у реагенсу на 2Х3ДУСТ4.
Сазнајте више о прорачунима са хемијским једначинама на:
- Балансирање хемијских једначина
- Стехиометрија
- Стехиометријски прорачуни
- Вежбе стехиометрије
- Вежбе периодичног система
