Испаравање то је прелазак из течног стања у гасовито стање. Јавља се на слободној површини течности, полако и постепено, на било којој температури.
Када је супстанца у течном стању, она има мању кохезиону силу између атома него када је у чврстом стању.
У овом стању, молекули су даље раздвојени, у сталном мешању и крећу се унутар течности различитим брзинама.
На тај начин, честице са већом брзином, постизањем слободне површине течности, успевају да побегну прелазећи у гасовито стање.

Брзина испаравања
Постоје фактори који утичу на брзину испаравања, а то су:
- Температура: што је температура виша, брзина испаравања је бржа. Јер што је температура виша, то је већа кинетичке енергије честица. На тај начин ће више честица побећи са површине течности.
- Природа течности: постоје супстанце које лакше испаравају, називају се испарљивим супстанцама. Етар, алкохол и ацетон су примери испарљивих супстанци.
- слободна површина: како се испаравање одвија на слободној површини течности, што је површина већа, већа је количина честица која ће напустити течност.
- Концентрација паре на течности: што је већа количина паре, нижа је стопа испаравања.
- Притисак на течност: што је већи притисак, нижа је брзина испаравања.
Разлика између испаравања и кључања
И испаравање и кипећи представљају промену из течног у гасовито стање. Међутим, док се испаравање одвија постепено, кључање се догађа брзо.
Да би дошло до кључања, течност мора да достигне, за дати притисак, одређену температуру, која се назива тачка кључања. Испаравање се може догодити на било којој температури.
Одвајање смеша
Фракциона кристализација је процес раздвајања хетерогених смеша. Користи се када су супстанце које чине смешу у чврстом стању.
У овом процесу се смеши додаје течност која раствара све чврсте компоненте. Компоненте затим одвојено кристалишу након што раствор испари.
Овај поступак се користи, на пример, у соланама за добијање соли из морске воде.

Испаравање и водени циклус
Испаравање је један од процеса који чине циклус воде. Сунчева енергија загрева слободну површину језера, река, мора и океана.
Ово загревање доводи до испаравања дела воде у парно стање. То се, досезањем највиших слојева атмосфере, хлади и кондензује формирајући облаке.
Када се појаве падавине, вода се враћа на површину у течном облику, инфилтрирајући се у тло и формирајући подземне листове.
Део ове воде апсорбују биљке које транспирацијом враћају водену пару у атмосферу.
фазне промене
Генерично се назива промена из течног у гасовито стање испаравање, јер обухвата, поред испаравања, још два процеса: кључање и загревање.
Постоје и други процеси промене стања. Да ли су они:
- Фузија
- Солидифицатион
- Укапљивање или кондензација
- Сублимација
На доњем дијаграму представљамо три физичка стања материје и одговарајуће промене стања:
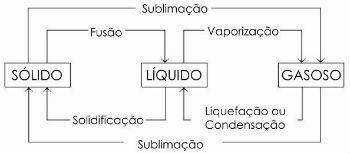
Сазнајте више на: Промене физичког стања.