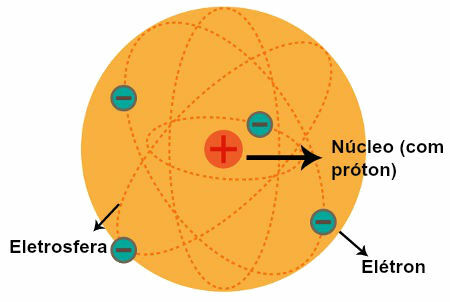
Текст "Молекул са асиметричним угљеником и оптичким изомерима”Показао је да када молекул има само један асиметрични или хирални угљеник (са свим лигандима међусобно различити), има два оптички активна изомера и један оптички неактиван изомер (смеша рацемични).
Хајде сада да размотримо случај да постоје два или више различитих асиметричних угљеника, то јест, они се сматрају различитим међусобно, јер бар један њихов лиганд није исти. На пример, размотрите формулу аспартама, који је 180 пута слађи од сахарозе (шећера) и због тога се користи у вештачким заслађивачима:
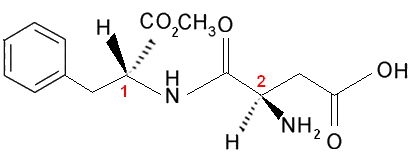
Имајте на уму да овај молекул има два хирална угљеника, која су на слици идентификована бројевима 1 и 2. Ови угљеници имају своје четири групе веза које се међусобно разликују, па се сматрају асиметричним. Када се упоређују угљенични лиганди 1 са оним карбонским 2, видимо да је једини понављајући лиганд Х (водоник), будући да су, према томе, различити асиметрични угљеници.
Овај молекул и сви они који имају два асиметрична угљеника увек ће имати: 4 оптички активна изомера и 2 оптички неактивна изомера (две рацемске смеше).
То знамо јер су могуће вероватноће:

Било који други пар изомера биће дијастереоизомери (који међусобно не представљају зрцалне слике), попут мешавине угљен-десноруке-1 и угљеник-десноруке.
Међутим, било би веома тешко када бисмо морали да наставимо да испитујемо све могућности за сваки молекул, јер многи имају 3, 4, 5 или више асиметричних угљеника.
Дакле, најлакши начин да се утврди количина оптички активних и неактивних изомера молекула који има неколико различити асиметрични угљеникови су кроз доле приказане математичке изразе које су предложили Ван'т Хофф и Ле Бел:
Не заустављај се сада... После оглашавања има још;)
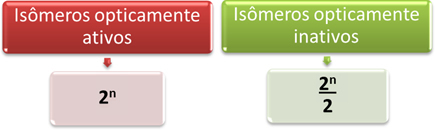
Где је „н“ количина различитих асиметричних угљеника у молекулу. На пример, у случају аспартама, то су два асиметрична угљеника, па имамо:
- Оптички активни изомери: 2не = 22 = 4;
- Оптички неактивни изомери: 2не = 22 = 2.
2 2
Дао је тачно износ који смо раније поменули.
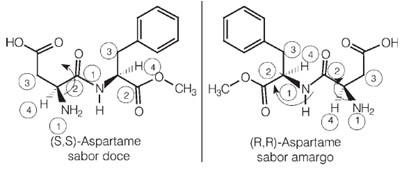
Занимљиво је да један од енантиомера аспартама има овај слаткасти укус који се користи у вештачким заслађивачима, али један од његових оптичких изомера има горак укус.
Сада погледајте још један пример, молекул фруктозе:
ОХ О Х ОХ ОХ ОХ
│ ║ │ │ │ │
Х Ц ─ Ц ─ Ц ─ Ц ─ Ц ─ Ц ─ Х.
│ │ │ │ │
Х ОХ Х Х Х
Фруктоза има три асиметрична атома угљеника, дакле, имамо 8 оптички активних изомера и 4 оптички неактивна изомера, што су 4 рацемске смеше.
- Оптички активни изомери: 2не = 23 = 8;
- Оптички неактивни изомери: 2не = 23 = 4.
2 2
Јеннифер Фогаца
Дипломирао хемију
Да ли бисте желели да се на овај текст упутите у школи или у академском раду? Погледајте:
ФОГАЊА, Јеннифер Роцха Варгас. „Изомери у молекулима са различитим асиметричним угљеницима“; Бразил Сцхоол. Може се наћи у: https://brasilescola.uol.com.br/quimica/isomeros-moleculas-com-carbonos-assimetricos-diferentes.htm. Приступљено 28. јуна 2021.