Валентни слој је последњи слој електронске дистрибуције атома. Како је то најудаљенији слој, уједно је и најудаљенији од атомског језгра.
Према Правило октета, валентној љусци је потребно осам електрона да се стабилизује.
Дакле, атоми добијају стабилност када у валентној љусци имају 8 електрона. То се дешава са племенитим гасовима, они имају комплетан валентни слој. Једини изузетак је елемент Хелијум који има 2 електрона.
Остали елементи треба да направе хемијске везе да би примили нестале електроне и дошли до осам електрона у валентној љусци.
Електрони валентне љуске су ти који учествују у везама, јер су они најекстернији.
Слојеви електросфере
Према Рутхерфорд-Бохровом атомском моделу, електрони се окрећу око атомског језгра, у различитим енергетским слојевима.
Постоји седам слојева означених словима К, Л, М, Н, О, П и К. Свака подржава максималан број електрона.
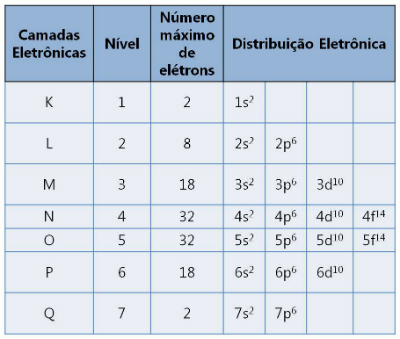 Електронски слојеви и бројеви електрона које подржавају
Електронски слојеви и бројеви електрона које подржавају
Прочитајте такође:
- Боров атомски модел
- Рутхерфорд Атомиц Модел
- Племените гасове
- Правило октета
Како одредити слој Валенсије?
Валентни слој се може одредити на два начина: Елетрониц дистрибуција и Периодни систем.
Да би се одредио валентни слој електронском дистрибуцијом, Дијаграм Линуса Паулинга.
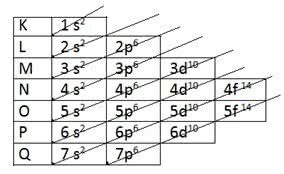 Паулингов дијаграм
Паулингов дијаграм
Подсетимо се да Паулинг-ов дијаграм прати растући редослед енергије. Последњи слој добијен у електронској дистрибуцији је валентни слој.
1с2 2с2 2п6 3с2 3п6 4с2 3д10 4п6 5с2 4д10 5п6 6с2 4ф14 5д10 6п6 7с2 5ф14 6д10 7п6
Дакле, у валентном слоју, најенергичнији подниво је последњи слој.
Примери:
Азот - Н.
Атомски број: 7
Електронска дистрибуција: 1с2 2с2 2п3
Слој Валенсије: 2 с2 2п3, Н има 5 електрона у валентној љусци.
Гвожђе - Фе
Атомски број: 26
Електронска дистрибуција: 1с2 2с2 2п6 3с2 3п6 4с2 3д6
Слој Валенсије: 4 с2, Фе има 2 електрона у валентној љусци.
Хлор - Кл
Атомски број: 17
Електронска дистрибуција: 1с2 2с2 2п6 3с2 3п5
Слој Валенсије: 3 с2 3п5, Цл има 7 електрона у валентној љусци.
Кисеоник - О.
Атомски број: 8
Електронска дистрибуција: 1с2 2с2 2п4
Слој Валенсије: 2 с2 2п4, кисеоник има 6 електрона у валентној љусци.
Угљеник - Ц.
Атомски број: 6
Електронска дистрибуција: 1с2 2с2 2п2
Слој Валенсије: 2 с2 2п2, угљеник има 4 електрона у валентној љусци.
Такође прочитајте о Квантни бројеви.
До сада су коришћени примери са елементима у основном стању. Али исти принцип се може користити за јони, катиони и аниони. Погледајте пример:
Хлорид анион - Цл-
Атомски број хлора је 17. Да је у основном стању, број електрона био би једнак броју протона. Међутим, у овом случају постоји добитак од 1 електрона.
Прво извршите електронску дистрибуцију елемента Хлор:
1с2 2с2 2п6 3с2 3п5
Са појачањем додатног електрона, додајте у последњи слој:
1с2 2с2 2п6 3с2 3п6. Дакле, у валентној љусци има 8 електрона (3с2 3п6).
Погледајте такође: Вежбе о електронској дистрибуцији.
Да би се одредио валентни слој кроз периодни систем, потребно је идентификовати период и породицу елемената.
Дакле, док породица 1А има 1 валентни електрон, 2А има 2 итд. Хемијски елементи садржани у њему породица периодног система имају исти број електрона у валентној љусци.
Међутим, ово важи само за групе 1, 2, 13, 14, 15, 16 и 17 које имају следећи број електрона у валентној љусци 1, 2, 3, 4, 5, 6 и 7, респективно.
За елементе где овај однос није могућ, треба користити електронску дистрибуцију.
Не заборавите! У хемијске везе настају из потребе за стабилизацијом атома и тако формирањем молекула. То се постиже донирањем електрона из валентне љуске који, јер су даље од језгра, имају тенденцију да донирају.
Такође прочитајте о Молекуларна геометрија.
Вежбе
1. Пронађите валентни слој следећих елемената:
Бром
35бр
1с2 2с2 2п6 3с2 3п6 4с2 3д10 4п5
Бромова валентна љуска (породица 7А) има 7 електрона. То је зато што 4с2 и 4п5 припадају слоју Н, док 3д10 припада слоју М.
Алуминијум
13Ал
1с2 2с2 2п6 3с2 3п1
Алуминијумска валентна љуска (породица 3А) има 3 електрона.
2. (УФСЦ) Број електрона у сваком подниву атома стронцијума (38Ср) у растућем редоследу енергије је:
а) 1с2 2с2 2п6 3с2 3п6 4с2 3д10 4п6 5с2
б) 1с2 2с2 2п6 3с2 3п6 4с2 4п6 3д10 5с2
в) 1с2 2с2 2п6 3с2 3п6 3д10 4с2 4п6 5с2
г) 1с2 2с2 2п6 3с2 3п6 4п6 4с2 3д10 5с2
д) 1с2 2с2 2п6 3п6 3с2 4с2 4п6 3д10 5с2
а) 1с2 2с2 2п6 3с2 3п6 4с2 3д10 4п6 5с2
3. (ИФСП / 2013) Број електрона у валентној овојници атома калцијума (З = 20), у основном стању, је
до 1
б) 2
ц) 6
д) 8
е) 10
б) 2
Проверите питања пријемног испита са коментарисаном резолуцијом у: Вежбе на периодном систему.



