Халид је органско једињење које има најмање један атом халогена. - односно хемијски елементи из породице 17 или ВИИ периодног система (Ф, Цл, Бр, И или генерички: Кс) - везан за групу изведену из угљоводоника.
РКС (где је Кс = Ф, Цл, Бр или И)
Неки халогениди су приказани у наставку:

Јод је најреактивнији од свих, а флуор најмање, јер се енергија везивања између халогена и угљеника повећава из правца јода у флуор.
Друга ствар је да се реактивност такође повећава у овом смислу:

Ова реактивност се стога са већом лакоћом јавља код терцијарних халогенида угљеника, због карактера који добија угљеник повезан са органским халидом:

Дакле, супституентну групу, попут ОХ која ће формирати алкохол, снажније привлачи терцијарни угљеник који има позитиван карактер (1+), а супституција је лакша.
Халогениди могу проћи реакције које нам омогућавају да добијемо практично све друге органске функције (алкохол, етар, алкин, цијанид или нитрил, амин, између осталог). Међутим, то је у пракси неизводљиво, јер су халогениди веома скупа једињења.
На пример, да би се створио алкохол, халид у воденој средини реагује са јаком базом, као што је натријум хидроксид. Да видимо пример у наставку, у коме ће се из алкалне хидролизе етил хлорида (хлороетана) формирати етанол:
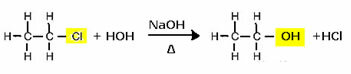
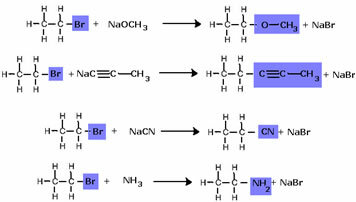
Имајте на уму да је халогенидна група замењена ОХ, алкохолном функционалном групом. Иста шема следи за формирање других група, диференцирајући само реагенс:
Јеннифер Фогаца
Дипломирао хемију
Бразилски школски тим
Извор: Бразил Сцхоол - https://brasilescola.uol.com.br/quimica/reacoes-substituicao-haletos-organicos.htm
