дефинише се као хибридизација унија непотпуних атомских орбитала. Орбитала се класификује као непотпуна када има само једну електрона унутар њега уместо два. Погледајте приказ непотпуне и потпуне орбитале:

На слици А имамо комплетну орбиталу; на слици Б, непотпуна орбитала.
Хибридизација је природни феномен који се јавља код неких хемијских елемената, попут фосфора, сумпора, угљеника итд. Хибридизација угљеника омогућава да атоми овог елемента могу да направе четири хемијске везе, то јест, угљеник ствара само четири везе након што прође феномен хибридизације.
Али зашто се угљеник хибридизује и ствара четири везе? Да бисмо разумели овај феномен, морамо знати електронску дистрибуцију овог елемента:
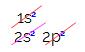
У електронској расподели угљеника видимо да је 1с подниво потпун (са два електрона), 2с је комплетан (са два електрона), а 2п подниво је непотпун (п подниво подржава шест електрона, али постоји само два). Дистрибуирајући 2п електроне на репрезентативан начин, морамо:
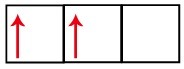
П подниво има три орбитале - у случају угљеника, две су непотпуне, а једна празна. Из овог разлога овај елемент треба да изводи само две везе, јер број непотпуних орбитала увек одређује број веза.
Међутим, када примају енергију из спољне средине, електрони присутни у угљенику се побуђују. Дакле, један од електрона присутних у поднивоу 2с се помера у орбиталу поднивоа п који је био празан:
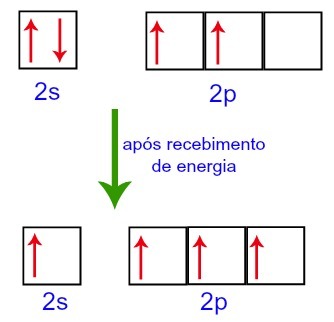
Орбитали угљеника пре и после пријема енергије из спољног окружења
Дакле, угљеник има четири непотпуне орбитале у свом другом нивоу. Потом се орбитала 2с поднивоа спаја са три п орбитале, што конфигурише феномен хибридизација.
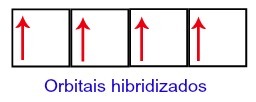
Орбитале угљеника након хибридизације
Ја сам, Диого Лопес Диас
Извор: Бразил Сцхоол - https://brasilescola.uol.com.br/quimica/hibridizacao-carbono.htm
