ти оксиди састоје се од два различита елемента, од којих је један кисеоник, који треба да буде најелектрогативнији од њих.
Номенклатура неорганских оксида следи правила која зависе од тога да ли је оксид молекулски, ковалентни или јонски. Погледајмо сваки случај:
* Номенклатура молекуларних оксида или ковалентне мреже:
Молекуларни или ковалентни мрежни оксиди су они који имају кисеоник везан за а аметал, као што су угљен (Ц), азот (Н), сумпор (С), флуор (Ф), између осталог. Номенклатура ових оксида следи следеће правило:

Правило номенклатуре за оксиде настале са металима
Моно префикс испред елемента повезаног са кисеоником није обавезан.
На пример, имамо следећи молекуларни оксид: ЦО.
- Префикс који означава количину кисеоника: 1 кисеоник: моно;
- оксид;
- Префикс који означава број атома другог елемента: 1 угљеник: моно;
- Назив елемента повезаног са кисеоником: угљеник.
Дакле, ваше име је овако: ЦО = монокарбон моноксид или угљен моноксид.
Погледајте још примера:
угљен-диоксид - ЦО2
Сумпорни триоксид - СО
Дихлоро хептоксид - Цл2О.7
Динитроген моноксид - Н.2О.
Динитроген триоксид - Н.2О.3
Азотни моноксид -НО
Азотни диоксид - НЕ2
Динитроген пентоксид - Н.2О.5
Силицијум диоксид - СиО2
Дифосфор пентоксид - П.2О.5
Сумпорни триоксид - СО3
* Номенклатура јонских оксида:
Јонски оксиди су они који имају кисеоник везан за а метал, као што су гвожђе (Фе), олово (Пб), натријум (На), калцијум (Ца), сребро (Аг), између осталог. Генерално, електрично пуњење кисеоника је -2.
Номенклатура поменута за молекуларне или ковалентне мрежне оксиде такође се тренутно примењује на металне оксиде и сматра се званичном. Погледајте неке примере:
Гвожђе моноксид - ФеО
Оловни моноксид - ПбО
Оловни диоксид - ПбО2
Различити триоксид - Фе2О.3
Међутим, постоји посебна номенклатура за оксиде метала која се још увек широко користи. Заснован је на валенцији елемента повезаног са кисеоником.
Ако елемент има једна валенца, то јест, ако постоји само један начин за везивање кисеоника и формирање само једне врсте оксида, правило именовања даће:

Правило именовања једноструког валентног јонског оксида
Примери:
- Натријум оксид - На2О.
- Калцијум оксид - ЦаО
- калијум оксид - К.2О.
- Алуминијум-оксид - Ал2О.3
- Сребрни оксид - Аг2О.
Али постоје и јонски оксиди настали елементима са више валенција. У овим случајевима, правило именовања је следеће:
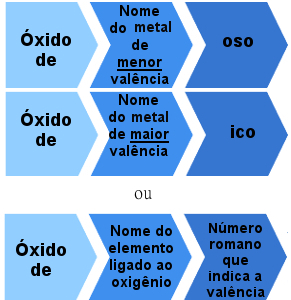
Правило номенклатуре за јонске оксиде са више од једне валенције
Примери:
Фероксид - ФеО
Жељезни оксид - Фе2О.3
Бакарни оксид - Цу2О.
бакар оксид - ЦуО
Или:
Гвоздени оксид ИИ - ФеО (Гвожђе нок = +2)
Гвоздени оксид ИИИ - Фе2О.3 (Гвожђе нок = +3).
Бакров оксид И - Цу2О (гвожђе нок = +1)
Бакров оксид ИИ - ЦуО (гвожђе нок = +2).
Јеннифер Фогаца
Дипломирао хемију
Извор: Бразил Сцхоол - https://brasilescola.uol.com.br/quimica/nomenclatura-dos-oxidos.htm
