Угљоводоници, такође названи водоник карбиди, су органска једињења чији састав има само атоме угљеник (Ц) и од водоник (Х), имајући тако општу формулу Ц.ИксХ.г..
Угљоводоник се састоји од структуре угљеника за коју се атоми водоника везују ковалентна веза.
То је најважније једињење у органској хемији.
Све врсте угљоводоника лако оксидирају, ослобађајући тако топлоту. Већина њих није растворљива у води.
Природни угљоводоници су хемијска једињења настала унутар Земље (удаљене више од 150 км од дубина) при високом притиску и геолошким процесима достижу зоне нижег притиска.
Где се налазе угљоводоници?
Главни извор угљоводоника је нафта. Због тога је угљоводоник присутан у неколико деривата као што су керозин, парафин, природни гас, Бензин, Вазелин, дизел уље, ТНГ (Течни нафтни гас), полимера (попут пластике и гуме), између осталог.
Ово органско једињење чини 48% бразилске енергетске матрице.
Угљенични ланац који чини део састава угљоводоника је четверовалентан, односно може успоставити четири везе.
Угљеник је способан да се веже за друге атоме угљеника и за водонике једноставне везе, дубл или тројке.
Класификација угљоводоника
Класификација угљоводоника се заснива на три специфичности: а облик главног угљеничног ланца, Везе ланаца угљеника, присуство алкил радикала у ланцу угљеника и присуство хетероатома поделу ланца угљеника.
знати више о водоник.
Облик главног угљеничног ланца
С обзиром на облик главног угљеничног ланца, класификација угљоводоника је подељена на алифатски и циклични.
Проверите од чега се састоји сваки од ових облика ланаца угљеника.
алифатски угљоводоници
Алифатски угљоводоници настају угљеничним ланцима отворен или ацикличне. У овим ланцима угљеници су терминали.
Примери:
алкан
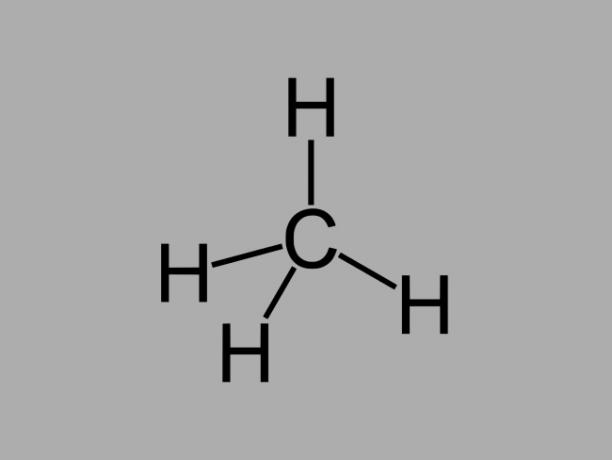
Алкански угљоводоници, такође тзв парафини или парафински, су масна једињења где између угљеника постоје само једноставне везе.
Општа формула за алкан је Ц.неХ2не + 2 (н = било који цео број).
алкен
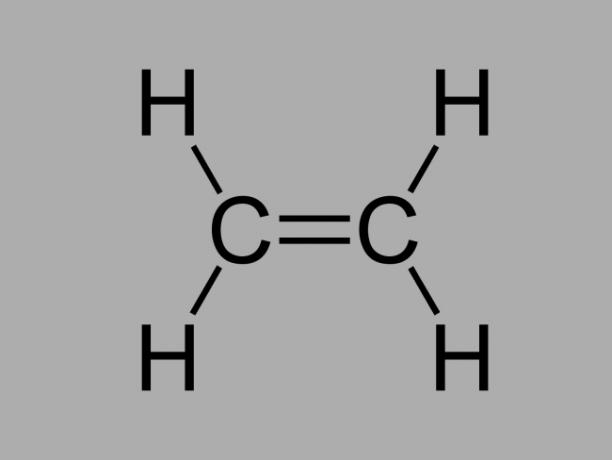
Такође зван олефин, алкен или етилен угљоводоник, алкен је слабо реактивно једињење где постоји двострука веза између угљеника.
Општа формула за алкен је Ц.неХ2не.
алкин
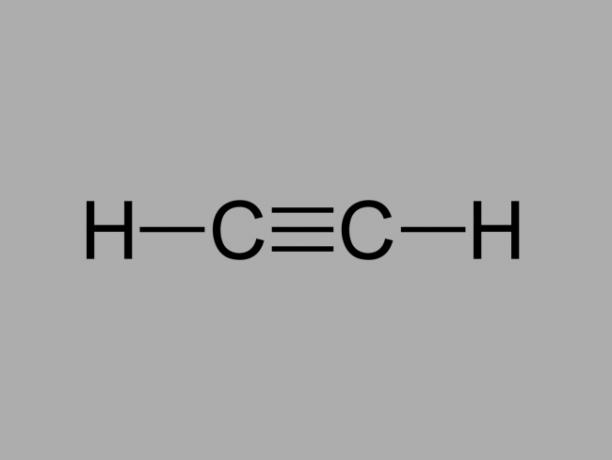
Такође зван метилацетилен, алкин је угљоводоник где су постојеће везе између угљеника троструке.
Општа формула за алкин је Ц.неХ2не-2.
алкадиене

Такође звани диени или диолефини, алкадиени су угљоводоници где су везе између угљеника двоструке.
Општа формула за алкадиен је Ц.неХ2не-2.
Циклични угљоводоници
Циклични угљоводоници настају затвореним или цикличним ланцима угљеника. Ови ланци немају крајње угљенике.
Примери:
Цицлан
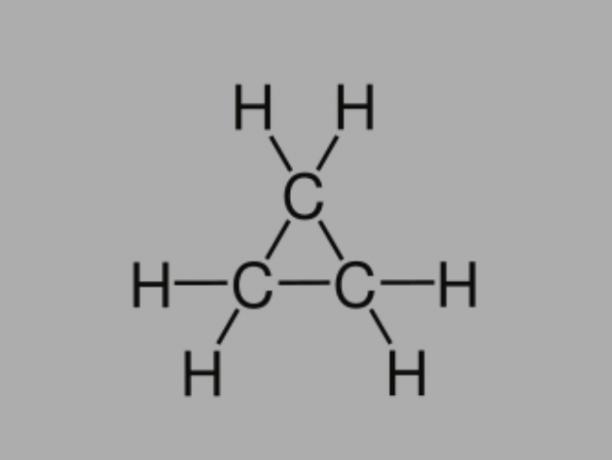
Такође зван циклоалкан, циклопарафин или нафтенски угљоводоник, циклан је засићени угљоводоник, састављен од једноструких веза.
Има затворени ланац угљеника и његова општа формула је Ц.неХ2не.
Циклонски

Такође зван циклоалкенициклини су незасићени угљоводоници, састављени од двоструких веза.
Циклус има затворени ланац угљеника и његова општа формула је Ц.неХ2не−2.
бициклиста
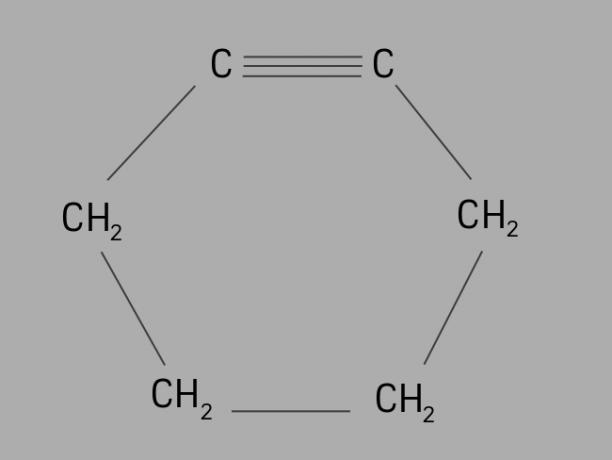
Такође зван циклоалкин или циклоалкин, циклин је циклични и незасићени угљоводоник.
Формиран је затвореним угљеничним ланцем, са троструким везама и његова општа формула је Ц.неХ2не-4.
Ароматична

или

Такође зван арене, ароматични угљоводоници су незасићена једињења настала двоструким везама.
Ароматик има затворени или циклични ланац угљеника и његова општа формула је Ц.6Х.6.
Тип везивања угљеничних ланаца
У зависности од врсте повезаности угљеничних ланаца, угљоводоници се могу класификовати засићен или незасићен.
У наставку погледајте у чему се састоји свака од ових класификација.
Засићени угљоводоници
Засићени угљоводоници настају помоћу једноставне везе.
Примери: алкани, циклани.
незасићени угљоводоници
Незасићени угљоводоници настају помоћу двоструке везе или тројке.
Примери: алкени, алкини, алкадијени.
Присуство алкил радикала
Што се тиче присуства алкилних радикала, угљоводоници могу имати ланац угљеника нормално или разгранати.
нормалан ланац угљеника
Уобичајени угљоводоник угљеничног ланца нема алкил радикале.
Пример: пентан
разгранати ланац угљеника
Када угљоводоник има разгранати ланац угљеника, то значи да његов главни ланац угљеника има алкил радикале.
Пример: метилпропан
Присуство хетероатома који деле ланац угљеника
Секвенцијални ланац угљеника се може или не мора раздвојити у зависности од присуства хетероатома.
Хомогени ланац угљеника
Када угљоводоник има хомогени главни ланац угљеника, то значи да тај ланац није подељен хетероатомима.
Хетерогени ланац угљеника
Ако угљоводоник има хетерогени главни ланац угљеника, овај ланац је имао свој раздвојени ланац угљеника хетероатомом.
Номенклатура угљоводоника
Номенклатура угљоводоника дефинисана је комбинацијом три дела:

Префикс идентификује количину угљеника, средњи идентификује врсту везе, а суфикс означава функцију којој једињење припада (у овом случају класа угљоводоника).
Погледајте доле листу префикса и интермедијара који се комбинују за означавање угљоводоника.
Листа префикса
| Број угљеника | Префикс |
|---|---|
| 1 | Мет- |
| 2 | Ет- |
| 3 | Проп- |
| 4 | Али- |
| 5 | пент- |
| 6 | Хек- |
| 7 | Хепт- |
| 8 | Окт- |
| 9 | Не- |
| 10 | Дец- |
Листа посредника
| Тип конекције | Посредник |
|---|---|
| Само појединачни позиви | -ан- |
| Пар | -ен- |
| троструко | -у- |
| два пара | -диен- |
Погледајте неке примере именовања угљоводоника.
Примери:
ЦХ3 - ЦХ2 - ЦХ2 - ЦХ3
У горњој структурној форми можемо видети једињење од 4 угљеника које има само једноструке везе (означено симболом „-“).
- Префикс за 4 угљеника = али-
- Интермедијар за појединачне везе = -ан-
- Суфикс угљоводоника = -о
Погледајте да унија префикс + средњи + суфикс рађа име БУТАНЕ.
ЦХ2 = ЦХ2
Горе наведени структурни облик има 2 угљеника и 1 двоструку везу (означен симболом „=“).
- Префикс за 2 угљеника = ет-
- Интермедијар за двоструке везе = -ен-
- Суфикс угљоводоника = -о
Погледајте да унија префикс + средњи + суфикс рађа име ЕТХЕНЕ.
ЦХ2 = ЦХ - ЦХ2 - ЦХ3
ЦХ3 - ЦХ = ЦХ2 - ЦХ3
Имајте на уму да оба горе наведена структурна облика имају 4 угљеника и 1 двоструку везу (означена симболом „=“).
Тако имамо:
- Префикс за 4 угљеника = али-
- Интермедијар за двоструке везе = -ен-
- Суфикс угљоводоника = -о
Погледајте да унија префикс + средњи + суфикс дало би порекло имену БУТЕНЕ за два структурна облика.
Међутим, имајте на уму да структурни облици нису идентични, тако да и номенклатуре не могу бити исте.
Разлика између два структурна облика лежи у месту двоструке везе.
У овом случају угљенике у ланцу морамо нумерисати од краја најближег двоструком. Према томе, у предметним случајевима морамо бројати слева надесно.
У ЦХ2 = ЦХ - ЦХ2 - ЦХ3:
- ЦХ2 биће 1
- ЦХ ће бити 2
- ЦХ2 биће 3
- ЦХ3 ће бити 4
Имајте на уму да двострука веза је између угљеник 1 то је угљеник 2.
Морамо користити најмањи број (1) да бисмо пронашли двоструку везу: БУТЕНЕ -1
У ЦХ3 - ЦХ = ЦХ2 - ЦХ3:
- ЦХ3 биће 1
- ЦХ ће бити 2
- ЦХ2 биће 3
- ЦХ3 ће бити 4
Имајте на уму да је двострука веза између угљеник 2 то је угљеник 3.
Морамо користити најмањи број (2) да бисмо пронашли двоструку везу: БУТЕН -2
Према ИУПАЦ (Међународна унија чисте и примењене хемије - Међународна унија за чисту и примењену хемију), место треба назначити мало пре налази се (у случају горе наведених структурних формала, двострука веза, представљена интермедијером „-Ен-“).
Уз то, имамо други начин, који је успут најтачније, писање номенклатуре доступних структурних облика.
ЦХ2 = ЦХ - ЦХ2 - ЦХ3: БУТЕНЕ -1 или БУТ-1-ЕНО (тачнији облик)
ЦХ3 - ЦХ = ЦХ2 - ЦХ3: БУТЕНЕ -2 или БУТ-2-ЕНЕ (тачнији облик)
Сазнајте више о ИУПАЦ и номенклатура.



