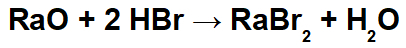Једно реакција супституције заснива се на размени између компонената два различита реагенса. Већа је вероватноћа да ће овај процес проћи једињења са већом стабилношћу (засићена, односно само једноставним везама између угљеника). Међутим, и бензен то може.
То знамо у структури бензен постоје три двоструке везе (три пи везе), то јест, ово једињење је незасићено, али ови двојници све време пролазе кроз феномен резонанце (наизменичног смештаја положаја три пи везе). Из тог разлога, његова структура има већу стабилност, јер везе пролазе кроз све угљенике.
Реакције супституције које се могу јавити у бензену су:
Халогенизација;
Нитрација;
Сулфонирање;
Алкилација;
Ацилација.
а) Халогенизација
У овој реакцији бензен делује у интеракцији са халогенима (Бр2, Цл2 Хеј!2), увек уз присуство катализатора, који може бити неорганска со (АлЦл3, ФеЦл3 и ФеБр3). Процес се одвија разменом бензен водоника за атом халогена. Резултат је настајање органског халогенида и халогени хидрид. Погледајте пример:
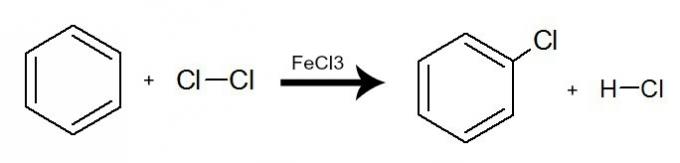
Једначина која представља халогенирање бензена употребом молекуларног хлора (Цл2)
б) Нитрација
У овој реакцији бензен делује у интеракцији са азотном киселином (ХНО3), увек уз присуство катализатора сумпорне киселине (Х.2САМО4) и грејање. Процес се одвија изменом водоника из бензена за НО групу2 киселине. Резултат је формирање а нитро једињење и воде.
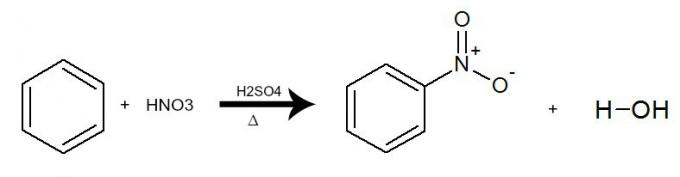
Једначина која представља нитрирање бензена употребом азотне киселине
в) Сулфонизација
У овој реакцији бензен делује у интеракцији са сумпорном киселином (Х2САМО4), увек уз присуство катализатора сумпор-триоксида (СО3) и грејање. Процес се одвија изменом водоника из бензена СО групом3Х киселине. Резултат је формирање киселина сулфонска и воде.
Не заустављај се сада... После оглашавања има још;)
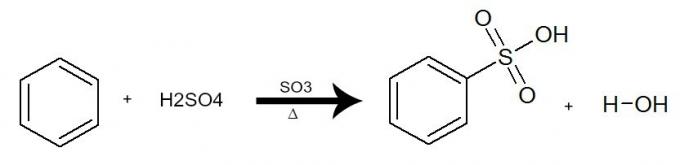
Једначина која представља сулфонацију бензена употребом сумпорне киселине
г) алкилација
У овој реакцији бензен делује у а органски халид (Р-Кс), увек уз присуство катализатор алуминијум трихлорид (АлЦл3) и грејање. Процес се одвија разменом водоника из бензена са Р групом (органским супституентом) из халогенида. Резултат је настајање разгранатог ароматичног угљоводоникаи неорганска киселина (ХКС).
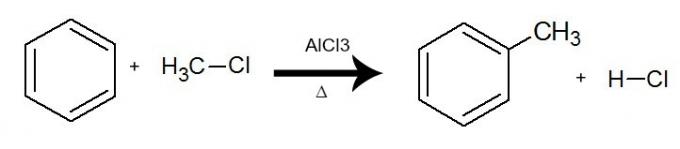
Једначина која представља алкилацију бензена употребом хлора метана
е) Ацилација
У овој реакцији бензен делује у интеракцији са халидом киселине, који може бити представљен етаноил хлоридом:
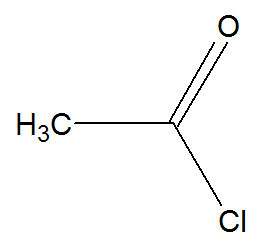
Структурна формула етаноил хлорида
Реакција се дешава у присуству катализатор алуминијум трихлорид (АлЦл3) и долази до размене једног водоника из бензена за целу халогенидну киселинску групу (са изузетком Кс-халогена). Резултат је формирање а кетон и неорганска киселина (ХКС). Погледајте пример:
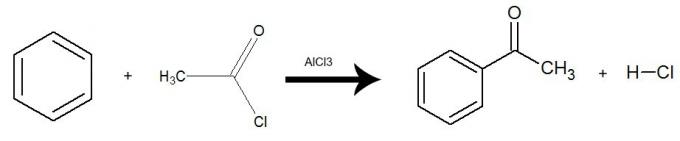
Једначина која представља ациловање бензена употребом етаноил хлорида
Ја сам, Диого Лопес Диас
Да ли бисте желели да се на овај текст упутите у школи или академском раду? Погледајте:
ДАНИ, Диого Лопес. „Реакције супституције у бензену“; Бразил Сцхоол. Може се наћи у: https://brasilescola.uol.com.br/quimica/reacoes-substituicao-no-benzeno.htm. Приступљено 27. јуна 2021.
Хемија

Ароматична једињења, арени, поларитет, нерастворљиви, растворљиви, неполарни растварачи, етар, тетрахлорид угљеника, угљоводоници, инсектициди, боје, растварачи, експлозиви, канцерогени, толуен, метилбензен, лекови, лепак постолар.
Хемија

Кликните овде и сазнајте више о реакцији супституције, хемијском процесу у којем коришћени реагенси (органски и неоргански) међусобно размењују једну од својих компонената, формирајући нове супстанце. Међу супстанцама које се највише користе као реагенси су алкани, бензен и органски халогениди.