У реакције сагоревања присутни су у многим аспектима нашег свакодневног живота. На пример, главни извори производње енергије настају сагоревањем или сагоревањем одређених горива, попут етанола, бензина, угља, између осталог. Даље, енергија која нам је потребна да преживимо и радимо резултат је реакција сагоревања које се одвијају у нашим ћелијама када „сагоревамо“ храну коју једемо.
Али шта је потребно да би се дошло до реакције сагоревања?
Потребне су три ствари:
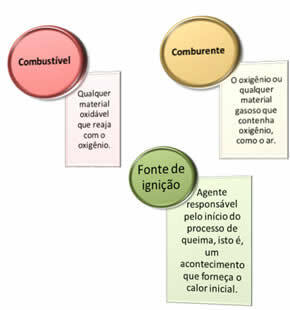
Ова три фактора чине ватрени троугао, јер када реакција сагоревања започне, ослобођена енергија одржава реакцију и омогућава јој да се настави све док гориво, оксиданс или топлота (ослобођена енергија) не нестану. То значи да ће постојати Ланчана реакција.
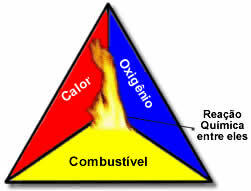
На пример, ако неко баци запаљену цигарету у шуму, биће пожар (реакција сагоревања). У овом случају, Буш то је гориво, О. кисеоник присутан у ваздуху атмосферски је оксидант то је цигарета осветљен је био извор паљења. Ово сагоревање ће се наставити док се не елиминише један од три фактора. Ако ватрогасци баце воду, врућина ће бити елиминисана. Али чак и ако се ништа не предузме да заустави ово сагоревање, оно ће се завршити у неком тренутку, односно када гориво (коров) понестане.
Као што је већ поменуто, у тим реакцијама се ослобађа топлота, па је сагоревање егзотермна реакција. Међутим, ова врста реакције је непотпуно сагоревање. Да бисте разумели зашто, погледајте разлику између потпуног и непотпуног сагоревања:
Не заустављај се сада... После оглашавања има још;)
Потпуно сагоревање:
Анализирајући органска једињења као горива, морамо:
| ТХЕ потпуно сагоревање настаће када се угљеников ланац прекине и сви атоми угљеника у угљеничном ланцу потпуно оксидирају. |
| ти формирани производи угљоводоницима ће бити ЦО2 (угљен-диоксид) и Х.2О. (Вода). |
Посматрајте потпуно сагоревање изоктана, који је једна од компоненти бензина.
Ц8Х.18 (г) +25/2 О.2 (г) → 8 ЦО2 (г) + 9 ам2О.(1)
Непотпуно сагоревање
| У овом случају нема довољно оксиданса, односно довољно кисеоника да сагори цело гориво. |
| Дакле, настали производи су ЦО (угљен моноксид) и Х.2О.. |
Примети исто сагоревање изоктана, међутим, сада непотпуно:
Ц8Х.18 (г) + 17/2 О.2(г) → 8 ЦО (г) + 9 ам2О.(1)
Пример је паљење шума, јер се резултирајуће емисије састоје од ЦО и одређених материја, попут чађи (Ц), као и пепела и других једноставних и сложених органских једињења. Азотни оксид, озон и алдехиди такође могу настати као резултат секундарних реакција због присуства других компонената у ваздуху.
Ц8Х.18 (г) + 9/2 О.2 (г) → 8Ц (г) + 9 ам2О.(1)
Јеннифер Фогаца
Дипломирао хемију
Бразилски школски тим
Да ли бисте желели да се на овај текст упутите у школи или у академском раду? Погледајте:
ФОГАЊА, Јеннифер Роцха Варгас. „Потпуно и непотпуно сагоревање“; Бразил Сцхоол. Може се наћи у: https://brasilescola.uol.com.br/quimica/combustao-completa-incompleta.htm. Приступљено 27. јуна 2021.