У реакције хидратације у алкадиенес су реакције сабирања, односно компоненте (хидронијум и хидроксид) молекула воде додају се у алкадиен.
ти алкадиенес су угљоводоници који имају отворен ланац и две двоструке везе (формиране сигмом и пи) између угљеника, као што можемо видети у следећој структури:

Структурна формула алкадиена
за реакција хидратације у алкадиенима неопходно је да се веза пи, присутна у двострукој вези, прекине под утицајем топлоте и сумпорне киселине (Х2САМО4). Прекидом пи везе настају два места везе, свако на једном од угљеника укључених у двоструку везу.

Појава места везивања уз поремећај везивања пи
Појава места везивања на молекулу алкадиена неопходна је за јоне (Х+ и ох-) из воде додају се алкадиену, формирајући, на пример, алкохол (алкохол са два хидроксила).
Додатак Х.+ и ох- у структури алкадиене
БЕЛЕШКА: Додатак Х.+ и ох- у алкадиенској структури следи Владавина Марковникова, односно Х.+ везује се за највише хидрогенизовани угљеник и ОХ- везује се за мање хидрогенизовани угљеник.

Пример примене правила Марковникова у хидратацији алкадиена
Како постоје различите врсте алкадиена у односу на положај двоструких веза, може бити да хидратација алкадиена ствара различита једињења. Погледајте следеће случајеве:
→ Акумулирани или згуснути алкадиен
То је алкадиен који има две двоструке везе које истовремено укључују три атома угљеник, односно не постоји једнострука веза која раздваја угљенике који су укључени у везе дубл.

Структурна формула нагомиланог алкадиена
Током реакције хидратације наизменичног алкадиена, пи везе су прекинуте, Х је+ додат хидрогенизованим угљенима и ОХ- додаје се мање хидрогенизованим угљенима:
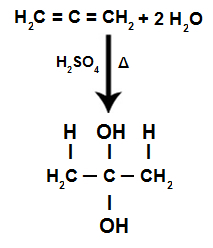
Једначина реакције хидратације алкадиенеа
Имамо да у хидратацији акумулираног алкадиена, исти атом угљеника прима два хидроксила, формирајући двоструки алкохол, који је нестабилна структура.

Структура алкохола близанца
Како је двојаки алкохол нестабилан, имамо формирање молекула воде са компонентама два хидроксила и стварање пи везе између угљеника и кисеоника.
Не заустављај се сада... После оглашавања има још;)

Стварање кетона из двојаког алкохола
Због тога ће реакција хидратације нагомиланих алкадиена резултирати стварањем а кетон.
→ Коњуговани или алтернативни алкадиен
То је алкадиен који има две двоструке везе које истовремено укључују четири атоми угљеника, односно постоји једнострука веза која раздваја угљенике који су укључени у везе дубл.
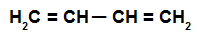
Структурна формула наизменичног алкадиена
У наизменичним алкадијенима долази до резонанције њихових двоструких веза. Дакле, електрони пи везе мењају положај (црвене стрелице), као на следећем дијаграму:
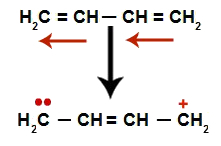
Шема која приказује резонанцу у наизменичном алкадиену
Генерално, имамо појаву двоструке везе тачно између угљеника где су претходно била два двојника стварање два места за везу, по једно на сваком угљенику који више не ствара двоструку везу (у примеру, угљеници 1 и 4). Угљеници 1 и 4 ланца добијају Х.+ и ох- из воде.

Делимична хидратација у наизменичном алкадиену
После резонанције, пи веза нове двоструке везе се прекида, а Х.+ и ох- додају се молекулу алкадиена. ОХ се додаје угљенику најближем првој додатој ОХ групи јер подлеже електронској привлачности групе која је електронегативнија.

Престанак хидратације у наизменичном алкадиену
Због резонанце кажемо да је наизменични алкадиен подвргнут 1,4-хидратацији, формирајући диалкохол.
→ Алкадиене изоловани
То је алкадиен који има две двоструке везе које укључују најмање пет атома истовремено. угљеника, односно постоје најмање две појединачне везе које раздвајају угљенике који су укључени у везе. дубл.

Структурна формула изолованог алкадиена
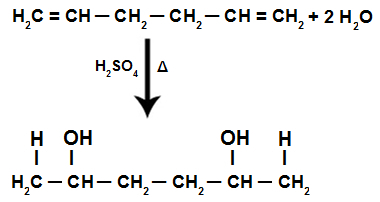
Током реакције хидратације изолованог алкадиена, пи везе су покидане, Х.+ додат хидрогенизованим угљенима и ОХ- додата у мање хидрогенизоване угљенике.

Изолована једначина реакције хидратације алкадиена
Због тога, уз додатак изолованог алкадиена, имамо само формирање дијаалкохола.
Ја сам, Диого Лопес Диас
Да ли бисте желели да се на овај текст упутите у школи или академском раду? Погледајте:
ДАНИ, Диого Лопес. „Реакције хидратације у алкадиенима“; Бразил Сцхоол. Може се наћи у: https://brasilescola.uol.com.br/quimica/reacoes-hidratacao-alcadienos.htm. Приступљено 28. јуна 2021.