активни изомери или оптички активни изомери (ИОА) су молекули одређене хемијске супстанце који могу да изврше поларизацију и одступање план светло десно или лево. Да бисте проверили да ли нека супстанца има активне изомере, само проверите да ли у њеној структурној формули постоји асиметрични угљеник:

Анализирајући ланац представљен на горњој слици, можемо видети да централни угљеник има четири различита лиганда (ОХ, Х, ЦХ3 и Цл), што га чини а угљеник асиметрична, који се називају и угљеник хирални. Дакле, кад год ланац има један или више хиралних угљеника, биће активних изомера.
ти врсте активних изомера(ИОА) су:
Дешњак: Активни оптички изомер који савија поларизовану светлост удесно;
Левогиро: Активни оптички изомер који савија поларизовану светлост улево.
Посматрање: Присуство асиметричног угљеника у структурној формули указује на то да супстанца мора имати леворотациони изомер и декросротациони изомер. Није на нама да знамо на који начин је светлост била скренута, јер присуство хиралног угљеника већ сведочи о овој чињеници. Увек је половина постојећих молекула леворука, а друга половина деснорука.
Леворуки и десноруки молекули било које органске супстанце увек имају иста физичка својства (тачка топљење, тачка кључања, густина, растворљивост итд.), али представљају хемијске активности (понашање у организму) многи различити. Пример је адреналин. У телу делује само молекул адреналина левогира, док декстрогира не.
Не заустављај се сада... После оглашавања има још;)
Погледајте сада структурну формулу супстанце бутан-2-ол да бисте проверили да ли има активне изомере или не:
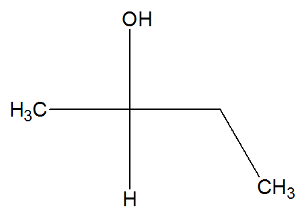
У структури бутан-2-ола можемо приметити да угљеник 2 има четири различита везива (ОХ, Х, ЦХ3, ЦХ2-ЦХ3), па је хирални угљеник и представљен је десно окретно активни изомер и други леворотациони активни изомер.
Прорачун активних изомера (ИОА)
Холандски хемичар Јацобус Хенрицус ван'т Хофф развио формулу која омогућава израчунавање колико активних изомера (ИОА) може дати нека супстанца. Погледајте:
ИОА: 2не
н: је број хиралних угљеника у структурној формули супстанце.
Следите два примера примене Вант'т Хоффове формуле:
5-Дихлоро-2,3-дихидрокси-хександиојска киселина

У структурној формули једињења постоје три хирални угљеници или асиметрични, дакле:
ИОА = 2не
ИОА = 23
ИОА = 8
2,3,4,5-тетрахидроксихексанал

У структурној формули једињења постоје четири хирални угљеници (црвене стрелице) или асиметрични, дакле:
ИОА = 2не
ИОА = 24
ИОА = 16
Посматрање: Постоји могућност да структурна формула има два асиметрична угљеника која имају потпуно исте лиганде. Ако се то догоди, у прорачунима узимамо у обзир само 1 за вредност н, а не 2. Погледајте пример:
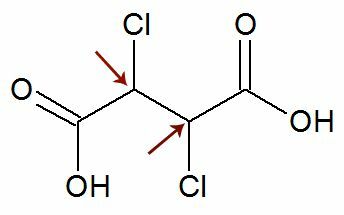
Као два хирална угљеника су једнако, сматрамо само једним угљеник у прорачуну:
ИОА = 2не
ИОА = 21
ИОА = 2
Ја сам, Диого Лопес Диас
Да ли бисте желели да се на овај текст упутите у школи или у академском раду? Погледајте:
ДАНИ, Диого Лопес. „Активни изомери“; Бразил Сцхоол. Може се наћи у: https://brasilescola.uol.com.br/quimica/isomeros-ativos.htm. Приступљено 27. јуна 2021.
