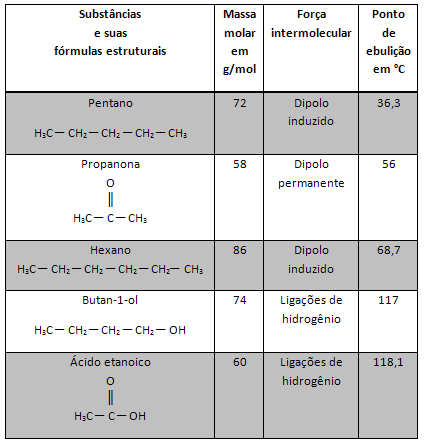
Питања о хемијске ваге у Енем-у врло се понављају. Имајући ово на уму, креирали смо овај материјал који доноси најважније теме о овој грани физичке хемије обухваћене Државним средњошколским испитом (Енем).
Међу питањима која се односе на хемијску равнотежу имамо константу равнотеже у смислу концентрације у мол / Л и у смислу притиска, константа јонске равнотеже, константа јонизације, помак равнотеже, пХ и пОХ, константа хидролизе, пуфер и константа растворљивост.
Међу горе описаним субјектима, неки од њих добијају већу важност у Енем-у:
Промена равнотеже
Константа јонизације
пХ
слана хидролиза
Видео лекција о хемијској равнотежи у Енем-у
1. Промена равнотеже у Енему
1.1- (Енем 2015) Хипоксија или болест висине састоји се од смањеног кисеоника (О2) у артеријској крви тела. Из тог разлога, многи спортисти доживљавају нелагоду (главобоље, вртоглавица, отежано дисање) приликом вежбања физичке активности на великим висинама. Под овим условима доћи ће до смањења концентрације оксигенираног хемоглобина (ХбО2) у равнотежи у крви, према односу:
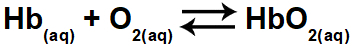
До промене концентрације оксигенираног хемоглобина у крви долази због:
а) повишење крвног притиска.
б) пораст телесне температуре.
в) смањење температуре околине.
г) пад парцијалног притиска кисеоника.
е) смањење количине црвених крвних зрнаца.
Кисеонични хемоглобин (ХбО2) налази се у реактантима (десна страна) једначине. Вежба поставља питање која би од опција довела до промене оксигенираног хемоглобина у крви, односно померала би равнотежу лево или десно.
а) Нетачно. Повећани проток крви нема никакве везе са повећаним крвним притиском.
б) Нетачно. Температура не мења равнотежу.
в) Нетачно. Температура не мења равнотежу.
г) Тачно. Смањењем парцијалног притиска кисеоника смањује се количина оксигенираног хемоглобина, померајући равнотежу улево.
д) Нетачно. Пад броја црвених крвних зрнаца довешће до пада како броја хемоглобина, тако и кисеоничних хемоглобина.
1.2- (Енем 2011) Безалкохолна пића постају све више и више мета јавних здравствених политика. Производи од лепка садрже фосфорну киселину, супстанцу штетну за фиксацију калцијума, минерала који је главна компонента матрице зуба. Каријес је динамичан процес неравнотеже у процесу денталне деминерализације, губитка минерала услед киселости. Познато је да је главна компонента зубне глеђи сол која се назива хидроксиапатит. Сода, присуством сахарозе, смањује пХ биофилма (бактеријски плак), узрокујући деминерализацију зубне глеђи. Одбрамбеним механизмима пљувачке треба 20 до 30 минута да нормализују ниво пХ, реминерализујући зуб. Следећа хемијска једначина представља овај процес:

С обзиром на то да особа свакодневно конзумира безалкохолна пића, може доћи до процеса деминерализације зуба као резултат повећане концентрације:
а) ОХ-, који реагује са Ца јонима2+, померање равнотеже удесно.
б) Х.+, који реагује са ОХ хидроксилима-, померање равнотеже удесно.
ц) ОХ-, који реагује са Ца јонима2+, померајући равнотежу улево.
д) Х.+, који реагује са ОХ хидроксилима-, померајући равнотежу улево.
е) Ца2+, који реагује са ОХ хидроксилима-, померајући равнотежу улево.
Прави одговор: Слово Б.
Резолуција
Процес деминерализације помера равнотежу удесно. Када особа пије соду, она уноси кисели материјал, то јест, повећава количину Х.+ у средини. Х+ брзо ступа у интеракцију са ОХ- равнотеже, смањујући количину ОХ-. На тај начин се равнотежа помера удесно, деминерализујући зуб.
1.3- (Енем-2013) Један од корака у третману воде је дезинфекција, а хлорисање је најчешће коришћена метода. Ова метода се састоји од растварања гаса хлора у раствору под притиском и наношења у воду која се дезинфикује. Укључене једначине хемијске реакције су:

Дејством дезинфекције контролише се хлороводонична киселина која има потенцијал дезинфекције око 80 пута већи од хипоклорит аниона. ПХ средине је важан јер утиче на то у којој мери се хлороводонична киселина јонизује. Да би дезинфекција била ефикаснија, пХ воде која се третира мора бити ближи:
а) 0
б) 5
ц) 7
д) 9
е) 14
Прави одговор: Слово Б.
Према тексту, најбоље дезинфекционо дејство врши супстанца ХЦлО. Према томе, свако тумачење и закључак мора бити усмерено ка начину добијања ове супстанце.
Супстанца ХЦлО је присутна у другој равнотежи, па је занимљива тактика померање ове равнотеже улево. За ово, према принцип Ле Цхателиер-а, имамо могућност да повећамо количину Х.+ (додавањем киселе супстанце, пХ мање од 7) или повећати количину Цл-.
Значајно је да у првој једначини постоји још једна хемијска равнотежа која представља ХЦлО врсту-, који има афинитет са Х.+, померајући равнотежу улево. Ово је потез који не желимо.
Због тога морамо користити кисели пХ (испод 7). Међутим, овај пХ не би требало да буде превише кисео да би се избегло пуно Х катиона.+ у средини.
Погледајте такође:Хемијска равнотежа у пећинама
2. пХ и хидролиза физиолошког раствора у Енем-у
2.1- (Енем-2017) Процесом екстракције из биљака се може добити неколико природних производа. Лапацхол је из класе нафтокинона. Његова структура има енол хидроксил (пКа = 6,0) који омогућава изоловање овог једињења из пиљевине ипе екстракцијом одговарајућим раствором, праћеном једноставном филтрацијом. Узмимо у обзир да је пКа = -лог Ка и да је Ка киселинска константа реакције јонизације лапацхол-а.

Које решење треба користити за ефикасније издвајање лапахола из ипе пиљевине?
а) На раствор2ЦО3 да се формира сол лапахола.
б) Раствор пуфера сирћетне киселине / натријум ацетата (пХ = 4,5).
в) раствор НаЦИ у циљу повећања јонске снаге медијума.
г) На раствор2САМО4 да би се формирао јонски пар са лапаколом.
е) ХЦИ раствор како би се екстраховао киселинско-базном реакцијом.
Изјава указује да је пКа супстанце 6,0. Ова вредност пКа мора се користити у изразу пКа:
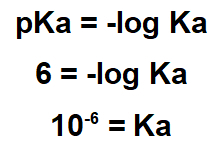
Како је ваш Ка мали, лапацхол је кисела супстанца, па је за његово уклањање корисно користити основну супстанцу.
истинска. Сол је основна, јер потиче из јаке базе (јер је из породице ИА), и ЦО3 потиче од слабе киселине (Х.2ЦО3).
б) Нетачно. Раствор пуфера је кисео и потребна нам је база.
в) Нетачно. НаЦл је неутрална со, јер потиче из јаке базе (јер је из породице ИА), а Цл долази из јаке киселине (ХЦл).
г) Нетачно. У2САМО4 је неутрална со, јер На потиче из јаке базе (јер је из породице ИА), и СО4 потиче од јаке киселине (Х.2САМО4).
лажно је. ХЦл је киселина и потребна нам је база.
2.2- (Енем- 2014) У циљу минимизирања утицаја на животну средину, бразилско законодавство утврђује да хемијски остаци испуштени директно у тело пријема имају пХ између 5,0 и 9,0. Водени течни отпад настао у индустријском процесу има концентрацију хидроксилних јона 1,0.10-10 мол / Л. Да би се придржавао законских прописа, хемичар је раздвојио следеће супстанце доступне у складишту компаније: ЦХ3КОО, На2СО4, ЦХ3ОХ, К.2ЦО3 и НХ4Кл.
Не заустављај се сада... После оглашавања има још;)
Да би се остатак пустио директно у тело које прима, која супстанца би могла да се користи за подешавање пХ?
а) ЦХ3ЦООХ
б) У2САМО4
ц) ЦХ3ох
д) К.2ЦО3
е) НХ4Кл
Прави одговор: Слово Д.
Резолуција
Корак 1: Одредити пХ остатка.
Вежба показује да остатак има концентрацију хидроксида једнаку 10-10.
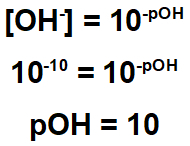
Стога можемо израчунати пХ овог остатка:

Из горе наведеног имамо да остатак има кисели карактер, јер је његов пХ мањи од 7. Стога је за његову неутрализацију неопходно користити супстанцу основног карактера.
Корак 2: Одредите карактер сваке соли да бисте назначили која је основна, као ЦХ3ЦООХ (алтернатива а) је киселина, а ЦХ3ОХ (алтернатива ц) је алкохол органске класе киселог карактера.
б) Неутрална сол, јер На потиче из јаке базе (јер је из породице ИА), а СО4 потиче од јаке киселине (Х.2САМО4).
г) Основна со, јер К потиче из јаке базе (јер је из породице ИА), и ЦО3 потиче од слабе киселине (Х.2ЦО3).
д) Киселинска со, као НХ4 потиче из слабе базе (НХ4ОХ), а Цл потиче од јаке киселине (ХЦл).
2.3- (Енем- 2014) Истраживач примећује да је налепница на једној од тегли у којој држи концентрат дигестивних ензима нечитка. Не зна који ензим чаша садржи, али сумња да је у питању желучана протеаза, која делује на стомак тако што пробавља протеине. Знајући да је варење у желуцу кисело, а црево основно, он саставља пет епрувета са храном различито, додајте концентрат ензима у растворе са утврђеним пХ и сачекајте да видите да ли ензим делује у било ком њихов. Епрувета у којој ензим мора деловати да би указао на исправност хипотезе истраживача је она која садржи:
а) коцка кромпира у раствору са пХ = 9.
б) комад меса у раствору са пХ = 5.
в) кувано бело јаје у раствору са пХ = 9.
г) део јуфке у раствору са пХ = 5.
д) лоптица путера у раствору са пХ = 9.
Прави одговор: Слово Б.
Вежба захтева од ученика добру интерпретацију и корелацију са биохемијским познавањем намирница. Обавештава да истраживач мисли да је ензим пробавни, делује на кисели пХ и делује на протеине (јер је протеаза).
Ако овај ензим делује у киселом окружењу, пХ мора бити мањи од 7. Месо се састоји од протеина, док тестенине чине угљени хидрати. Дакле, тачан одговор је алтернатива б.
2.4- (Енем- 2012) Домаћица је случајно испустила воду из одмрзавања рибе у фрижидеру, што је оставило јак и непријатан мирис унутар уређаја. Познато је да је карактеристичан мирис рибе због амина и да се ова једињења понашају као база. У табели су наведене концентрације водоника неких материјала који се налазе у кухињи, а које домаћица размишља да користи приликом чишћења фрижидера.

Међу наведеним материјалима, који су прикладни за ублажавање овог мириса?
а) Алкохол или сапун
б) Лимунов сок или алкохол
в) Лимунов сок или сирће
г) Лимунов сок, млеко или сапун
д) Сапун или сода / сода пепео
Прави одговор: Слово Ц.
Резолуција
Вежба предлаже проблематичну ситуацију у којој фрижидер домаћице има јак мирис изазван супстанцом основне природе. Стога се поставља питање који би материјали били занимљиви за решавање овог проблема.
Да бисте неутралисали базу, потребно је користити материјал киселе природе или са пХ нижим од 7. Како су вежбе дале вредности концентрација Х+ материјала било је довољно да се сваки користи у доњем изразу:

Тако:
Сок: пХ = 2
Млеко: пХ = 6
Сирће: пХ = 3
Алкохол: пХ = 8
Сапун: пХ = 12
Цев: пХ = 12
Кисели карактер су сок, сирће и млеко. Дакле, само алтернатива ц доноси материјале киселе природе.
3. Константа равнотеже у Енему
3.1- (Енем-2016) Након потпуног хабања, гуме се могу спалити за производњу електричне енергије. Међу гасовима који настају у потпуном сагоревању вулканизоване гуме, неки су загађивачи и изазивају киселе кише. Да би се спречило њихово бекство у атмосферу, ови гасови се могу мехурићи претворити у водени раствор који садржи одговарајућу супстанцу. Узмите у обзир податке о супстанци наведеним у доњој табели:

Међу супстанцама наведеним у табели, она која је у стању да најефикасније уклања загађујуће гасове је (а)
а) фенол.
б) пиридин.
ц) метиламин.
г) калијум хидроген фосфат.
д) калијум хидроген сулфат.
Прави одговор: Слово Д.
Резолуција
Вежба представља проблематичну ситуацију у којој загађујући гасови промовишу киселу кишу. Затим пита која би од поменутих супстанци била занимљива за неутралисање ових гасова и, сходно томе, избегавање киселих киша.
Да би се избегле киселе кише, кисели гасови морају се неутралисати основним раствором. Супстанце са овом карактеристиком су оне које преференцијално ослобађају ОХ групе- у средини. У табели су пиридин, метиламин и калијум хидроген фосфат основне супстанце.
Дакле, да бисмо утврдили супстанцу која је у стању да ефикасније уклања загађујуће гасове, морамо анализирати вредност јонизационе константе. Што је константа већа, већа је и способност ослобађања ОХ-. Дакле, калијум хидроген фосфат је најпогоднија супстанца у овом случају.
3.2- (Енем-2015) Неколико киселина се користи у индустријама које отпадне воде одлажу у водена тела, попут река и језера, што може утицати на еколошку равнотежу. Да би се неутралисала киселост, у отпадне воде се може додати калцијум-карбонатна сол у одговарајућим количинама, јер она производи бикарбонат, који неутралише воду. Представљене су једначине укључене у процес:

На основу вредности константи равнотеже реакција ИИ, ИИИ и ИВ, на 25О. Ц, колика је нумеричка вредност константе равнотеже реакције И?
а) 4,5к10-26
б) 5к10-5
в) 0,8к10-9
г) 0,2к105
д) 2.2к1026
Прави одговор: Слово Б.
Резолуција
Ова вежба подразумева сталну јонизацију. У почетку је неопходно схватити да је једначина И заправо резултат (збир) једначина ИИ, ИИИ и ИВ. Стога, да бисмо покренули резолуцију, морамо се користити принципима Хесс-ов закон.
Корак 1: Употреба Хесс-овог закона.
Инвертујући једначину ИИ и задржавајући једначине ИИИ и ИВ, имамо:
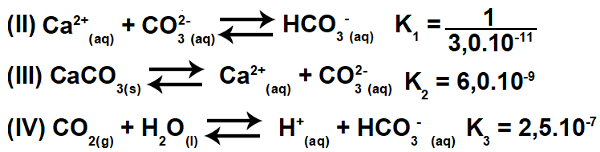
Овим можемо уочити да анион ЦО3-2 и Х катион+ ће бити елиминисани, а збир једначина резултираће једначином И.
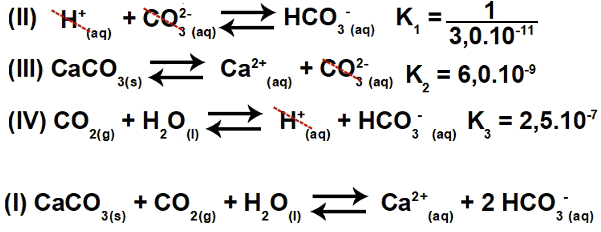
Корак 2: стални прорачун
Константа равнотеже једначине јонизације увек се даје множењем константи осталих једначина:

Ја сам, Диого Диас