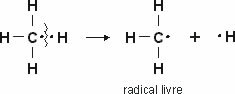
У реакције сабирањау алкени(угљоводоници који имају двоструку везу између два атома угљеника), пи веза између два угљеника се прекида и сваки од угљеника се везује за нови атом. Погледајте:
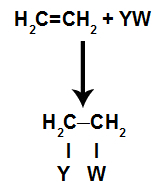
Општи шематски модел адиционе реакције
Принципи реакције сабирања
а) Прекид пи везе
Пи веза се лако прекида јер је слабија веза од сигме везе. Међутим, да би се то догодило, неопходно је да алкен буде подвргнут условима који омогућавају овај поремећај. Након прекида пи везе између два угљеника, место везивања (за нове атоме) увек се појави на сваком од угљеника.
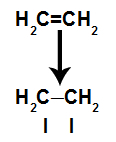
Шема која приказује прекид пи везе
б) Услови за раскидање пи везе
Фактори који фаворизују прекид пи везе су:
Употреба катализатора;
Грејање;
Присуство киселине у реакционом медијуму.
ц) Појава реакције адиције
Везна места створена након прекида пи-везе увек ће заузимати атоми реактанта који се налази у истом контејнеру као и алкен. Реакција додавања је добила име по типу реагенса помешаног са алкеном.
Врсте реакција сабирања у Алкенима
а) Хидрогенација
Алкен се помеша са гасовитим водоником (Х
2) у контејнеру и подвргнут дејству чврстог катализатора (никл, платина или паладијум) и загревању (Δ).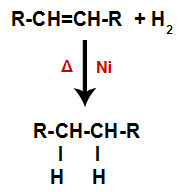
Општа шема реакције хидрогенирања у алкенима
Присуство катализатора и загревање узрокују пи везу алкена и сигма везу између водоника Х2 бити брже сломљен. Тиме имамо стварање два места везивања у алкену и два слободна атома водоника у реакционом медијуму.

Стварање места везивања и раздвајања атома
Тако, одмах након тога, сваки слободни атом водоника заузима једно од места везивања насталих у алкену. Како супстанца која настаје има само угљенике и водонике, као и само једноставне везе између угљеника, то је а алкан.
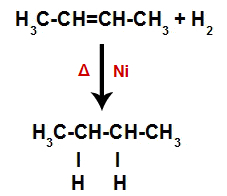
Једначина која представља стварање алкана у хидрогенизацији
Б) Халогенизација
Алкен је помешан са једноставним супстанцама (Ф2, Цл2, бр2 Хеј!2) формиран од халогени (хлор, флуор, јод и бром) у контејнеру и подвргнут дејству светлости (λ) и загревању (Δ).

Општа шема реакције халогенирања у алкенима
Деловање светлости и загревање брже прекидају везу алкена и сигма везу између супстанци насталих халогеном. Овим добијамо два места везивања у алкену и два слободна атома халогена у реакционом медијуму.
Не заустављај се сада... После оглашавања има још;)

Стварање места везивања и раздвајања атома
Тако, одмах након тога, сваки слободни атом халогена заузима једно од места везивања насталих у алкену. Како настала супстанца има халоген повезан са структуром која се састоји од угљеника и водоника, то је а органски халогенид.

Једначина која представља стварање органских халида у халогенизацији
ц) Хидратација
Алкен се помеша са водом (Х.2О) у контејнеру и подвргнут дејству катализатора (у овом случају сумпорне киселине).
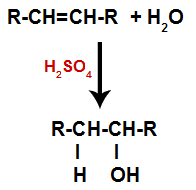
Општа шема реакције хидратације у алкенима
Присуство сумпорне киселине у реакцији чини да се брже прекидају веза алкена и сигма веза између водоника (Х) и хидроксила (ОХ) воде. Тиме имамо стварање два места везивања у алкену и једног слободног водоника и једног хидроксила у реакционом медијуму.
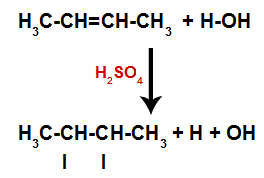
Стварање места везивања и раздвајања атома
Тако, убрзо након тога, водоник и хидроксил заузимају једно од места везивања насталих у алкену. Како се формирана супстанца веже за засићени угљеник (ствара само једноставне везе), то је алкохол.
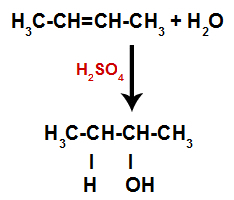
Једначина која представља стварање алкохола у хидратацији
г) Додавање водоник-халогенида
Алкен се у контејнеру помеша са халогенираном анорганском киселином (ХФ, ХИ, ХЦл, ХБр).

Општа шема реакције киселинских халида у алкенима
Присуство киселине у реакцији доводи до бржег пуцања пи везе алкена. Појединачна веза у киселини је прекинута јер се ове супстанце природно јонизују. Тако се у алкену стварају два места везивања и у реакционом медијуму је присуство слободног водоника и халогена.
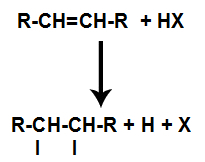
Стварање места везивања и раздвајања атома
Тако, убрзо након тога, водоник и халоген заузимају једно од места везивања насталих у алкену. Како настала супстанца има халоген повезан са структуром која се састоји од угљеника и водоника, то је органски халид.
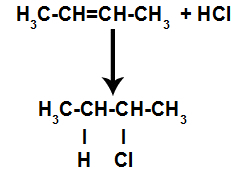
Једначина која представља стварање органских халида у халогенизацији
Ја сам, Диого Лопес Диас
Да ли бисте желели да се на овај текст упутите у школи или у академском раду? Погледајте:
ДАНИ, Диого Лопес. „Реакције адиције у Алкенима“; Бразил Сцхоол. Може се наћи у: https://brasilescola.uol.com.br/quimica/reacoes-adicao-alcenos.htm. Приступљено 28. јуна 2021.
Хемија

Алкани, угљоводоници, метан, засићени ланац, алифати, парафини, горива, бензин, минерални восак, нафта, уљни шкриљац, природни гас, петрохемијска индустрија.
Хемија

Алкени, гас, етен, етилен, пластика, синтетичка гума, боје, синтетичке тканине, експлозиви, нафтни крекинг, полиетилен, олефиантни гас, олефини, угљоводоници, ланац ациклични угљен-диоксид.
Алкини, етични угљоводоници, ацетиленски угљоводоници, ациклични ланац угљеника, ланац угљеника хомогени, незасићени ланац угљеника, трострука веза, ПВЦ, ПВА, ацетилен, синтетичка гума, пластика, жице текстила.