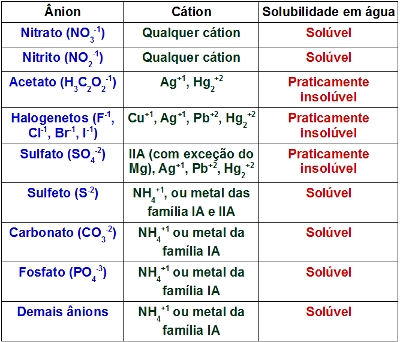
Анализа физичких и хемијских својстава једињења која спроводе ковалентне везе (дељењем електрона) показује нам да постоје велике разлике између ових материјала. Али пре него што погледамо саме ове карактеристике, погледајмо која је разлика између молекуларних и ковалентних супстанци.
У молекуларне супстанце они су они који настају када су атоми повезани ковалентним везама, дајући молекуле одређеног броја.
Међутим, ковалентна веза такође може да произведе једињења у мрежној структури са врло великим и неодређеним бројем атома, који су макромолекуле. Такве супстанце се називају ковалентна једињења или чврсте супстанце ковалентне мреже. Неки примери ових једињења су: дијамант (Ц), графит (Ц), силицијум диоксид (СиО2) и силицијум-карбид (СиЦ).
Сада, погледајмо његова главна својства:
- Физичко стање на собној температури: У амбијенталним условима налазе се молекуларна и ковалентна једињења у три физичка стања (чврста, течна и гасна).
Примери:
О. Чврст: шећер (сахароза), силицијум диоксид (песак), дијамант, графит;
О. Течност: вода, ацетон, етанол;
О. Гасовит: Водоник-сулфид, гас хлора, гас бром, гас водоник.

- Тачка топљења и кључања: Генерално, тачке топљења и кључања ових супстанци су мањи од оних код јонских супстанци.
Ковалентне супстанце имају више температуре кључања од молекуларних, увек изнад 1000 ° Ц. То је зато што како су њихови молекули тесније повезани, стварајући кристалне решетке, неопходно је обезбедити више енергије да би их натерали да промене своје стање.
Два фактора ометају тачке кључања и топљења ковалентних и молекуларних једињења: а моларна маса и интермолекуларна сила.
Не заустављај се сада... После оглашавања има још;)
Што је већа моларна маса, већа је инерција молекула и, сходно томе, већа је тачка кључања и топљења. Ако се моларне масе приближе, посматрамо интермолекуларне силе. Најинтензивнија интермолекуларна сила је сила водоничног везивања, што доводи до више тачке кључања и топљења. Интермедијар је трајни дипол, а најслабији, што доводи до ниже тачке кључања и топљења, је индуковани дипол.
- Електрична струја: У свом чистом облику, и течности и чврсте материје не проводе електричну струју.
Изузетак је графит који проводи електричну струју у чврстом облику, јер његови електрони са двоструком везом резонирају и због тога имају одређену покретљивост.
- Растворљивост: Полари се растварају у поларе, а неполари се растварају у неполаре.
- Истрајност: Отпорност ковалентних супстанци на удар или механички удар је мала. Генерално, то су крхке чврсте материје, као што је приказано у случају стакла које чине натријум и калцијум силикати.

- Жилавост: Генерално, имају високу тврдоћу. Изузев графита, јер су његови атоми угљеника повезани са још три атома угљеника, чинећи хексагоналне плоче са одређеном покретљивошћу, чинећи га меким. Због тога се чак користи и као мазиво.
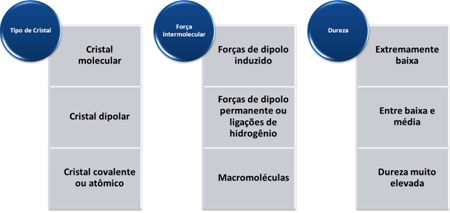
Тврдоћа ових супстанци варира у зависности од врсте кристала, као што је приказано у доњој табели:
Јеннифер Фогаца
Дипломирао хемију
Да ли бисте желели да се на овај текст упутите у школи или у академском раду? Погледајте:
ФОГАЊА, Јеннифер Роцха Варгас. „Особине ковалентних и молекуларних једињења“; Бразил Сцхоол. Може се наћи у: https://brasilescola.uol.com.br/quimica/propriedades-dos-compostos-covalentes-moleculares.htm. Приступљено 28. јуна 2021.
Јонска једињења, главне карактеристике јонских једињења, веза између јона, коначни пренос електрона, електростатичке привлачне силе између јона, негативних и позитивних јона, ањони, катиони, јонска веза, молекуларна структура он