Besedilo Reakcije seštevanja je pokazala, da so te vrste organskih reakcij poimenovane na ta način, ker se organski molekuli doda reaktant, ki prekine vezi med ogljiki. V tem besedilu je bil prikazan primer alkenov, tukaj bomo že razmislili, kako se to dogaja z alkini, oz torej s tistimi ogljikovodiki (ki jih tvorijo samo atomi ogljika in vodika), ki imajo vez trojna.
Ranljiva točka alkinov je ravno trojna vez, pri kateri se lahko vezi tipa pi (π) pretrgajo (dodatek delno) ali dvakrat (skupni dodatek) in povzroči nastanek novih spojin z dvojnimi (alkeni) ali enojnimi vezmi (alkani).
Oglejmo si primere adicijskih reakcij v alkinih:
1. Dodajanje vodika ali hidrogeniranje:
V tem primeru molekula H2 se doda alkinu z uporabo katalizatorja, ki je običajno nikelj v prahu (Ni), platina (Pt) ali paladij (Pd). Zaradi potrebe po uporabi katalizatorja se imenuje tudi ta reakcija katalitsko hidrogeniranje in se pojavlja v fazah: v prvi fazi dobite alken, v drugi fazi, ki je počasnejši, pa alkan.
Če je katalizator močan, na primer nikelj in platina, reakcija neposredno tvori alkan. Paladij zmešan z BaSO
4 je šibek katalizator in proizvaja alken. Možno je uporabiti tudi delni zaviralec katalizatorja, da dosežemo samo alken. Ta reakcija poteka tudi pri visokih tlakih in temperaturah.Nato dodamo vodik etanu, pri čemer nastane etilen in nato etan:

2. Dodajanje halogenov ali halogeniranja:
Alkinska pi vez se pretrga in molekuli dodamo dva atoma halogena (elementi iz družine 17A periodnega sistema, najpogosteje uporabljeni: Cl2 in Br2), ki tvori vicinalni dihalid, kar pomeni, da sta dva atoma halogena vezana na sosednje atome ogljika. Reakcija se lahko nadaljuje, pretrga drugo pi vez in molekuli doda še dva atoma halogena.
V spodnjem primeru imamo poleg podkupnine še to vrsto:
KlCl ClKl
││ ││
H ─C ≡ C CH3 + Kl2 → H ─ C ═ C CH3 + Kl2 → H ─ C ─ C CH3
││
KlKl
ALCINO DI-HALETTE TETRAHALETE
3. Dodajanje vodikovih halogenidov (halogenhidridi ali hidrohalogeniranje):
Tu se alkinu doda vodikov halid, lahko pa tudi delni in popolni dodatek. Pomemben vidik te vrste reakcije je, da sledi Pravilo Markovnikova, to pomeni, da se vodik veže na bolj hidrogenirano ogljik (z več atomi vodika), halogen pa na manj hidrogeniran ogljik.
Pri celotnem hidrohalogeniranju nastane gemični dihalid, to je spojina, ki ima na isti ogljik dva atoma halogena.
Ne ustavi se zdaj... Po oglaševanju je še več;)
Pazi:
HBr Hbr
││ ││
H ─C ≡ C CH3 + HBr → H ─ C ═ C CH3 + HBr → H ─ C ─ C CH3
││
Hbr
GEMIČNI DI-HALOGID ALCINO HALIDA
Pomemben primer te vrste reakcije je tista, ki se pojavi, ko se etinu doda vodikov klorid, ki tvori kloroeten ali vinil monoklorid, ki je monomer, ki tvori polimer polivinilklorida, bolj znan po svoji kratici PVC.
HClHKl
││ ││
H ─C ≡ C ─ H + HCl → H ─ C ═ C ─ H + HCl → H ─ C ─ C ─ H
││
HKl
ETHINO KLOROETEN 1,1-DIKLOROETAN
(PVC monomer)
PVC je snov, ki se v industriji pogosto uporablja za izdelavo različnih izdelkov, kot so sandali, stekleničke z zdravili, medicinski pripomočki, plastične hlače za dojenčke, torbe, žične prevleke, igrače, oblazinjenje pohištva, oblazinjenje avtomobilov, dežni plašči, plastični čevlji, vinilne plošče, tla, embalažne folije, cevi, ki se uporabljajo v vodovodnih ceveh in kanalizacija itd.
4. Dodatek vode (hidracija):
V tej reakciji voda reagira z alkinom in sprva tvori enol, ki se molekularno preuredi in spremeni v aldehid (v primeru alkinov, manjših od acetilena). Enol in aldehid ostajata v dinamičnem ravnovesju s prevladujočim aldehidom. To je primer Dinamična konstitucikonalna izomerija ali tavtomerija.
Primer:

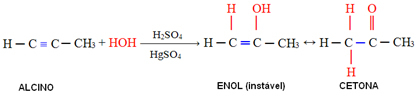
Pri alkinih, večjih od acetilena, se upošteva pravilo Markovnikova in enol povzroči keton:
Avtorica Jennifer Fogaça
Diplomiral iz kemije