Ob reakcije izgorevanja prisotni so v mnogih pogledih našega vsakdana. Na primer, glavni viri pridobivanja energije so posledica zgorevanja ali izgorevanja nekaterih goriv, kot so etanol, bencin, oglje, med drugim. Poleg tega je energija, ki jo potrebujemo za preživetje in delo, rezultat reakcij izgorevanja, ki potekajo v naših celicah, ko hrano, ki jo zaužijemo, "zažgemo".
Toda kaj je potrebno, da imamo reakcijo zgorevanja?
Potrebne so tri stvari:
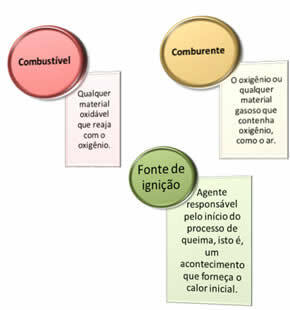
Ti trije dejavniki tvorijo ognjeni trikotnik, kajti ko se reakcija izgorevanja začne, sproščena energija ohrani reakcijo in ji omogoči, da se nadaljuje, dokler gorivo, oksidant ali toplota (sproščena energija) ne izgine. To pomeni, da bo Verižna reakcija.
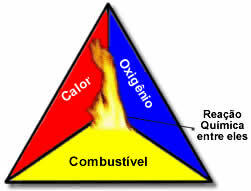
Na primer, če nekdo v gozd vrže prižgano cigareto, bo prišlo do požara (reakcija zgorevanja). V tem primeru je Bush to je gorivo, O kisik v zraku atmosferski je oksidant to je cigaret prižgana je bila vir vžiga. To gorenje se bo nadaljevalo, dokler se ne odpravi eden od treh dejavnikov. Če gasilci vržejo vodo, bo toplota odpravljena. A tudi če se nič ne ustavi, da bi se to gorenje ustavilo, se bo na neki točki končalo, torej ko zmanjka goriva (gozda).
Kot smo že omenili, se pri teh reakcijah sprošča toplota, zato je izgorevanje eksotermna reakcija. Vendar je ta vrsta reakcije nepopolno zgorevanje. Če želite razumeti, zakaj, poglejte razliko med popolnim in nepopolnim zgorevanjem:
Ne ustavi se zdaj... Po oglaševanju je še več;)
Popolno zgorevanje:
Če analiziramo organske spojine kot goriva, moramo:
| THE popolno zgorevanje zgodilo se bo, ko bo ogljikova veriga prekinjena in bodo vsi ogljikovi atomi v ogljikovi verigi popolnoma oksidirani. |
| Ti oblikovani izdelki z ogljikovodiki bo CO2 (ogljikov dioksid) in H2O (Voda). |
Opazujte popolno zgorevanje izoktana, ki je ena od komponent bencina.
Ç8H18 (g) +25/2 O.2 (g) → 8 CO2 (g) + 9.002O(1)
Nepopolno zgorevanje
| V tem primeru ni dovolj oksidanta, to je dovolj kisika, da bi pokurilo vse gorivo. |
| Tako nastali izdelki so CO (ogljikov monoksid) in H2O. |
Opazite enako zgorevanje izoktana, vendar zdaj nepopolno:
Ç8H18 (g) + 17/2 O.2(g) → 8 CO (g) + 9.002O(1)
Primer je zgorevanje gozdov, saj nastale emisije sestavljajo CO in določene snovi, kot so saj (C), pa tudi pepel in druge enostavne in zapletene organske spojine. Dušikov oksid, ozon in aldehidi lahko nastanejo tudi kot posledica sekundarnih reakcij zaradi prisotnosti drugih komponent v zraku.
Ç8H18 (g) + 9/2 O.2 (g) → 8C (g) + 9.002O(1)
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Brazilska šolska ekipa
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
FOGAÇA, Jennifer Rocha Vargas. "Popolno in nepopolno zgorevanje"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/combustao-completa-incompleta.htm. Dostop 27. junija 2021.