Kisline in baze so dve med seboj povezani kemijski skupini. Gre za dve snovi velikega pomena, ki sta prisotni v vsakdanjem življenju.
Kisline in baze preučuje Anorganska kemija, veja, ki preučuje spojine, ki jih ne tvori ogljik.
Pojmi o kislinah in osnovah
Arrenijev koncept
Eden prvih konceptov kislin in baz, ki ga je v poznem 19. stoletju razvil švedski kemik Svante Arrhenius.
Po Arrheniusu so kisline snovi, ki v vodni raztopini trpijo ionizacija, sprošča kot kation samo H +.
HCl (vodna) → H+ (aq) + Cl- (tukaj)
Baze so medtem snovi, ki trpijo ionska disocijacija, pri čemer se kot edina vrsta aniona sproščajo ioni OH- (hidroksil).
NaOH (aq) → Na+ (vodno) + OH- (tukaj)
Vendar je bil Arrheniusov koncept kislin in baz omejen na vodo.
Preberite tudi o: Arreniusova teorija in Nevtralizacijska reakcija.
Koncept Bronsted-Lowry
Koncept Bronsted-Lowry je širši od Arrheniusovega in je bil uveden leta 1923.
Po tej novi definiciji so kisline snovi, ki lahko dajo proton H+ drugim snovem. In baze so snovi, ki lahko sprejmejo H-proton+ drugih snovi.
Se pravi kislina je darovalec protona, baza pa protonski receptor.
Označuje a močna kislina kot tista, ki popolnoma ionizira v vodi, torej sprošča ione H+.
Snov pa je lahko amfiprotična, to je sposobna se obnašati kot kislina ali Bronstedova baza. Poglejte primer vode (H2O), amfiprotična snov:
HNO3(aq) + H2O(l) → NE3- (vodno) + H3O+(aq) = Bronstedova baza, sprejela je proton
NH3(aq) + H2O(l) → NH4+(aq) + OH-(aq) = Bronsted kislina, darovana protona
Poleg tega se snovi obnašajo kot konjugirani pari. Vse reakcije med kislino in a osnova Bronsteda vključujejo prenos protona in imajo dva konjugirana kislinsko-bazična para. Glej primer:
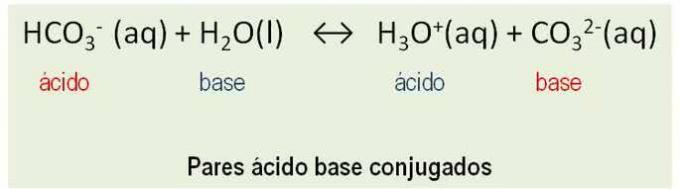
HCO3- in CO32-; H2O in H3O+ so konjugirani pari kislinskih baz.
Izvedite več o:
- Anorganske funkcije
- Kislinsko-bazični kazalniki
- Titracija
Nomenklatura kislin
Za opredelitev nomenklature so kisline razdeljene v dve skupini:
- Hidracidi: kisline brez kisika;
- Oksiakisline: kisline s kisikom.
Hidracidi
Nomenklatura se pojavlja na naslednji način:
kislina + ime elementa + hidrik
Primeri:
HCl = klorovodikova kislina
HI = hidriodna kislina
HF = fluorovodikova kislina
oksiacidi
Nomenklatura oksidnih kislin upošteva naslednja pravila:
Ti standardne kisline vsake družine (družine 14, 15, 16 in 17 periodnega sistema) upoštevajte splošno pravilo:
kislina + ime elementa + ic
Primeri:
HClO3 = klorovodik
H2SAMO4 = žveplova kislina
H2CO3: ogljikova kislina
Za druge kisline, ki se tvorijo z istim jedrnim elementom, jih poimenujemo glede na količino kisika po naslednjem pravilu:
| Količina kisika glede na standardno kislino | Nomenklatura |
|---|---|
| + 1 kisik | Kislina + na + ime elementa + ico |
| - 1 kisik | Kislina + ime elementa + kost |
| - 2 kisika | Kislina + hipo + ime elementa + kost |
Primeri:
HClO4 (4 atomi kisika, en več kot običajna kislina): klorovodikova kislina;
HClO2 (2 atoma kisika, en manj kot standardna kislina): klorovodikova kislina;
HClO (1 atom kisika, dva manj kot standardna kislina): klorovodikova kislina.
Morda vas bodo zanimali tudi: žveplova kislina
Osnovna nomenklatura
Za osnovno nomenklaturo se upošteva splošno pravilo:
Ime hidroksida + kation
Primer:
NaOH = Natrijev hidroksid
Ko pa isti element tvori katione z različnimi naboji, se na koncu imena z rimskimi številkami doda število naboja iona.
Ali pa lahko najmanj napolnjenem ionu dodate pripono -oso, najbolj naelektrenemu ionu pa pripono -ico.
Primer:
Železo
Vera2+ = Fe (OH)2 = Železov hidroksid II ali železov hidroksid;
Vera3+ = Fe (OH)3 = Železov hidroksid III ali železov hidroksid.
Ne pozabite preveriti vprašanj o sprejemnem izpitu na to temo s komentirano resolucijo v: Vaje na anorganske funkcije.
