Klor je kemični element s simbolom Cl, atomsko število 17, atomska masa 35,5. Spada v družino halogenov, skupina 17 ali 7A, in v tretje obdobje periodnega sistema.
Njegovo ime izhaja iz grščine kloros, kar pomeni zelenkasto. To je zato, ker je v normalnih pogojih temperature in tlaka za klor značilno, da je zelenkasto rumen plin z močnim vonjem.
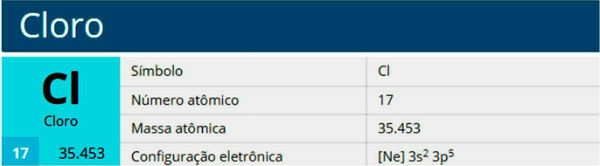
Lastnosti
Klor je leta 1774 odkril švedski znanstvenik Carl Wilhelm Scheele (1742-1786). Takrat pa sem verjel, da gre za spojino s kisikom. Leta 1810 je Humphry Davy (1778-1829) dokazal, da gre za nov kemični element.
Ker gre za izredno reaktiven element, ga v naravi skorajda ni mogoče najti v čisti obliki, z izjemo majhne količine, ki se med vulkanskimi izbruhi odda v obliki HCl.
Tako ga običajno najdemo v obliki natrijevega klorida (NaCl), znanega tudi kot kuhinjska sol. V mineralih se pojavlja v obliki karnalita in silvita.
Dobite ga lahko tudi elektroliza NaCl, v vodni raztopini. Klor v procesu kloridov proizvaja tudi veliko soli iz kloridov oksidacija.
Izvedite več, preberite tudi:
- Periodična tabela
- Kemični elementi
- Halogeni
aplikacij
Plinski klor (Cl2) je strupen in draži, zaradi česar je bil med 1. svetovno vojno uporabljen kot kemično orožje. Ta plin povzroča draženje dihalnih poti in kože, zadrževanje vode v pljučih, solzenje in vdihavanje v velikih količinah lahko privede do smrti.
Nekatere druge uporabe klora so:
- Beljenje papirja in tkanin z uporabo klorovega dioksida (ClO2).
- Priprava vode, dodajanje klora, naredi vodo pitno in primerno za prehrano ljudi. Ta postopek se imenuje kloriranje in uporablja klorovodikovo kislino (HClO).
- Dezinfekcija vode v bazenu in industrijskih odpadkov, saj je klor sposoben ubiti mikroorganizme.
- Proizvodnja plastičnih spojin, kot sta PVC (polivinilklorid) in sintetična guma.
- Proizvodnja nekaterih vrst organskih in anorganskih spojin.