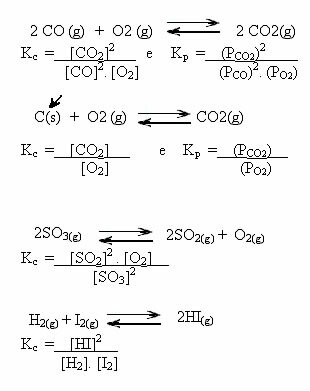
Nevtralizirajoča reakcija se pojavi, ko kislina reagira z bazo in tvori vodo in sol. Kislina zagotavlja ione H+ in osnova zagotavlja ione OH- za tvorjenje vode (H2O):
1 uro+(tukaj) + 1 OH-(tukaj) → H2O(ℓ)
Ta vrsta reakcije se imenuje "nevtralizacija", ker je nevtraliziran pH medija; pH vode je 7,0 (nevtralno).
Da bi se te reakcije pojavile, je treba sprostiti določeno količino toplote, saj je le del energije z ioni tvorijo vezi, ki povzročajo molekule vode, medtem ko se preostala energija sprošča v čisto. Ta sproščena energija se imenuje Nevtralizacijska entalpija (∆Hnevtralizacija).

Ne ustavi se zdaj... Po oglaševanju je še več;)
Ker sprošča toploto, ustreza eksotermnim reakcijam, pri katerih bo entalpija (globalna energija sistema) vedno negativna, manjša od nič.
V primeru reakcije med močnimi kislinami in močnimi bazami bo vrednost nevtralizirajoče entalpije vedno enaka - 13,8 kcal / mol ali - 57,7 kJ / mol. To se zgodi, ker so baze in močne kisline popolnoma ločene v raztopini in so zato edine Reakcija, ki je odgovorna za pojav toplote, bo nastanek vode, kot je prikazano v spodnjih treh primerih:
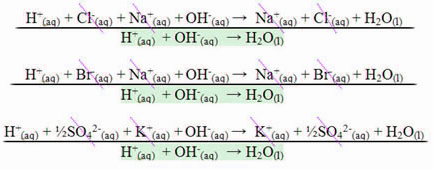
V primeru nevtralizacijskih reakcij, ki vključujejo šibke kisline ali baze, bo vrednost nevtralizirajoče entalpije manjša od –57,7 kJ / mol.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
FOGAÇA, Jennifer Rocha Vargas. "Entalpija nevtralizacije"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/entalpia-neutralizacao.htm. Dostopno 28. junija 2021.