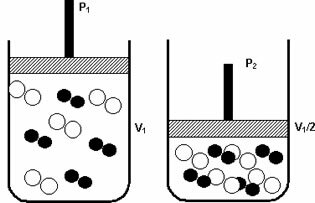
Spodaj si oglejte generično reverzibilno reakcijo, kjer male črke ustrezajo uravnoteženim reakcijskim koeficientom, velike črke pa so reaktanti, vsi proizvodi pa plinasti:

Upoštevajoč vsako od smeri reakcije posebej, so njihove stopnje razvoja (Td) podane z:
* Neposredna reakcija: aA + bB → cC + dD
Vseneposredno = Kneposredno. [THE]The. [B]B
* Povratna reakcija: cC + dD → aA + bB
Vseinverzno = Kvzvratno. [Ç]ç. [D]d
Kemijska ravnotežna konstanta glede koncentracije v količini snovi (Kç) in glede na parcialni tlak (KP) bo podano z delitvijo Kneposredno avtor Kvzvratno.
Torej imamo:
Kneposredno. [THE]The. [B]B = 1 → Kneposredno__ = __[Ç]ç. [D]d___
Kvzvratno. [Ç]ç. [D]d Kvzvratno [THE]The. [B]B
Biti, Kç =_Kneposredno_
Kvzvratno
Torej imamo:
Kç =__[Ç]ç. [D]d___ ali KP =__(Praça)ç. (pD)d___ |
Kjer je p delni tlak vsake snovi v ravnovesju.
Na ta način se vsaka koncentracija poveča na eksponent, ki ustreza koeficientu posamezne snovi v reakciji, in Kç nima enote *.
Poleg tega je v tem izrazu zelo pomemben vidik
ne smejo biti zastopane niti trdne komponente niti čiste tekočine., saj v tem izrazu sodelujejo samo zadeve, ki lahko trpijo zaradi sprememb. Koncentracija snovi v trdnem stanju v snovi je konstantna in je tako že vključena v vrednost samega K.ç. Enako velja za čiste tekočine, kot je voda. V kratkem, pri izražanju sodelujejo samo snovi v plinastem stanju in v vodni raztopini.Ne ustavi se zdaj... Po oglaševanju je še več;)
Upoštevajte spodnje primere:
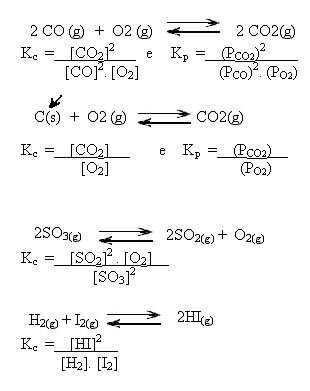
K vrednostiç nam lahko pokaže, ali so koncentracije reaktantov in produktov enake ali je eden večji od drugega:
- če Kç ali KP je enako ena (Kç = 1), to pomeni, da je koncentracija reaktantov in produktov enaka;
- če je vrednost Kç ali KP biti visok, to pomeni, da so izdelki v večji koncentraciji, ker v izražanju Kç izdelki so v števcu;
- če je vrednost Kç ali KP je nizka, to pomeni, da so reagenti v višji koncentraciji, ker v izražanju Kç reagenti so v imenovalcu.
* Kç in KP so brezdimenzijska števila, to so čista števila, brez enote, povezane z velikostjo ali razmerjem med velikostmi.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
FOGAÇA, Jennifer Rocha Vargas. "Konstanti ravnotežja Kc in Kp"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/constantes-equilibrio-kc-kp.htm. Dostopno 28. junija 2021.