Americký chemik Gilbert N. Lewis (1875-1946) navrhol pravidlo oktetu, ktoré hovorí:
„Atómy rôznych prvkov vytvárajú chemické väzby darovaním, prijímaním alebo zdieľaním elektrónov s cieľom získať elektronickú konfiguráciu ušľachtilý plyn, to znamená s 8 elektrónmi v poslednom obale (alebo s 2 elektrónmi v prípade atómov, ktoré majú iba jeden elektrónový obal, ako sa to vyskytuje u vodík). ““
V roku 1916 Lewis navrhol, že zostať stabilný a dosiahnuť oktet alebo duet, prvky, ktoré tvoria molekulárne látky vykonať zdieľanie párov elektrónov. Tieto látky sú tvorené iba atómami vodík, nekovy a polokovy, všetko s tendencia prijímať elektróny. Preto pre nikoho z nich neexistuje spôsob, ako darovať akýkoľvek elektrón (ako je to u kovov v iónových väzbách), ale každý potrebuje prijať, takže sa delí o svoje elektróny prostredníctvom kovalentnej väzby alebo molekulárne.
Gilbert Lewis teda navrhol spôsob, ako reprezentovať kovalentnú alebo molekulárnu väzbu, ktorá sa stala známa ako Lewisov vzorec. Tiež sa volá
elektronický vzorec alebo ešte Lewisova elektronická formula, pretože jeho hlavnou charakteristikou je, že je ukazuje elektróny vo valenčnom plášti každého atómu a tvorbu elektronických párov.Každý elektrón je reprezentovaný bodkou., ktorý obklopuje symbol zodpovedajúceho chemického prvku. Okolo prvku sú iba elektróny valenčnej škrupiny.
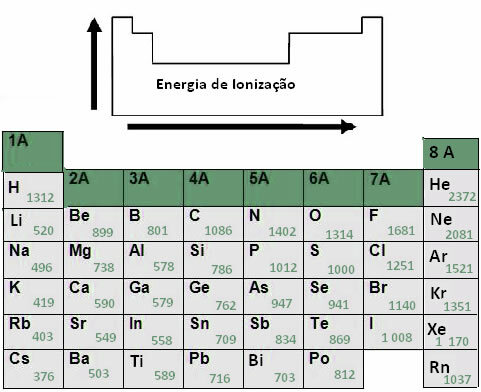
Ako ukazuje nasledujúca tabuľka, aby ste poznali množstvo elektrónov vo valenčnom škrupine, stačí poznať rodinu periodických tabuliek:
Teraz neprestávajte... Po reklame je toho viac;)

V Lewisovom vzorci každý zdieľaný elektrónový pár predstavuje chemickú (kovalentnú) väzbu, kde sa elektróny stretávajú v oblasti elektrosféry, ktorá je spoločná pre každý pár atómov, ktoré sú spojené. Preto sú v znázornení umiestnené vedľa seba.
Napríklad poďme zistiť, čo je Lewisov vzorec pre plynný vodík, ktorého molekulárny vzorec je: H2.
Každý atóm vodíka má vo valenčnom plášti iba jeden elektrón, pretože tento prvok patrí do rodiny 1 periodickej tabuľky. Každý musí prijať ďalší elektrón, aby bol stabilný, pričom v elektrónovom obale K sú dva elektróny. Zdieľajú teda svoje elektróny a obaja dostanú dva. Pozri:
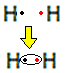
Toto je Lewisov vzorec pre molekulu plynného vodíka.
Kyslík má vo svojom elektrónovom obale šesť elektrónov, takže každý musí prijať dva ďalšie elektróny, aby bol stabilný, a to s ôsmimi elektrónmi. Preto Lewisov vzorec pre molekulu kyslíka je:

Uvidíte, že existujú dva odkazy, pretože existujú dva zdieľané páry.
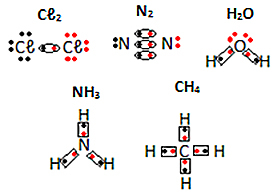
Ďalšie príklady elektronických vzorcov molekulárnych látok nájdete nižšie:
Autor: Jennifer Fogaça
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. „Lewis Electronic Formula“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/formula-eletronica-lewis.htm. Prístup k 28. júnu 2021.
Uhlíkový priestorový vzorec, Lewisov elektronový vzorec, rovinná štruktúra, elektronické páry, väzba kovalentná, valenčná vrstva, vývoj atómového modelu, molekulárny vzorec, štruktúrny vzorec, vzorce trojrozmerný.
Chemické vzorce, plochý štruktúrny vzorec, Couperov štruktúrny vzorec, trojitá väzba, plyn dusík, elektronický vzorec, Lewisov vzorec, molekulárny vzorec, jednoduchá väzba, dvojitá väzba, plyn uhličitý.
Chémia
Molekulárne látky, teplota varu, kontaktná plocha, teplota varu, medzimolekulové príťažlivé sily, chemická väzba, molekulárne zlúčeniny, kovalentné chemické väzby, iónové väzby, kovové väzby, fyzikálne stavy zlé