THE konštanta hydrolýzy (Kh) označuje a chemická rovnováha založený na hydrolýze soli (chemická reakcia zahŕňajúca rozpustnú soľ a vodu).
Ako konštanta akejkoľvek inej rovnováhy vyjadrenie konštanta hydrolýzy je zostrojený z produktu koncentrácií produktu vydeleného produktom koncentrácií činidla nasledovne:
Kh = [Produkty]
[činidlá]
Práca s hydrolýznou konštantou zahŕňa poznanie troch dôležitých javov:
- Disociácia solí;
- Ionizácia vody;
- Hydrolýza solí.
Disociácia solí
Keď sa rozpustná soľ pridá do vody, disociuje a uvoľňuje katión iný ako hydronium (H +) a anión iný ako hydroxyl (OH-).

Aby sme vám pripomenuli, kedy je alebo nie je soľ rozpustná vo vode, Kliknite tu a študujte tabuľku rozpustnosti solí.
ionizácia vody
Voda je látka, ktorá prirodzene prechádza javom ionizácie, to znamená, že produkuje hydróniový katión a hydroxylový anión.
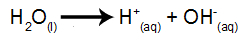
vodná ionizačná rovnica
hydrolýza soli
Ako rozpustná soľ uvoľňuje ióny do vody a voda prechádza ionizáciou a produkuje sa ióny v strede môže prebiehať reakcia (hydrolýza) medzi iónmi soli a vodnými iónmi. Keď dôjde k tejto reakcii, možné interakcie sú:
- Katión soli s aniónom vody (tvorba bázy);
- Anión soli s katiónom vody (tvorba soli);
Vyššie uvedené interakcie nastanú, iba ak je vytvorená báza alebo kyselina slabá.
Teraz neprestávajte... Po reklame je toho viac;)
Pozri príklad hydrolýzy soli:
→ Hydrolýza chlórnanu amónneho (NH4ClO)
Po pridaní chlórnanu amónneho do vody sa rozpúšťa a disociuje za uvoľňovania iónov amónneho katiónu (NH4 +) a chlórnanového aniónu (ClO-):

Rovnica ukazujúca ióny uvoľnené pri disociácii chlórnanu amónneho
Pretože voda, keď podstupuje ionizáciu, produkuje H + a OH-, máme v roztoku dva katióny a dva anióny, ktoré môžu reagovať. Katión NH4 + reaguje iba s OH- aniónom, pretože vytvára slabú bázu (NH4OH). Anión ClO- reaguje iba s katiónom H +, pretože vytvára slabú kyselinu (HClO).

Rovnováha hydrolýzy chlórnanu amónneho
Konštrukcia expresie hydrolýznej konštanty
Konštrukcia hydrolýznej konštanty soli závisí výlučne od rovnice hydrolýzy pre túto soľ. Napríklad hydrolýza chlórnanu amónneho, na ktorej sa pracovalo v predchádzajúcej položke, vygenerovala nasledujúcu rovnicu:

Rovnováha hydrolýzy chlórnanu amónneho
Ako vytvoriť výraz konštanta hydrolýzy zohľadňuje výrobky a činidlá, vyjadrenie konštanty by bolo:
Kh = [HClO]. [NH4OH]
[ClO -]. [NH4 +]
POZNÁMKA: Voda sa na rovnici nezúčastňuje, pretože je to kvapalné činidlo a tiež preto, že je základným prostriedkom na vznik hydrolýzy, to znamená, že je konštantná.
Podľa mňa. Diogo Lopes Dias
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
DNI, Diogo Lopes. „Čo je to konštanta hydrolýzy?“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-constante-hidrolise.htm. Prístup k 28. júnu 2021.
Čo je to chémia?

Pochopte, čo je Kp, rovnovážna konštanta z hľadiska tlaku, a vedieť, ako ju získať pomocou tlakov častice všetkých plynov prítomných v chemickej rovnováhe, ktoré môžu byť v atmosférach (atm) alebo milimetroch ortuti (mmHg). Kliknite sem a dozviete sa viac o tejto téme!
Chémia

Otestujte si svoje vedomosti a dozviete sa viac s týmto zoznamom vyriešených cvičení o chemických bilanciách. Prostredníctvom tohto materiálu budete schopní lepšie pochopiť, ako pracovať s rovnovážnymi konštantami (Kp, Kc a Ki), rovnovážnym posunom, pH a pOH, ako aj s rovnovážnymi stavmi v takzvaných tlmivých roztokoch.

