Batéria je zariadenie, v ktorom sa vyrába elektrický prúd z chemickej energie pochádzajúcej z a oxidoredukčná reakcia, to znamená, že jeden druh reaktantu stráca elektróny (oxidácia), zatiaľ čo iný druh získava elektróny (redukcia).
Pozrite si predstavy o oxidačných a redukčných reakciách, ktoré sa vyskytujú v ktoromkoľvek zásobníku:
Oxidácia: X → a + X+
Druh X stratí elektrón a zmení sa na katión.
Zníženie: Y.- + a → Y
anión Y.- získa elektrón a transformuje sa na neutrálny druh Y.
Základné komponenty stohu
Základné komponenty stohu sú:
Anóda: záporná elektróda, v ktorej prebieha oxidačná reakcia, to znamená strata elektrónov;
Katóda: kladná elektróda, v ktorej prebieha redukčná reakcia, to znamená zisk elektrónov;
Elektrolytický roztok (soľný mostík) alebo vodivý materiál (napríklad grafitová tyč): je prostriedok, ktorým sa elektróny vzdané anódou dostanú ku katóde.
Základy fungovania batérie
Fungovanie zásobníka nastáva z nasledujúcich udalostí:
1. zásada: Oxidácia anódy
Kov v anóde, pretože má väčšiu tendenciu strácať elektróny, sa stáva katiónom, ako vidíme v nižšie uvedenej rovnici:
Zn → Zn2+ + 2 a
2. princíp: redukcia katódy
Katióny, ktoré sú súčasťou materiálu prítomného v katóde (ako príklad použijeme meď), keď sú prijímané elektróny z anódy sa transformujú na kovovú meď, ako vidíme na rovnici nižšie:
Ass2+ + 2e → Cu
prvé hromady
a) Batéria Alessandra Voltu
Alessandrova hromada späť (prvá hromada v histórii), zhromaždená v roku 1800, bola tvorená interkalovanými kovovými diskami, ako na obrázku nižšie:

Zostavenie podobné Alessandrovmu Späť na vašu hromadu
Disky boli prekladané, pretože mali odlišné zloženie. Jeden bol vyrobený z kovového zinku a druhý z medi. Vždy boli oddelené bavlnou namočenou v slanom náleve (roztok tvorený vodou a soľou).
Teraz neprestávajte... Po reklame je toho viac;)
B) Daniellina hromada
Daniellina hromada, zhromaždená v roku 1836, pozostávala z dvoch polčlánkov spojených vodivým drôtom a soľným mostom.
Polčlánok 1: bola to anóda, to znamená záporný pól batérie.
Skladal sa z pozinkovanej platne a časť tejto platne bola ponorená do roztoku tvoreného vodou a síranom zinočnatým (ZnSO4).
Polčlánok 2: bola to katóda, teda kladný pól batérie.
Skladal sa z medenej platne a časť tejto platne bola ponorená do roztoku tvoreného vodou a síranom meďnatým (CuSO4).
soľný most
Trubica v tvare U, ktorá obsahovala roztok tvorený vodou a chloridom draselným (KCl), ktorý spájal dva polčlánky (zinok a meď) a na oboch koncoch mal sklenenú vatu.
batérie v súčasnosti
V súčasnosti existuje niekoľko modelov komínov, ale vo všeobecnosti vyzerajú takto:
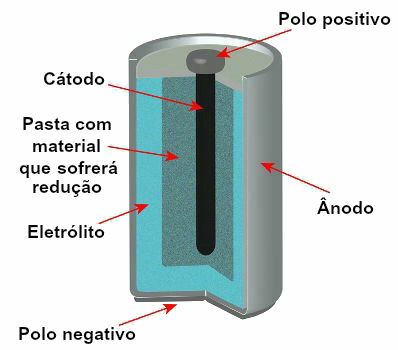
Schematické znázornenie modelu aktuálneho zásobníka
Najpoužívanejšími modelmi sú takzvaná batéria Leclanché a alkalická batéria, ktoré sa vyznačujú nasledujúcimi rozdielmi:
) Hromada Leclanche
Má anódu tvorenú kovovým zinkom;
Má katódu tvorenú pastou s chloridom amónnym, vodou, škrobom a oxidom manganičitým;
Má grafitovú tyč, ktorá slúži ako vodič pre elektróny, ktoré odchádzajú z katódy smerom k anóde.
B) Alkalická batéria
Má anódu tvorenú kovovým zinkom alebo kadmiom;
Má katódu tvorenú oxidom ortuti, oxidom niklu a jódom;
Musí mať zmiešanú základňu v materiáli, z ktorého sa skladá katóda.
Podľa mňa. Diogo Lopes Dias
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
DNI, Diogo Lopes. „Čo je to batéria?“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-pilha.htm. Sprístupnené 27. júna 2021.