Jeden energetická oxidačná reakcia v alkénoch nastáva, keď dôjde k prasknutiu molekuly, to znamená k súčasnému porušeniu dvoch dvojitých väzieb a prívod kyslíka v organickej molekule.
Tento typ reakcie je možné uskutočniť s alkénmi pri použití manganistanu draselného (KMnO4) alebo dvojchrómanu draselného (K.2Cr2O7) zahustené za horúca v kyslom prostredí.
V kyslom prostredí sú H ióny3O+ čo spôsobuje rozklad KMnO4 a uvoľnenie 5 atómov vznikajúceho kyslíka [O] na každé 2 KMnO4. Všimnite si tento rozklad nižšie:

Táto reakcia sa nazýva „energetická“, pretože porušuje dve väzby dvojnej (pri miernej oxidácii sa iba väzba preruší) pi), ďalším faktorom je, že táto redukcia mangánu v kyslom prostredí je oveľa intenzívnejšia ako v základnom prostredí, ako sa to deje v mierna oxidácia.
Uvoľňovaný rodiaci sa kyslík potom reaguje s alkénom, ale konečný produkt závisí od toho, čo typy uhlíka, ktoré vytvárajú dvojitú väzbu, tj ak sú primárne, sekundárne alebo terciárny. Zistite, čo sa stane v obidvoch prípadoch:
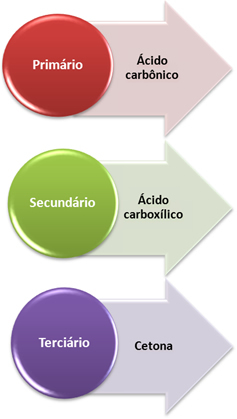
- Primárny uhlík: Ak je nenasýtenie medzi dvoma primárnymi uhlíkmi, vzniknutými produktmi budú dva kyseliny uhličité (H2CO3). Ak je primárny iba jeden z uhlíkov v dvojitej väzbe, bude iba jednou z vytvorených molekúl kyselina uhličitá. Táto zlúčenina je však nestabilná a nikdy nebola izolovaná, rozkladá sa na voda a oxid uhličitý.
- Sekundárny uhlík: Ak je nenasýtenie medzi dvoma sekundárnymi uhlíkmi, budú sa tvoriť dva produkty karboxylové kyseliny. Ak je iba jeden z uhlíkov sekundárny, vznikne z neho molekula karboxylovej kyseliny, zatiaľ čo druhý bude závisieť od druhého uhlíka.
- Terciárny uhlík: Dáva stúpať k ketón.
Pozrite si príklady nižšie:
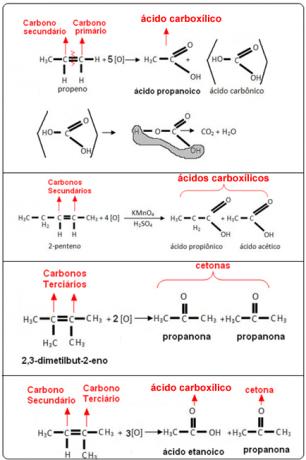
Autor: Jennifer Fogaça
Vyštudoval chémiu
Zdroj: Brazílska škola - https://brasilescola.uol.com.br/quimica/oxidacao-energetica-alcenos.htm
