Pre uskutočnenie chemickej reakcie je potrebné splniť štyri základné podmienky, ktorými sú:
1. Je potrebné kontaktovať činidlá;
2. Medzi činidlami musí byť chemická afinita;
3. Kolízie medzi časticami činidla musia byť účinné;
4. Musí sa dosiahnuť aktivačná energia.
Stručne pozri jednotlivé prípady:
1.Kontakt medzi reagentmi:
Táto podmienka je zrejmá, pretože aj keď majú reaktanty k sebe veľkú afinitu, ako v prípade kyselín a zásad, ak sú oddelené, k reakcii nedôjde. Musia prísť do kontaktu, aby sa ich častice mohli zraziť, prerušiť väzby reaktantov a vytvoriť väzby produktov.

2.Chemická afinita:
Ako sme videli, uvedenie činidiel do kontaktu je nevyhnutné, ale nie dostatočné. Napríklad ak dáme sodík do styku s vodou, dôjde k mimoriadne prudkej reakcii, ale ak dáme zlato, nebudeme vidieť žiadny rozdiel. Je to tak preto, lebo rôzne látky majú navzájom rôznu chemickú afinitu alebo nemusia mať vôbec žiadnu afinitu. Čím vyššia je chemická afinita, tým rýchlejšia je reakcia.
V uvedených príkladoch má sodík veľkú afinitu k vode, a to tak, že sa kovový sodík uchováva v petroleji, aby neprišiel do styku s vlhkosťou vo vzduchu. Zlato je inertné, a preto zlaté pamätníky trvajú tak dlho, ako napríklad egyptské sarkofágy.

3.Kolízna teória:
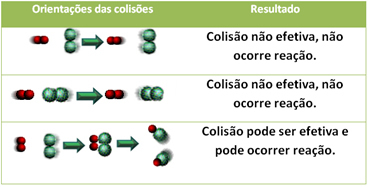
Aj pri zlúčeninách, ktoré majú chemickú afinitu, je pre uskutočnenie reakcie potrebné, aby sa ich častice, atómy alebo molekuly účinne zrazili. Nie všetky častice, ktoré sa zrazia, to urobia efektívne, ale nárazy, ktoré vedú k rozbitiu reagenčné väzby a tvorba nových väzieb sú tie, ktoré sa vyskytujú v správnej orientácii a s energiou dosť.
Teraz neprestávajte... Po reklame je toho viac;)
Ďalej je uvedený prípad dvoch neúčinných kolízií a jednej efektívnej kolízie, ktorá má za následok vznik reakcie.
4.Aktivačná energia a aktivovaný komplex:
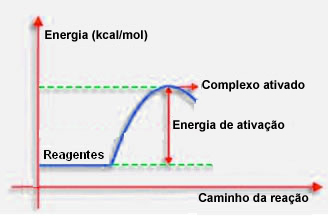
Ako je uvedené v predchádzajúcej položke, efektívna zrážka vyžaduje okrem priaznivého vedenia aj dostatok energie. Minimálne množstvo energie potrebné na uskutočnenie každej reakcie sa nazýva aktivačná energia.
Ak majú reaktanty energiu rovnakú alebo väčšiu ako aktivačná energia, počas dobre zameraného šoku vytvorí sa pôvodne aktivovaný komplex, ktorý je medziproduktom medzi reaktantmi a Produkty. V aktivovanom komplexe sa vytvárajú oslabené väzby reagencií a nové väzby produktu.
Aktivačná energia teda funguje ako druh bariéry pre uskutočnenie reakcie, pretože čím je väčšia, tým ťažšie bude pre ňu dôjsť. V niektorých prípadoch je potrebné dodať reagentom energiu. Napríklad plyn na varenie má afinitu k interakcii s kyslíkom vo vzduchu, ale potrebujeme dodať energiu, keď spojíme zápalku, inak reakcia neprebehne. Ale akonáhle začne, samotná reakcia uvoľní dostatok energie na aktiváciu ďalších molekúl a udržanie reakcie v chode.
Autor: Jennifer Fogaça
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. „Podmienky pre výskyt chemických reakcií“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/condicoes-para-ocorrencia-reacoes-quimicas.htm. Prístup k 27. júnu 2021.


