Vy kovy sú to chemické prvky, ktoré ako svoju hlavnú fyzikálnu charakteristiku predstavujú schopnosť stratiť elektróny a následne vytvárať kovové katióny. Z tohto dôvodu môžu vytvárať dva typy chemických väzieb: iónovú väzbu a kovová väzba.
THE iónová väzba nastáva, keď kov interaguje s prvkom kovovej povahy, ktorým môže byť a ametal alebo vodík. Pri tomto type väzby máme stratu elektrónov kovmi a zisk elektrónov nekovmi alebo vodíkom.
už je kovová väzba vzniká medzi atómami jedného kovového prvku. Tento typ väzby sa vyskytuje iba medzi atómami jedného kovu a výlučne preto, že kov nemôže vytvoriť chemickú väzbu s iným odlišným kovovým prvkom.
Všeobecné charakteristiky kovov
Pevné látky pri izbovej teplote, s výnimkou ortuti;
Sú brilantné;
Majú vysoké teploty topenia a varu;
Spravidla majú striebornú farbu, s výnimkou zlata, ktoré je zlaté, a medi, ktorá je červenkastá;
Čisté kovy sú tvorené zhlukmi atómov (jedného chemického prvku), ktoré sa nazývajú kryštalické mriežky.
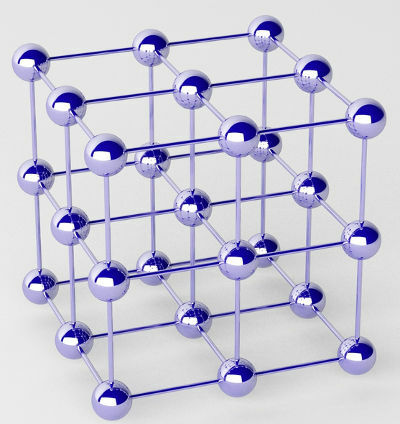
Reprezentácia kryštalickej mriežky kovu
Princípy kovového spojenia
O kovová väzba, kryštalické mriežky, ktoré tvoria kovy, sú vlastne iónový klaster (zložený iba z katióny a elektróny). Elektróny prítomné vo valenčnej vrstve atómov kovu sú delokalizované, to znamená, že opúšťajú valenčnú vrstvu a spôsobujú, že sa atóm stáva katiónom (v elektrónoch je nedostatok).
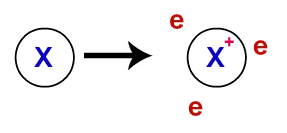
Reprezentácia delokalizovaných elektrónov z valenčného plášťa
Po delokalizácii začnú elektróny z atómov kovov obklopovať katióny a vytvárať skutočné „elektrónové more“. Každý z elektrónov prítomných v tomto mori má schopnosť voľne sa pohybovať cez kryštalickú mriežku kovu.
Teraz neprestávajte... Po reklame je toho viac;)

Reprezentácia modelu elektrónového mora
POZNÁMKA: Elektróny „z mora“ nie sú schopné opustiť krištáľovú mriežku a pohybovať sa cez ňu.
Vlastnosti kovov odôvodnené kovovým spojením
a) obchodovateľnosť
Prostredníctvom kovu je možné vyrábať plechy rôznych hrúbok a plechov. Vďaka tejto vlastnosti kovov môžeme stavať rôzne predmety, ako sú nože, meče atď.

Čepeľ meča je vyrobená z kovu
b) Vodivosť
Kovy sú všeobecne dobrými vodičmi elektrického prúdu a tepla. Keď je akýkoľvek kov v kontakte so zdrojom tepla alebo zdrojom elektrického prúdu, je schopný ich viesť.

Hliníková panvica v plameni kachlí sa vďaka vodivosti úplne zahreje.
c) ťažnosť
Cez kov môžeme vyrábať drôty. Použitie kovu vo forme drôtov uľahčuje jeho použitie, najmä v súvislosti s elektrickou vodivosťou.

Na výrobu drôtov sa môže použiť kov, napríklad meď.
Podľa mňa. Diogo Lopes Dias
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
DNI, Diogo Lopes. „Čo je to kovové spojenie?“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ligacao-metalica.htm. Prístup k 27. júnu 2021.
Chémia
Iónová väzba, usporiadanie medzi iónovými zlúčeninami, iónovými aglomerátmi, chloridom sodným, kuchynskou soľou, iónovými látkami, elektrostatické príťažlivé sily, chloridové anióny, katióny sodíka, polárne rozpúšťadlá, pozitívne ióny, katióny, negatívne ióny, anióny.