Disociácia základne to je a fyzický proces ktorá sa vyskytuje u tejto dôležitej skupiny anorganických látok, keď sú rozpustené vo vode, alebo keď prechádzajú procesom fúzie (prechod z pevného skupenstva do kvapalného stavu cez kúrenie).
Všeobecne platí, že fenomén disociácia bázy je to uvoľňovanie katiónov a aniónov, ktoré tvoria iónová zlúčenina, ktorá je v tomto prípade základňou. Takže počas disociácia bázy, vydanie ióny ktoré už v zlúčenine existujú, to znamená, že nevznikajú žiadne nové ióny.
Bázu tvorí akýkoľvek kov (X), ktorý je katiónom zlúčeniny, alebo amónny katión (skupina NH4+), viazané na hydroxidový anión (predstavovaný skupinou OH), ako je to znázornené nižšie:
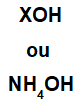
Všeobecné znázornenia základného vzorca
forma predstavujú disociácia bázy deje sa to pomocou rovnice, v ktorej v reaktante máme bázu a vo výrobkoch máme ióny (katióny a anióny). Rozdiel je v tom, ako prebieha disociácia:
Rozpustenie bázy vo vode:
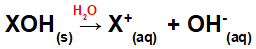
Rovnica predstavujúca disociáciu bázy vo vodnom prostredí
Disociácia podľa základného zlúčenia:
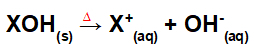
Rovnica predstavujúca disociáciu bázy procesom fúzie
Analýzou vyššie uvedených všeobecných rovníc overíme, že vo všetkých z nich vždy budeme mať bázu, katión (čo je kov alebo skupina NH).4+) a anión (OH.)-). Ale sú všetci takí? Nie je medzi nimi rozdiel? Na prvú otázku je odpoveď záporná a na druhú otázku kladná odpoveď.
Keď vykonávame disociácia od základne, je nevyhnutné najskôr analyzovať základný vzorec, pretože z neho môžeme určiť zaťaženie katión a molárne množstvo hydroxidových aniónov, pretože molárne množstvo katiónu je štandardné (vždy 1 mol).
Je potrebné pripomenúť, že množstvo OH skupín prítomných v základnom vzorci určuje náboj katiónu a množstvo mol hydroxidového aniónu v disociácii bázy.
Pozrime sa na príklady hydroxidu hlinitého [Al (OH)3] a hydroxid zlata (AuOH). Vo vzorci na báze hliníka sú tri skupiny OH a vo vzorci na báze zlata iba jedna skupina OH. Pri disociácii týchto báz teda máme:
Al (OH) disociácia3:
Pretože táto báza má vo vzorci tri skupiny OH, náboj na katióne bude +3 a množstvo v molách aniónov sa rovná 3 mol, ako vidíme v nasledujúcej rovnici:
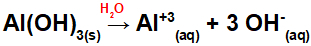
Rovnica disociácie hliníkovej bázy vo vodnom prostredí
Disociácia od AuOH:
Pretože táto báza má vo vzorci skupinu OH, náboj na katióne bude +1 a množstvo v móloch aniónov sa rovná 1 molu, ako vidíme v nasledujúcej rovnici:
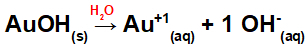
Rovnica disociácie bázy so zlatom vo vodnom prostredí
Podľa mňa. Diogo Lopes Dias
Zdroj: Brazílska škola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-dissociacao-das-bases.htm
