THE autooxi-redukcia alebo neprimeraná reakcia je typ redoxnej reakcie, pri ktorej dochádza k rovnakému chemickému prvku oxidácia a redukcia. Pozrime sa na dva príklady tohto typu reakcií a na to, ako ich vyvážiť pomocou redoxnej metódy:
1. príklad:
NA2- + H+ → NIE3- + NIE + H2O
- Výpočtom oxidačných čísel (NOX) všetkých atómov a iónov zapojených do reakcie je možné overiť, kto oxidoval a kto reagoval:
+3 -2 +1 +5 -2 +2 -2 +1 -2
NA2- + H+ → NIE3- + NIE + H2O
- Všimnite si, že dusík bol druh, ktorý reagoval aj oxidoval:
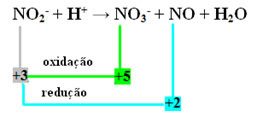
- Aby sme dosiahli redoxné vyváženie tejto reakcie, musíme vzťahovať NOX na produkty, nie na činidlá:
NA3- = ∆Nox = 5 - 3 = 2
NO = ∆Nox = 3 - 2 = 1
- Invertovaním ∆NOX koeficientmi máme:
NA3- = ∆NOX = 2 → 2 bude koeficientom NO
NO = ∆NOX = 1→ 1 bude koeficientom NO3-
NA2- + H+ → 1 NA3- + 2 NIE + H2O
- S týmto už vieme, že vo výrobku sú 3 N, teda koeficient NO2- bude 3:
3 NIE2- + H+ → 1 NO3- + 2 NIE + H2O
- Na stanovenie koeficientov H+ a od H2Ó, pamätaj, že počet prijatých elektrónov sa rovná rovnakému množstvu darovaných elektrónov; náboj činidla sa teda bude rovnať náboju produktu. Týmto spôsobom môžeme vytvoriť nasledujúcu schému:
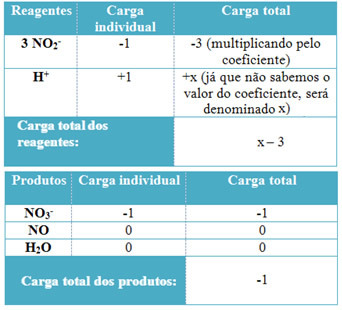
Na základe týchto informácií máme za to, že celkový náboj reagencií sa rovná x - 3 a výrobok sa rovná -1. Ako už bolo uvedené, obvinenia oboch osôb musia byť rovnaké. Pretože už máme celkové množstvo výrobkov, môžeme vykonať jednoduchý výpočet, aby sme vedeli, aká bude hodnota x:
x -3 = -1
x = -1 +3
x = 2
Teda koeficient H+ je 2 a v dôsledku toho je H2Bude 1:
3 NIE2- + 2 H+ → 1 NO3- + 2 NO + 1 H2O
2. príklad:
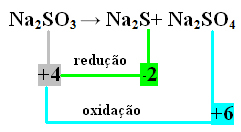
V tomto prípade to bol S, ktorý prešiel redukciou a oxidáciou súčasne. Teda, ako už bolo predtým urobené, môžeme spojiť NOX s výrobkami a prevrátiť ich hodnoty tak, že im priradíme koeficienty:
O2 S = ∆Nox = 4 - (-2) = 6 → 6 bude koeficient Na2 IBA4
O2 IBA4= ∆Nox = 6 - 4 = 2 → 2 bude koeficient Na2 s
O2 IBA3→ 2 O2 Y + 6 O2 IBA4
Pretože v druhej končatine je 8 sírov, koeficient Na2 IBA3 bude 8:
8 palcov2 IBA3→ 2 palce2 Vstup S + 62 IBA4
Autor: Jennifer Fogaça
Vyštudoval chémiu
Zdroj: Brazílska škola - https://brasilescola.uol.com.br/quimica/reacoes-auto-oxirreducao.htm
