Môžeme si to všimnúť kedykoľvek zvýšime koncentráciu jedného alebo všetkých reaktantov zúčastňujúcich sa na chemickej reakcii, dôjde k zvýšeniu jeho rýchlosti vývoja, to znamená rýchlosti reakcie.
Platí to aj naopak. Napríklad sa v súčasnosti odporúča, aby sme namiesto bežného alkoholu používali alkoholový gél, pretože existuje menšie riziko jeho horenia a zabránenia nehodám. Bežný tekutý alkohol je v skutočnosti zmes alkoholu a vody, pričom gélový alkohol obsahuje menšie množstvo alkoholu. Preto keď sa zníži koncentrácia jedného zo spaľovacích reaktantov, v prípade alkoholu prebieha reakcia pomalšie. Na druhej strane, čím je alkohol čistejší, tým rýchlejšia je spaľovacia reakcia.

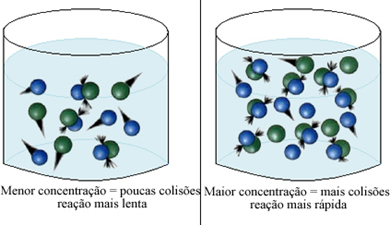
Ako je uvedené v texte Podmienky pre výskyt chemických reakcií, jednou z podmienok uskutočnenia reakcie je účinná kolízia medzi časticami. Teda zvýšenie koncentrácie činidiel umožňuje, aby bolo v rovnakom priestore obmedzené väčšie množstvo častíc alebo molekúl. Zvyšuje sa tým počet kolízií medzi nimi a tiež sa zvyšuje pravdepodobnosť, že dôjde k účinným kolíziám, ktoré budú mať za následok vznik reakcie. Výsledkom je, že reakcia prebehne rýchlejšie.
Ak to chcete vidieť, zamyslite sa nad nasledujúcim príkladom: keď máme horiaci uhlík a chceme, aby sa toto spaľovanie spracovalo rýchlejšie, fúkame alebo fúkame uhlík? Prečo to funguje?
Jedným z reaktantov v tejto spaľovacej reakcii je kyslík vo vzduchu. Keď sa zatrasieme, prúd vzduchu odstráni popol, ktorý sa vytvára pri spaľovaní, a to uľahčuje kontakt kyslíka s uhlíkom. Týmto spôsobom zvyšujeme kontakt medzi reaktantmi a urýchľujeme spaľovaciu reakciu.
Stručne povedané, máme:

Pri práci s plynmi existuje jeden spôsob, ako zvýšiť koncentráciu reaktantov znížte tlak. Keď to urobíme, znížime objem a v dôsledku toho dôjde k zvýšeniu koncentrácií činidla.

Autor: Jennifer Fogaça
Vyštudoval chémiu
Zdroj: Brazílska škola - https://brasilescola.uol.com.br/quimica/concentracao-dos-reagentes-velocidade-das-reacoes.htm
