A druhý termodynamický zákon určuje, aké podmienky existujú pre teplo premeniť na prácu v tepelných motoroch a chladničkách. Zaoberá sa aj definíciou entropia ako jav schopný merať dezorganizáciu častíc vo fyzikálnych systémoch.
Prečítajte si tiež: Kalorimetria - oblasť fyziky, ktorá študuje výmenu tepla
Témy tohto článku
- 1 - Zhrnutie druhého zákona termodynamiky
- 2 - Aký je druhý termodynamický zákon?
-
3 - Aplikácia druhého zákona termodynamiky
- Druhý zákon termodynamiky tepelných motorov
- Druhý zákon termodynamiky v chladničkách
- 4 - Entropia a druhý termodynamický zákon
-
5 - Vzorce druhého zákona termodynamiky
- Tepelné stroje a chladničky
- Chladničky
- Príklady použitia vzorcov
- 6 - Carnotov cyklus
- 7 - Zákony termodynamiky
- 8 - Vyriešené úlohy z druhého zákona termodynamiky
Zhrnutie druhého zákona termodynamiky
Druhý termodynamický zákon predstavujú výroky Clausiusa a Kelvina-Plancka.
Clausiusov výrok sa zaoberá tokom tepla z teplejšieho telesa do chladnejšieho telesa.
Vyhlásenie Kelvina-Plancka sa zaoberá neschopnosťou tepelných zariadení premeniť všetko svoje teplo na práca.
Druhý termodynamický zákon sa vzťahuje na tepelné motory a chladničky.
Carnotov cyklus je cyklus maximálnej účinnosti dosiahnutý tepelnými motormi.
Carnotov cyklus má štyri stupne, reverzibilnú izotermickú expanziu, vratnú adiabatickú expanziu, reverzibilnú izotermickú kompresiu a reverzibilnú adiabatickú kompresiu.
Carnotova veta sa vzťahuje na výnos z Carnotove stroje.
Aký je druhý zákon termodynamiky?
Druhým termodynamickým zákonom je a zákon, ktorý rieši obmedzenia vyskytujúce sa v termodynamických procesoch. Vyhlásili to fyzici Rudolf Clausius (1822-1888), Lord Kelvin (1824-1907) a Max Planck (1858-1947), ako uvidíme nižšie:
Fyzik a matematik Rudolf Clausius uviedol, že tok vedenia tepla prebieha z telesa s vyššou teplotou do telesa s nižšou teplotou. nižšia teplota, preto nie je prirodzené, aby došlo k inverznému procesu, preto je potrebné na tom pracovať systém. S tým uviedol:
Nie je možné uskutočniť proces, ktorého jediným účinkom je prenos tepla z chladnejšieho telesa na teplejšie teleso.|1|
Matematický fyzik William Thomson, známy ako Lord Kelvin, spolu s príspevkami fyzika Maxa Plancka, uviedol nemožnosť tepelných zariadení s účinnosťou 100%, pretože vždy dôjde k tepelným stratám.
Neprestávaj teraz... Po publicite je toho viac ;)
Aplikácie druhého zákona termodynamiky
Druhý termodynamický zákon sa vzťahuje na tepelné motory a chladničky.
Druhý zákon termodynamiky v strojoch tepelný
K Tepelné stroje sú schopné premieňať teplo na prácu. Horúci zdroj dodáva teplo tepelnému stroju, ktorý ho premieňa na prácu. Zvyšok tepla odošle do zdroja chladu, ako je znázornené na obrázku nižšie:
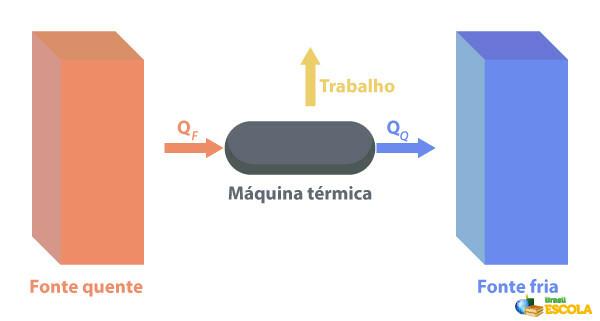
Niektoré príklady tepelných strojov sú: parné a petrolejové turbíny v prúdových lietadlách, spaľovacie motory, termonukleárne reaktory.
Druhý zákon termodynamiky v chladničkách
Chladničky sú stroje, ktoré Pracujú opačne ako tepelné motory., kde odoberajú teplo z regiónu s teplota nižšiu teplotu a dodávať ju do oblasti s vyššou teplotou. Keďže to nie je prirodzené, je potrebné, aby stroj vykonával prácu s využitím elektrickej energie, ako je popísané na obrázku nižšie:
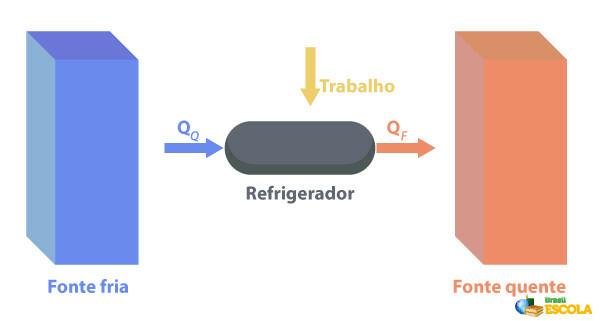
Niektoré príklady chladničiek sú chladničky a klimatizácie.
Entropia a druhý termodynamický zákon
A Druhý termodynamický zákon hovorí o existencii entropie, jeden fyzikálne množstvo zodpovedný za meranie stupňa dezorganizácie častíc vo fyzikálnom systéme alebo stupňa ireverzibilnosti termodynamické procesy zapojené do tepelných motorov, ktoré sú spontánne, nevyhnutné, nezvratné a expanzívna. Pomocou toho je možné iba pozorovať a kontrolovať stupeň volatility procesov. So zvyšujúcou sa entropiou sa zvyšuje aj stupeň neusporiadanosti systému.
A Nomenklatúra entropie je gréckeho pôvodu a znamená „transformácia“., „zmena“, teda sa používa v Fyzické na označenie náhodnosti a neporiadku. Entropiu možno vypočítať pomocou vzorca:
\(∆S=\frac{∆U}T\)
\(∆S\) je zmena entropie, meraná v [J/K].
\(∆U\) je zmena vnútornej energie meraná v jouloch [J].
T je teplota meraná v Kelvinoch [K].
Zo štatistického hľadiska sa entropia vypočíta podľa vzorca:
\(S=k\cdot ln\ Ω\)
S je entropia meraná v [J/K].
k je Boltzmannova konštanta, stojí za to \(1,4\cdot 10^{-23}\ J/K\).
Ω je počet možných mikrostavov pre systém.
Prečítajte si tiež: Procesy šírenia tepla
Vzorce druhého zákona termodynamiky
Tepelné stroje a chladničky
\(Q_Q=W+Q_F\)
\(Q_Q\) je teplo horúceho zdroja, merané v jouloch [J].
W je práca vykonaná tepelným motorom, meraná v jouloch [J].
\(Q_F\) je teplo zo zdroja chladu, merané v jouloch [J].
Môže byť reprezentovaný:
\(W=Q_Q-Q_F\)
W je práca vykonaná tepelným motorom, meraná v jouloch [J].
\(Q_Q\) je teplo horúceho zdroja, merané v jouloch [J].
\(Q_F\) je teplo zo zdroja chladu, merané v jouloch [J].
Chladničky
\(η=\frac{Q_F}{Q_Q-Q_F}\)
\(η\) je účinnosť chladničky.
\(Q_F\) je teplo zo zdroja chladu, merané v jouloch [J].
\(Q_Q\) je teplo horúceho zdroja, merané v jouloch [J].
Môže byť reprezentovaný ako:
\(η=\frac{Q_F}W\)
\(η\) je účinnosť chladničky.
\(Q_F\) je teplo zo zdroja chladu, merané v jouloch [J].
W je práca vykonaná tepelným motorom, meraná v jouloch [J].
Príklady aplikácie vzorcov
Príklad 1: Vypočítajte prácu, ktorú vykoná tepelný motor počas cyklu, ktorý prijme 500 J tepla z horúceho zdroja a odovzdá len 400 J tepla studenému zdroju.
Na výpočet práce tepelného motora použijeme vzorec:
\(W=Q_Q-Q_F\)
Nahradením hodnôt uvedených vo vyhlásení:
\(W=500-400\)
\(W=100\ J\)
Práca tepelného motora bola 100 joulov.
Príklad 2: Aká je účinnosť chladničky, ktorá prijme 150 J tepla z horúceho zdroja a odovzdá 50 J tepla studenému zdroju?
Na výpočet účinnosti chladničky použijeme vzorec:
\(η=\frac{Q_F}{Q_Q-Q_F}\)
Nahradením hodnôt uvedených vo vyhlásení dostaneme:
\(η=\frac{50}{150-50}\)
\(η=\frac{50}{100}\)
\(η=0,5\)
Vynásobenie výnosu 100%:
\(η=0,5\cdot100%\)
\(η=50\%\)
Chladnička má 50% účinnosť.
Carnotov cyklus
Carnotov cyklus bol vyvinutý vedcom Sadi Carnotom (1796-1832), s cieľom identifikovať maximálnu účinnosť, ktorú môže dosiahnuť tepelný motor, ktorý pracuje medzi horúcim zdrojom a studeným zdrojom.
Na základe svojich štúdií Carnot zistil, že v záujme dosiahnutia maximálnej účinnosti tepelného motora je to tak nevyhnutné na to, aby bol jeho proces reverzibilný, preto vyvinul cyklus maximálneho výnosu nazývaný cyklus Carnot a Tepelný stroj, ktorý ním pracuje, sa nazýva Carnotov tepelný motor.. Keďže Carnotov cyklus je reverzibilný, možno ho obrátiť, a tak boli vyvinuté chladničky.
Carnotov cyklus, bez ohľadu na použitú látku, sa skladá zo štyroch procesov opísaných v grafe tlaku podľa objemu (p×V), ako môžeme vidieť na obrázku nižšie:
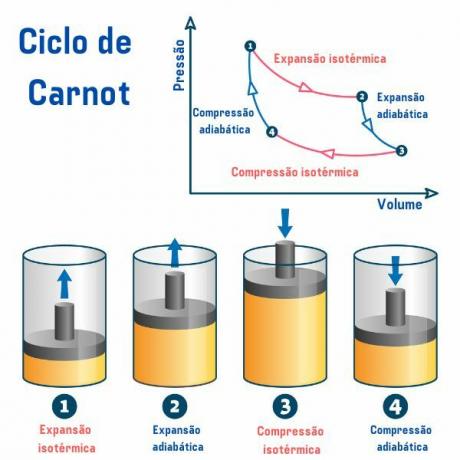
1. postup, z bodu 1 → 2: dochádza k reverzibilnej izotermickej expanzii (proces, pri ktorom teplota zostáva konštantná), pri ktorej plyn (alebo systém) pracuje a získava určité množstvo tepla z horúceho zdroja.
2. postup, z bodu 2 → 3: existuje adiabatická expanzia (proces, pri ktorom dochádza k výmene tepla s vonkajším prostredím) vratná, pri ktorej nedochádza k výmene tepla teplo s tepelnými zdrojmi, ale plyn funguje a dochádza k poklesu jeho vnútornej energie, čo spôsobuje pokles v teplota.
3. postup, od bodu 3 → 4: dochádza k reverzibilnej izotermickej kompresii, pri ktorej plyn prijíma prácu a odovzdáva množstvo tepla zdroju chladu.
4. postup, od bodu 4 → 1: nastáva reverzibilná adibatická kompresia, pri ktorej neprebieha žiadna výmena tepla s tepelnými zdrojmi a plyn áno zahrieva, kým nedosiahne teplotu horúceho zdroja, a teda sa s ním dostane do kontaktu, čím sa skončí cyklu.
zákony termodynamiky
Zákony termodynamiky sú štyri zákony, ktoré riadia celé štúdium termodynamikaštudovať vzťahy medzi objemom, teplotou a tlakom a inými fyzikálnymi veličinami, ako je teplo a energia.
Nultý zákon termodynamiky: je zákon o tepelná bilancia, skúma výmenu tepla medzi telesami, ktoré majú rôzne teploty.
prvý zákon termodynamiky: je zákon zachovania energie v termodynamických systémoch, študuje premenu tepla na prácu a/alebo vnútornú energiu.
Druhý zákon termodynamiky: je to zákon, ktorý sa zaoberá tepelnými strojmi, chladničkami a entropiou.
Tretí zákon termodynamiky: je zákon o absolútna nulaštuduje účinky tejto teploty.
Prečítajte si tiež: Výkon tepelných motorov
Vyriešené úlohy z druhého zákona termodynamiky
Otázka 1 Určte teplotu horúceho zdroja Carnotovho motora s vedomím, že teplota studeného zdroja je 450 K a jeho účinnosť je 80 %.
a) 2250 K
b) 450 tis
c) 1500 tis
d) 900 tis
e) 3640 K
Rozhodnutie:
Alternatíva A. Teplotu horúceho zdroja vypočítame na základe vzorca účinnosti Carnotovho motora:
\(η=1-\frac{T_F}{T_Q} \)
\(80 \%=1-\frac{450}{T_Q} \)
\(\frac{80}{100}=1-\frac{450}{T_Q} \)
\(0,8=1-\frac{450}{T_Q} \)
\(0,8-1=-\frac{450}{T_Q} \)
\(-0,2=-\frac{450}{T_Q} \)
\(0,2=\frac{450}{T_Q} \)
\(T_Q=\frac{450}{0,2}\)
\(T_Q=2250\ K\)
otázka 2 (Cefet-PR) 2. princíp termodynamiky možno konštatovať takto: „Nie je možné postaviť stroj tepelná energia pracujúca v cykloch, ktorej jediným účinkom je odoberať teplo zo zdroja a integrálne ho premieňať na práca". V rozšírení nás tento princíp vedie k záveru, že:
a) Vždy je možné postaviť tepelné stroje, ktorých účinnosť je 100%.
b) každý tepelný stroj potrebuje len jeden zdroj tepla.
c) teplo a práca nie sú homogénne veličiny.
d) každý tepelný motor odoberá teplo z horúceho zdroja a časť tohto tepla odvádza do studeného zdroja.
e) len pri studenom zdroji, vždy udržiavanom na 0 °C, by bolo možné pre určitý tepelný stroj úplne premeniť teplo na prácu.
Rozhodnutie:
Alternatíva D. Tento princíp nás informuje, že nie je možné odobrať všetko teplo z horúceho zdroja a odovzdať ho studenému zdroju.
Poznámka
|1| Základný kurz fyziky: Tekutiny, Kmity a vlny, Teplo (zv. 2).
Autor: Pamella Raphaella Melo
Učiteľ fyziky
Entropia systému nie je nič iné ako miera jeho dezorganizácie. Druhý zákon je možné formulovať z pojmu entropia.
Objavte fascinujúcu históriu tepelných motorov a ich hlavné využitie.
Viete, čo sú tepelné stroje, termodynamické cykly a účinnosť? Získajte viac informácií o týchto dôležitých termodynamických konceptoch.
Prejdite do textu a naučte sa definíciu prvého zákona termodynamiky, pozrite sa, aké vzorce používa tento zákon, a pozrite si vyriešené úlohy na túto tému.
Izotermická, izovolumetrická a adiabatická transformácia. Zoznámte sa s nimi!
Viete, čo je termodynamika? Prejdite do textu a zistite, ktoré sú najdôležitejšie pojmy na túto tému, dozviete sa o zákonoch termodynamiky.


