THE spoločná koncentrácia, tiež nazývaná koncentrácia v g/l, je pomer medzi hmotnosťou rozpustenej látky v objeme roztoku.
Matematicky je spoločná koncentrácia vyjadrená vzorcom:
C = m/v
Kde,
C: bežná koncentrácia;
m: hmotnosť rozpustenej látky;
V: objem roztoku.
Najbežnejšie používanou jednotkou bežnej koncentrácie je g/l, keďže hmotnosť rozpustenej látky sa počíta v gramoch (g) a objem roztoku v litroch (L).
Morská voda má napríklad veľké množstvo rozpustených solí a jednou z nich je chlorid sodný (NaCl), ľudovo nazývaný kuchynská soľ.
Koncentrácia chloridu sodného v morskej vode je v priemere 2,5 g/l. Takže v každom 1 litri morskej vody, ktorá je roztokom, je 2,5 gramu soli, čo je rozpustená látka.
Ako vypočítať bežnú koncentráciu?
Roztok je homogénna zmes tvorená látkou v menšom množstve, nazývanou rozpustená látka, rozpustenou v rozpúšťadle, ktoré je vo väčšom množstve.
Bežná koncentrácia sa teda vzťahuje na množstvo rozpustenej látky v danom objeme roztoku. Čím viac rozpustenej látky sa v roztoku rozpustí, tým je koncentrovanejší. V opačnom prípade, to znamená, že nízky obsah rozpustenej látky znamená, že roztok je zriedený.
Príklad 1: Aká je koncentrácia vg/l roztoku jodidu strieborného (AgI) s obsahom 2,6 g v 1l roztoku?
Keď dostaneme množstvo rozpustenej látky a objem roztoku, jednoducho zapojíme hodnoty do všeobecného vzorca koncentrácie, aby sme našli jej hodnotu.
Preto v 2,6 g/l roztoku jodidu strieborného je 2,6 g rozpustenej látky v každom 1 litri roztoku.
Príklad 2: Aká je hmotnosť získanej rozpustenej látky pri odparení rozpúšťadla z 500 ml fyziologického roztoku s koncentráciou 6 g/l?
Všimnite si, že v niektorých výpočtoch môžeme nájsť opísanú bežnú koncentráciu, aby sme mohli vypočítať hmotnosť rozpustenej látky.
Je potrebné venovať pozornosť aj jednotkám. Keďže bežná koncentrácia je uvedená v g/l, v tomto prípade musíme pred použitím vzorca previesť jednotku objemu.
Ako 1 l obsahuje 1000 ml, tak 500 ml zodpovedá 0,5 l.
Pri odparení rozpúšťadla z roztoku s koncentráciou 6 g/l sa tak získalo 12 g rozpustenej látky.
Získajte viac vedomostí s obsahom:
- Koncentrácia roztoku
- molárnej koncentrácie
- Riedenie roztokov
Vyriešené bežné koncentračné cvičenia
Pomocou nasledujúcich otázok si overte znalosti, ktoré ste získali predtým.
Otázka 1
(Unicamp) Rozpúšťadlo sa úplne odparí z 250 ml vodného roztoku MgCl2 koncentrácia 8,0 g/l. Koľko gramov rozpustenej látky sa získa?
a) 8,0
b) 6,0
c) 4,0
d) 2,0
e) 1,0
Správna alternatíva: d) 2.0.
otázka 2
Pozrite si obrázok nižšie.
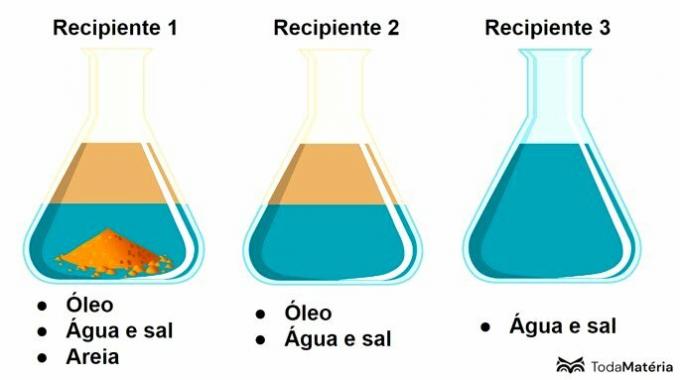
V tejto schéme kontajner 3 obsahuje a
a) heterogénna zmes
b) čistá látka
c) Riešenie
d) koloidná zmes
Správna alternatíva: c) Riešenie.
Nádoba 3 obsahuje roztok, čo je homogénna zmes tvorená rozpustenou látkou a rozpúšťadlom, kde soľ je rozpustená látka a voda je rozpúšťadlo.
Vo všeobecnosti môžeme povedať, že rozpustená látka je zložkou v najmenšom množstve a rozpúšťadlo je prítomné v najväčšom množstve.
Nádoba 1 predstavuje heterogénnu zmes s 3 fázami a nádoba 2 zodpovedá heterogénnej zmesi 2 fáz.
otázka 3
Roztok sa pripravil rozpustením 4,0 g chloridu horečnatého MgCl2 až do dosiahnutia koncentrácie 2,0 g/l. Aký objem roztoku bol pripravený?
a) 1 l
b) 2 l
c) 4 l
d) 6 l
Správna alternatíva: b) 2 l.
Ďalšie problémy s komentovaným riešením nájdete na adrese bežné koncentračné cvičenia.
Bibliografické odkazy
FONSECA, M. R. M. Chémia, 1. 1. vyd. São Paulo: Attika, 2013.
SANTOS, W.L.P; MOL, G.S. Občianska chémia, 1. 2. vyd. São Paulo: Editora AJS, 2013.
USBERCO, J. Pripojte chémiu, 1. 2. vyd. São Paulo: Saraiva, 2014.
- Cvičenia na spoločné sústredenie s komentovanou spätnou väzbou
- chemické roztoky
- Solute a Solvent: čo sú, rozdiely a príklady
- Koncentrácia roztoku
- Rozpustnosť
- Molarita alebo molárna koncentrácia: čo to je, vzorec a ako vypočítať
- Riedenie roztokov
- Cvičenia o vlastnostiach hmoty

