THE hassium, so symbolom Hs a atómové číslo 108, je jedným z prvkov známych ako transaktinidy. Rovnako ako všetky prvky tejto skupiny sa nenachádza v prírode, pretože je syntetický, okrem toho je rádioaktívny a nestabilný. Za jeho syntézu sa zaslúžili nemecké laboratóriá Helmholtzovho centra pre výskum ťažkých iónov (GSI), v meste Darmstadium v Nemecku a jeho názov bol daný na počesť nemeckého štátu Hesensko, ktorý sa nachádza v centrálnej oblasti rodičov.
Hassium je najťažší prvok, ktorého vlastnosti sa analyzujú prostredníctvom experimentov, ktoré vykonáva samotný GSI. Výsledky boli dôležité na potvrdenie pozície Hs v Periodická tabuľka, ako bola vnímaná podobnosť medzi týmto prvkom a osmiom a ruténiom, ľahšími prvkami skupiny 8.
Prečítajte si tiež:Bohrium — syntetický chemický prvok pomenovaný po Nielsovi Bohrovi
Hassium Zhrnutie
Je to syntetický chemický prvok nachádzajúci sa v skupine 8 periodickej tabuľky.
Bol syntetizovaný Gesellschaft für Schwerionenforschung (GSI) v Darmstadiu v Nemecku.
Je to a rádioaktívny prvok a nestabilné.
Teoretické a experimentálne údaje potvrdzujú, že svojimi vlastnosťami pripomína najľahšie prvky svojej skupiny.
Ako transaktinid sa nemôže vyrábať vo veľkom meradle, okrem toho, že sa vyrába v množstve niekoľkých kusov atómov.
Neprestávaj teraz... Po reklame viac ;)
Vlastnosti hassia
Symbol: hs
Atómové číslo: 108
Atómová hmotnosť: 277 c.u.
Elektronická konfigurácia: [Rn] 7 s2 5f14 6d6
Najstabilnejší izotop: 269Hs (polčas 14 sekúnd)
Chemická séria: skupina 8; transaktinidy; super ťažké prvky.
Vlastnosti Hassium
Hassium je a syntetický prvok a najťažší zo skupiny 8. Považuje sa za a transactinid, práve preto, že sa objavuje v periodickej tabuľke po sérii aktinidov. Rovnako ako všetky transaktinidy, hassium je prvok rádioaktívne a nestabilné.
To znamená, že jeho izotopy dosahujú málo času polovičný život (čas potrebný na to, aby hmotnosť atómov klesla na polovicu). V súčasnosti je známych sedem izotopov hassia, ktorých hmotnosť sa pohybuje od 264 do 270 hodín. Spomedzi všetkých je najstabilnejší izotop 269Hs, s polčasom rozpadu 14 sekúnd.
Hoci krátky polčas rozpadu sťažuje štúdium chemických vlastností transaktinidov, hassium má v tomto smere o niečo viac šťastia. V júni 2001 bolo oznámené, že sa stal najťažší prvok, ktorého vlastnosti sú analyzované.
Tímu sa podarilo v meste Darmstádio v Nemecku vyrobiť asi šesť atómov Hs s polčasom rozpadu približne 10 sekúnd. Hoci sa to zdá málo, stačilo to na potvrdenie, že oxid hassitý, HsO4má silnú podobnosť s oxidmi ľahších prvkov skupiny 8, RuO4 a OsO4, teda ten ruténium to je osmium.
Pozri tiež: Seaborgium — ďalší syntetický chemický prvok s rádioaktívnymi vlastnosťami a krátkym polčasom rozpadu
Získanie Hassium
Transaktinidy majú spoločnú obtiažnosť pri výrobe. Vo všeobecnosti sa vyžaduje najmodernejšie vybavenie ako napr urýchľovače častíc. V týchto sa iónové druhy zrážajú s prvkami vysokých atómová hmotnosť na vytvorenie superťažkých prvkov (v ktorých je zahrnutý Hs).
V prípade hassia štúdie, ktoré potvrdili jeho pozíciu v skupine 8 periodickej tabuľky, zahŕňali jeho výrobu prostredníctvom bombardovania horčíkom-26, pričom cieľom bolo kúrium-248.
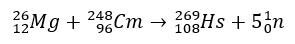
Experimenty s týmito prvkami sú drahé, a preto je bežné, že sa uskutočňujú teoretické štúdie, aby sa presne vypočítali a predpovedali chemické vlastnosti. Krátky polčas je ďalším komplikujúcim faktorom.
Experimentálne techniky separácia a detekcia musí byť veľmi rýchly, aby sa dosiahli dôveryhodné výsledky. Napokon, reakčná účinnosť týchto prvkov je veľmi nízka, pohybuje sa v rozmedzí niekoľkých atómových jednotiek.
Preventívne opatrenia s Hassium
Hs sa nevyrába vo veľkom, a preto sa s ním manipuluje nezahŕňa riziká. Okrem toho sa získava vo výskumných centrách s vysoko kontrolovaným prostredím.
história hassium

Transactinidy boli protagonistami vedeckého sporu kvôli Studená vojna, a Vojna transferov, názov vytvorený v súvislosti so spormi, ktoré sa týkali výroby a rozpoznávania prvkov po fermiu (Fm, Z = 100). Do tohto závodu sa zapojili laboratóriá:
Spojený ústav pre jadrový výskum, mesto Dubna, Rusko;
Lawrence Berkeley National Laboratory v Berkeley v Kalifornii;
Gesellschaft für Schwerionenforschung (GSI, lepšie preložené ako Helmholtzovo centrum pre výskum ťažkých iónov) v Darmstadiu v Nemecku.
V prípade prvku 108 boli zapojené skupiny GSI a Dubna. Hoci dubnskí vedci (na čele s Jurijom Oganessianom) najskôr hlásili prítomnosť prvku 108, zásluhu si pripísali tí z nemeckej skupiny, keďže GSI predložil presvedčivejšie výsledky, pričom v jednom experimente sa mu podarilo vyrobiť tri atómy izotopu 265, zatiaľ čo v inom vyrobil jeden atóm izotopu 264.
Tieto izotopy boli vyrobené pomocou univerzálneho lineárneho urýchľovača (Unilac, lepšie preložené ako univerzálny lineárny urýchľovač), s bombardovaním 208Pb by 58Viera. V roku 1997 Medzinárodná únia čistej a aplikovanej chémie (IUPAC) uznala prvok 108 so symbolom Hs ako Hassium na počesť nemeckej spolkovej krajiny Hesensko.
Cvičenia riešené na hassium
Otázka 1
Hassium, symbol Hs, sa považuje za najťažší prvok, ktorého vlastnosti boli experimentálne študované. V tom čase boli vedci schopní určiť vlastnosti oxidu hasitého, HsO4. V tomto druhu má Hs rovnaké NOx ako ľahšie prvky svojej skupiny, osmium (Os) a ruténium (Ru). Oxidačné číslo Hs v oxide hásnatém sa rovná:
a) 0
B) +2
C) +4
D) +6
E) +8
Rozhodnutie:
Alternatíva E
THE kyslík, keď v a oxid, získava náboj rovný -2. Takže NOx z Hs, ktoré budeme nazývať x, možno vypočítať ako:
x + 4 (-2) = 0
x - 8 = 0
x = +8
otázka 2
Najstabilnejší izotop hassia, Hs, má polčas rozpadu iba 14 sekúnd. To znamená:
A) za 14 sekúnd sa hmotnosť izotopu Hs zdvojnásobí.
B) po 14 sekundách bude hmotnosť izotopu Hs menšia ako polovica pôvodnej hmotnosti.
C) za necelú minútu bude hmotnosť izotopu Hs 1/16 jeho počiatočnej hmotnosti.
D) za jednu minútu bude hmotnosť izotopu Hs presne polovica jeho počiatočnej hmotnosti.
E) za 14 sekúnd sa hmotnosť izotopu Hs vydelí 4.
Rozhodnutie:
Alternatíva C
Polčas udáva čas potrebný na zníženie množstva atómových látok na polovicu. To znamená, že každých 14 sekúnd klesne množstvo Hs na polovicu. Pozorovaním tohto polčasu je jasné, že s 56 sekundami už boli dosiahnuté štyri polčasy, čo spôsobuje, že hmotnosť Hs sa delí 2.4, čo je 16.
Autor: Stefano Araújo Novais
Učiteľ chémie
