Alkoholy môžu podliehať oxidácii, keď sú vystavené oxidačnému činidlu, ako je vodný roztok dvojchrómanu draselného (K2Cr2O7) alebo manganistan draselný (KMnO4) v kyslom prostredí.
Vznikajúci kyslík [O] v strede napadne uhlík spojený s alkoholovou funkčnou skupinou (hydroxyl - OH), ktorá tvorí veľmi nestabilnú zlúčeninu nazývanú dvojitý diol, ktorá má dva hydroxyly spojené s rovnakým uhlíka. Keďže je nestabilná, táto zlúčenina uvoľňuje vodu a dáva vznik novému produktu.
Tento produkt bude závisieť od typu alkoholu, ktorý bol oxidovaný, či už ide o primárny, sekundárny, terciárny alebo metanol.
Stručne povedané, máme:
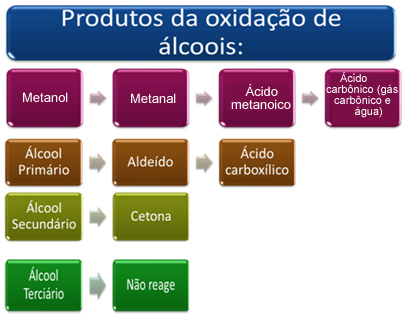
Pozrite si každý prípad nižšie:
- Metanol (H3C─ OH):
Metanol je jediný alkohol, ktorý má tri vodíky viazané na uhlík, ktorý podlieha oxidácii. V tomto prípade, keďže na molekule sú tri body, ktoré môže vznikajúci kyslík napadnúť, dôjde k trom následným oxidáciám, ako je znázornené na obrázku nižšie:
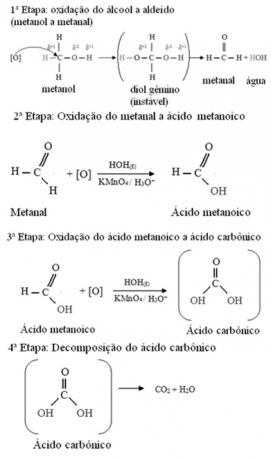
- Primárne alkoholy:
V týchto zlúčeninách je hydroxylový uhlík spojený iba s jedným atómom uhlíka, to znamená, že ďalšie dva ligandy sú vodíky a existujú dve miesta, kde môže vznikajúci kyslík útočiť.
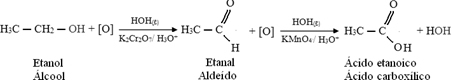
Po prvé, dôjde k tvorbe aldehydu, ako je uvedené nižšie:
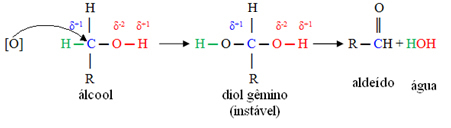
Oxidácia však pokračuje, pretože činidlá používané na oxidáciu alkoholu sú silnejšie ako činidlá používané na oxidáciu aldehydu. Potom ďalší vznikajúci kyslík napadne karbonylový uhlík a vytvorí karboxylovú kyselinu.
Nasleduje príklad oxidácie etanolu, najprv na etanal a potom na kyselinu etánovú (kyselinu octovú). Táto celková reakcia je premena vína na ocot.
Neprestávaj teraz... Po reklame viac ;)
Čiastočná oxidácia etanolu na etanol nastáva, keď alkoholik podstúpi jednorazový dychový test. Vo vnútri tohto zariadenia je tuhá zmes dvojchrómanu draselného a oxidu kremičitého v kyslom prostredí, pričom prebieha nasledujúca reakcia:
K2Cr2O7 (aq) + 4H2IBA4 (aq) + 3 CH3CH2oh(g) → Kr2(LEN4)3 (vod.) + 7 hodín ráno2O(1) + 3 CH3CHO(g) + K2IBA4 (aq)
Oranžováetanol (bezfarebný)zelenáetanal (bezfarebný)
Všimnite si, že okrem oxidácie etanolu (alkoholu) na etanal (aldehyd) dochádza súčasne k redukcii dichrómanu, ktorý je oranžový, na chróm (III) alebo dokonca chróm (II), ktorý je zelený. Zmena farby bude naznačovať, že osoba má viac alkoholu v krvi, ako je povolené.
- Sekundárne alkoholy:
Sú to zlúčeniny, v ktorých je hydroxylový uhlík viazaný na dva ďalšie atómy uhlíka a iba na jeden atóm vodíka. Preto bude existovať iba jedno miesto v molekule, kde môže nastupujúci kyslík napadnúť a vytvorí sa iba jeden typ produktu, ktorým bude vždy ketón:
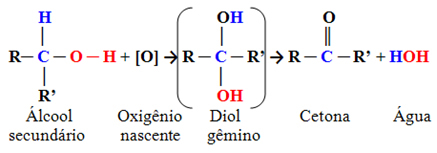
Pretože na karbonylovom uhlíku ketónu nie je priamo viazaný žiadny vodík, neexistuje už žiadna možnosť ďalšej oxidácie. Preto sa reakcia zastaví na ketóne.
- Terciárne alkoholy:
Terciárne alkoholy sú tie, v ktorých uhlík, ktorý má -OH skupinu, vytvára tri väzby s inými atómami uhlíka. Keďže sa neviažu s vodíkmi, na molekule nie je žiadny bod, ktorý by mohol napadnúť vznikajúci kyslík. Vďaka tejto skutočnosti terciárne alkoholy nepodliehajú oxidácii.
* Zdroj a autor obrázku: CostaPPPR.
Autor: Jennifer Fogaça
Vyštudoval chémiu
Chceli by ste odkázať na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. "Oxidácia alkoholov"; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/oxidacao-dos-alcoois.htm. Prístupné 27. júla 2021.
Chémia

Ako funguje dychový analyzátor, koncentrácia alkoholu, alkohol tester, reakcie zahŕňajúce etylalkohol, druhy dychové analyzátory, dvojchróman draselný, palivový článok, katalyzátor, uvoľňovanie elektrónov, kyselina octová, vodík, konc