Z tejto zmesi plynov vznikajú homogénne zmesi alebo plynné roztoky. Vzduchom sa šíria napríklad plyny, ktoré vychádzajú z továrenských komínov, či výfukov áut atmosférické a postupom času sme ich už nedokázali rozlíšiť, nakoľko dochádzalo k difúzii týchto plynov cez vzduchu.

Plyny emitované komínmi sa rozptyľujú a „stratia“ v atmosférickom vzduchu, pretože objem vzduchu je oveľa väčší ako objem dymu.
| THE difúzia plynu je samovoľný pohyb plynu cez iný, to znamená jeho šírenie v inom plynnom prostredí. |
| THE výpotok plynov je zvláštny typ difúzie, pri ktorej dochádza k úniku plynov cez malé otvory (alebo porézne steny, čo je súbor malých otvorov). |
Napríklad balóny predávané deťom sú plnené héliom. Postupom času tento plyn prechádza cez gumové póry balóna, to znamená, že dochádza k jeho výronu. Dokazuje to skutočnosť, že balón sa po niekoľkých hodinách vyfúkne.
Škótsky chemik Thomas Graham v roku 1829 študoval toto správanie plynov. Dospel k záveru, že rýchlosť, ktorou plyn difunduje alebo vyteká do iného, súvisí s jeho hustotou. Keď sa jeho experimentálne údaje opakovali pre všetky plyny, vytvoril nasledujúci zákon, ktorý nesie jeho meno:
Grahamov zákon: rýchlosť difúzie alebo efúzie plynu je nepriamo úmerná druhej odmocnine jeho hustoty.
Matematicky možno tento zákon vyjadriť rovnicou:
v α 
Alebo, pokiaľ ide o dva rôzne plyny, máme:
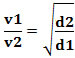
Jednotka použitá v tomto prípade je „objem, ktorý unikne za jednotku času“; teda všeobecne L/min (litrov za minútu).
Plyny s nižšou hustotou teda difundujú rýchlejšie. Ak je v rovnakých teplotných a tlakových podmienkach, môžete to tiež spojiť s hmotnosťou molárny plyn: čím väčšia je hustota plynu, tým väčšia je jeho molárna hmotnosť a tým nižšia je jeho rýchlosť difúzia; a naopak. Máme teda:
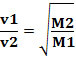
Autor: Jennifer Fogaça
Vyštudoval chémiu
Brazílsky školský tím
Zdroj: Brazílska škola - https://brasilescola.uol.com.br/quimica/difusao-efusao-dos-gases.htm