O teplo je tepelná energia prenášaná medzi dvoma telesami motivovaná rozdielom v teplota. Táto energia vždy prúdi z tela s najvyššou teplotou do tela s najnižšou teplotou a jej tok prestane, až keď sa teplota zúčastnených telies vyrovná.
Druhy tepla
Pri vystavení tepelnému zdroju môže akýkoľvek materiál meniť svoju teplotu alebo meniť svoju teplotu. fyzikálny stav agregácie molekúl.
hovorí sa horúčava citlivý keď je schopný meniť iba teplotu tela. hovorí sa horúčava latentný keď mení teplotu a generuje zmenu v stave agregácie molekúl látky.
Výpočet latentného tepla
Množstvo latentné teplo je určená súčinom hmotnosti (m) tela, ktoré prešlo transformáciou stavu a takzvaným latentným teplom fúzie alebo odparovania (L).
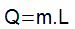
Množstvo tepla potrebné pre každý gram látky na zmenu stavu sa nazýva latentné teplo odparovania alebo fúzie. Napríklad v prípade vody je latentné odparovacie teplo 540 kal / g, to znamená, že každý gram voda pri 100 ° C potrebuje na prechod z kvapalného stavu do 540 kal tepla plynný.
Príklady
1. príklad (Uerj) - Nasledujúci graf ukazuje tepelné správanie 10 g látky, ktorá pri príjme tepla zo zdroja úplne prechádza z pevnej fázy do kvapalnej fázy.

Latentné teplo fúzie tejto látky v kal / g sa rovná:
a) 70
b) 80
c) 90
d) 100
Odpoveď: Písmeno A
Vodorovná časť grafu predstavuje zmenu fyzikálneho stavu, v ktorom teplo prestáva pôsobiť pri teplotných výkyvoch a začína pôsobiť takým spôsobom, že mení agregačný stav prvku. V tejto časti grafu bolo zahrnuté množstvo tepla 700 kal. (1 000 - 300 = 700 kal.).
Latentné teplo fúzie možno určiť z rovnice latentného tepla:
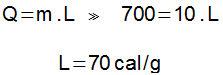
2. príklad - Hmotnosť 2 000 g vody je presne pri 100 ° C. S vedomím, že odparovacie teplo vody je 540 kal / g, určte množstvo tepla v kcal potrebné na odparenie 30% hmotnosti vody.
a) 224
b) 250
c) 300
d) 360
e) 324
Odpoveď: Písmeno E
Hmotnosť vody, ktorá sa má brať do úvahy, je 600 g, čo zodpovedá 30% z celkovej vody. Množstvo tepla potrebného na odparenie teda bude:

Joab Silas
Vyštudoval fyziku
Zdroj: Brazílska škola - https://brasilescola.uol.com.br/o-que-e/fisica/o-que-e-calor-latente.htm
