Uhľovodíky sú zlúčeniny tvorené iba uhlíkom a vodíkom so všeobecným vzorcom: CXHr.
Je to rozsiahle množstvo látok, z ktorých najznámejšie sú zložky ropy a zemného plynu.
Kostra uhľovodíka je tvorená uhlíkom a atómy vodíka sa následne viažu prostredníctvom kovalentnej väzby.
Používajú sa často v chemickom priemysle a majú zásadný význam pri výrobe ropných derivátov: okrem iného palivá, polyméry, parafíny.
Vlastnosti uhľovodíkov
| molekulárna interakcia | Sú to prakticky nepolárne zlúčeniny a ich molekuly sú spojené indukovaným dipólom. |
|---|---|
| Teplota topenia a varu | V porovnaní s polárnymi zlúčeninami sú nízke. |
| agregačné stavy |
|
| Hustota | Majú nižšiu hustotu ako voda. |
| Rozpustnosť | Sú nerozpustné vo vode a rozpustné v nepolárnych látkach. |
| Reaktivita |
|
Klasifikácia uhľovodíkov
Pokiaľ ide o formu hlavného uhlíkového reťazca, uhľovodíky sa delia na:
alifatické uhľovodíky
Tvorené otvorenými alebo acyklickými uhlíkovými reťazcami, ktoré majú konečné uhlíky.
- alkány
- alkény
- Alkyny
- Alkadienov
Príklad:
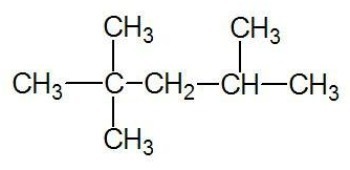
Pozri tiež: uhlíkové reťazce
Cyklické uhľovodíky
Tvorené uzavretými alebo cyklickými uhlíkovými reťazcami, ktoré nemajú konečné uhlíky.
- Cyklány
- Cykly
- cyklistov
- Aromatické látky
Príklady:
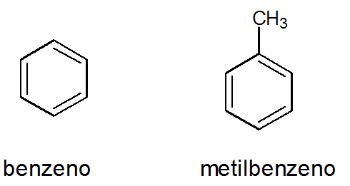
Pozri tiež: benzén
Pokiaľ ide o väzby uhlíkových reťazcov, či už jednoduché, dvojité alebo trojité:
Nasýtené uhľovodíky
Zlúčeniny sú tvorené jednoduchými väzbami medzi atómami uhlíka a vodíka.
- alkány
- Cyklány
Príklad:
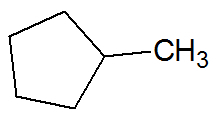
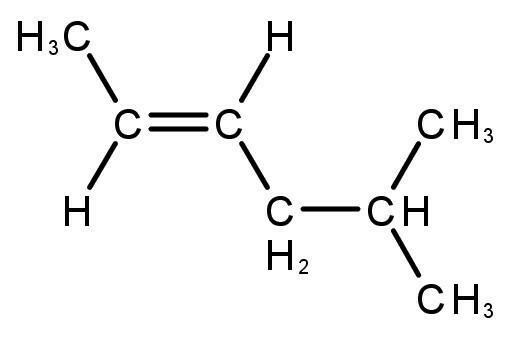
nenasýtené uhľovodíky
Vytvorené zlúčeniny majú dvojité alebo trojité väzby medzi atómami uhlíka a vodíka.
- alkény
- Alkyny
- Alkadienov
- Cykly
- cyklistov
- Aromatické látky
Prečítajte si tiež o:
- Chemické väzby
- Organická chémia
- Organické funkcie
Nomenklatúra
Nomenklatúra uhľovodíkov je definovaná týmito výrazmi:
| PREFIX | SPROSTREDKOVATEĽ | DOSTATOK |
|---|---|---|
| Udáva počet uhlíkov prítomných v reťazci. | Typ odkazu nájdeného v reťazci. | Identifikácia funkčnej skupiny. |
| PREFIX | SPROSTREDKOVATEĽ | DOSTATOK | ||
|---|---|---|---|---|
| 1C | MET | Iba jeden odkaz | AN | O |
| 2C | ET | |||
| 3C | PROP | dvojitá väzba | EN | |
| 4C | ALE | |||
| 5C | PENT | dve dvojité väzby | DIEN | |
| 6C | ŠESTÁ | |||
| 7C | HEPT | trojitý odkaz | IN |
|
| 8C | ZKÚ | |||
| 9C | NIE | Dva trojité odkazy | DIIN | |
| 10C | DEC |
Príklady
Postupujte podľa toho, ako sa tvoria názvy uhľovodíkov:
| Ethane |
- Predpona: ET, čo zodpovedá 2 uhlíkom.
- Sprostredkovateľ: AN, čo zodpovedá jednotlivým odkazom.
- Prípona: O, čo zodpovedá uhľovodíkovej funkcii.
Pozrite sa na ďalšie príklady:
| Propán | |
| Etén | |
| Etino | |
| propadiene |
V niektorých prípadoch je potrebné označiť polohu dvojitej alebo trojitej väzby. Číslovanie musí začínať od najbližšieho konca tohto odkazu.
| 1,3-butadién | |
| 1-butín |
Viac informácií sa dozviete na:
- Bután
- Metán
Druhy uhľovodíkov
Zoznámte sa s hlavnými typmi uhľovodíkov, ich charakteristikami a použitými zlúčeninami:
alkány
Sú to uhľovodíky s otvoreným reťazcom s jednoduchými väzbami medzi atómami uhlíka a vodíka, ktorých všeobecný vzorec je ÇčH2n + 2.
Alkánové charakteristiky
- Tiež sa nazývajú parafíny alebo parafíny.
- Nachádzajú sa v prírode v zemnom plyne a rope.
- Používajú sa ako palivo: plyn na varenie, benzín, nafta atď.
Príklady alkánov

alkény
Sú to uhľovodíky s otvoreným reťazcom a majú dvojitú väzbu, ktorej všeobecný vzorec je ÇčH2n.
Alkenove vlastnosti
- Nazývajú sa tiež olefíny, alkény alebo etylénové uhľovodíky.
- Priemyselne sa získavajú krakovaním alkánov prítomných v rope.
- Používajú sa ako surovina v priemysle: plasty, farbivá, výbušniny atď.
Príklady alkénov

Alkyny
Sú to uhľovodíky s otvoreným reťazcom s prítomnosťou dvojitej väzby, ktorej všeobecný vzorec je ÇčH2n-2.
Alkynové charakteristiky
- Vďaka trojitej väzbe sú reaktívnejšie ako alkány a alkény.
- Alkyny s viac ako 14 atómami uhlíka sú tuhé.
- Najpoužívanejším alkínom je acetylén, ktorý sa bežne používa na výrobu syntetických kaučukov, textilných vlákien a plastov.
Príklady alkínov

Alkadienov
Sú to uhľovodíky s otvoreným reťazcom a prítomnosť dvoch dvojitých väzieb, ktorých všeobecný vzorec je ÇčH2n-2
Charakteristika alkadiénov
- Tiež sa nazývajú diény alebo diolefíny
- V prírode sa nachádzajú v terpénoch, ktoré sa získavajú z éterických ovocných olejov.
- Najznámejšou zlúčeninou je izoprén, ktorý sa nachádza v prírodnom kaučuku a éterických olejoch.
Príklady alkadiénov

Cyklány
Sú to uhľovodíky s uzavretým reťazcom s jednoduchými väzbami medzi atómami uhlíka a vodíka, ktorých všeobecný vzorec je ÇčH2n.
Cyklické vlastnosti
- Tiež sa nazývajú cykloalkány alebo cykloparafíny.
- Pri pôsobení vysokého tlaku sú nestabilné.
- Reťaze s viac ako 6 atómami uhlíka sú stabilné, zatiaľ čo reťazce s menej ako 5 atómami uhlíka sú reaktívne.
Príklady cyklánov

Cykly
Sú to uhľovodíky s uzavretým reťazcom s prítomnosťou dvojnej väzby, ktorej štruktúrny vzorec je ÇčH2n-2.
Charakteristika cyklénov
- Tiež sa nazývajú cykloalkény.
- Zlúčeniny s 3 až 5 uhlíkmi sú nestabilné.
- Spravidla sa nachádzajú v zemnom plyne, nafte a rope.
Príklady cyklénov
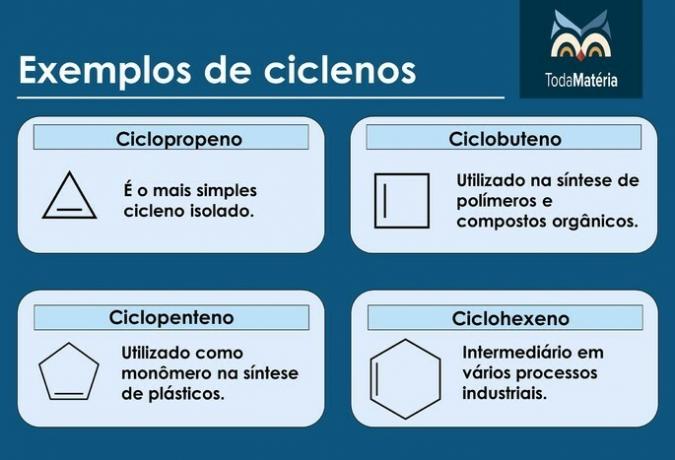
cyklistov
Sú to uhľovodíky s uzavretým reťazcom s prítomnosťou trojitej väzby, ktorej štruktúrny vzorec je ÇčH2n-4.
Cyklistické vlastnosti
- Tiež sa nazývajú cykloalkyny alebo cykloalkyny.
- Sú to cyklické a nenasýtené uhľovodíky.
- Sú nestabilné v dôsledku trojitého spojenia a nenachádzajú sa v prírode.
Príklady cyklínov

Aromatické látky
Sú to uzavreté reťazce uhľovodíkov so striedavými jednoduchými a dvojitými väzbami.
Charakteristika aromatických látok
- Hovorí sa im aj arény.
- Sú to nenasýtené zlúčeniny, pretože majú 3 dvojité väzby.
- Skladajú sa z najmenej jedného aromatického kruhu.
Príklady aromatických látok
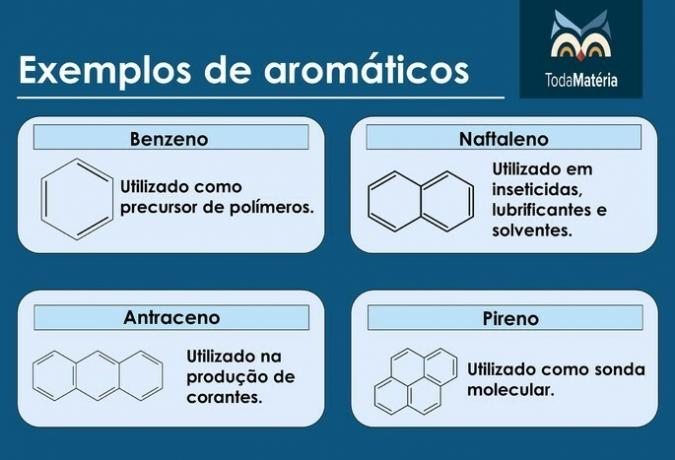
- Ropa
- rafinácia ropy
- Acetylén
Zhrnutie uhľovodíkov
| Zamestnanie | Všeobecný vzorec |
Vlastnosti |
|---|---|---|
| alkán | Otvorená reťaz s jednoduchými článkami. |
|
| alkén | Otvorená reťaz s dvojitou väzbou. | |
| alkín | Otvorená reťaz s trojitou väzbou. | |
| alkadién | Otvorená reťaz s dvoma dvojitými väzbami. | |
| Cyklány | Uzavretá reťaz s jednoduchými spojmi. | |
| Cykly | Uzavretá reťaz s dvojitou väzbou. | |
| cyklistov | Uzavretá reťaz s trojitým článkom. | |
| Aromatické | Variabilné | Uzavretý reťazec so striedajúcimi sa jednoduchými a dvojitými väzbami. |
Cvičenia o uhľovodíkoch
1. (UEMA) LPG (skvapalnený ropný plyn), tiež ľudovo známy ako plyn na varenie, je palivo neobnoviteľné fosílie, ktoré môžu vyčerpať cez noc, ak sa nepoužívajú s plánovaním a bez nich prebytok. Skladá sa okrem iných plynov z propánu C.3H8bután C.4H10 a malé množstvá propylénu C3H6 a butén C.4H8. Tieto organické zlúčeniny sú klasifikované ako uhľovodíky, ktoré sa navzájom líšia. Na základe typu väzby medzi uhlíkmi a klasifikácie uhlíkového reťazca vyššie uvedených zlúčenín možno konštatovať, že:
a) nenasýtené zlúčeniny sú propán a bután.
b) nenasýtené zlúčeniny sú propén a butén.
c) nenasýtené zlúčeniny sú propén a bután.
d) zlúčeniny majú homocyklické reťazce.
e) zlúčeniny majú heterocyklické reťazce.
Alternatívne b) nenasýtené zlúčeniny sú propén a butén.
a) NESPRÁVNE. Tieto zlúčeniny nemajú nenasýtenie, ich väzby sú jednoduché.
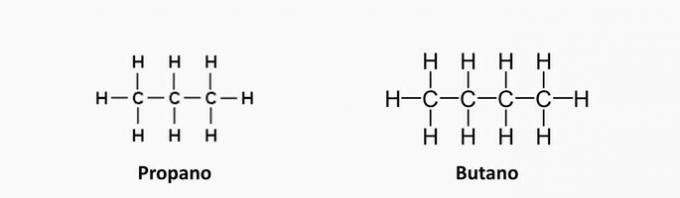
b) SPRÁVNE. Termín „en“ označuje prítomnosť dvojitých väzieb v zlúčeninách.

c) NESPRÁVNE. Bután nemá žiadne nenasýtenia.

d) NESPRÁVNE. Tieto reťazce sú uzavreté a atómy uhlíka sú spojené jednoduchými väzbami.
e) NESPRÁVNE. Tieto reťazce majú heteroatóm, ako je kyslík a dusík.

2. (Uel) Jeden z uhľovodíkov so vzorcom C.5H12 môže mať uhlíkový reťazec:
a) nasýtený cyklický.
b) heterogénna acyklická.
c) rozvetvený cyklický.
d) nenasýtené otvorené.
e) otvorené rozvetvené.
Alternatíva e) otvorené rozvetvené.
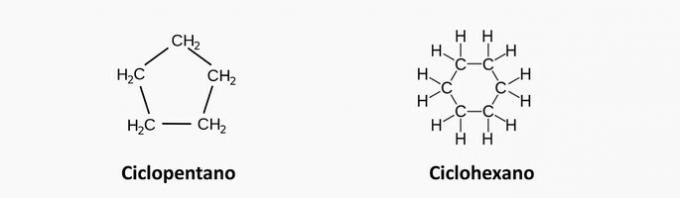
a) NESPRÁVNE. Nasýtená cyklická zlúčenina zodpovedá cyklánu, ktorého vzorec je CčH2n.
Príklad:
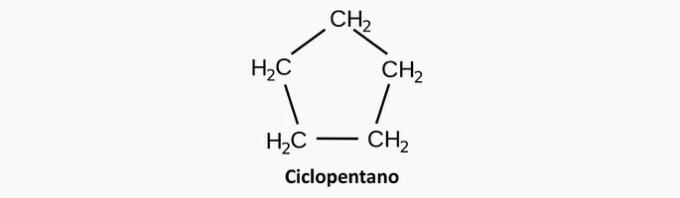
b) NESPRÁVNE. Heterogénna acyklická zlúčenina má okrem interkalovaného uhlíka v reťazci aj prítomnosť ďalšieho prvku.
Príklad:
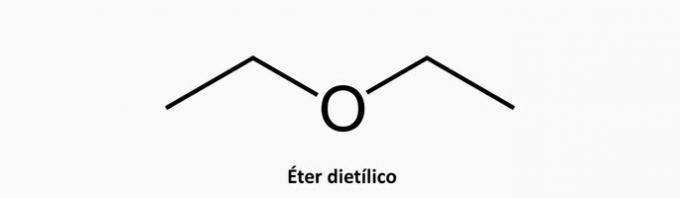
c) NESPRÁVNE. Rozvetvená cyklická zlúčenina má vzorec C.čH2n.
Príklad:
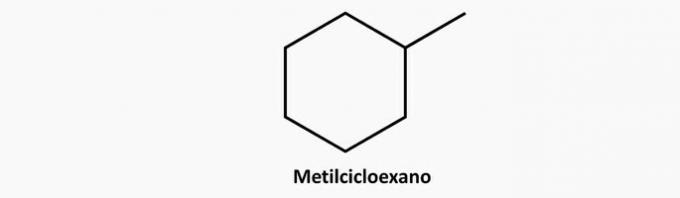
d) NESPRÁVNE. Nenasýtenou zlúčeninou s otvoreným reťazcom môže byť alkén alebo alkín, ktorých vzorec je C.čH2n a C.čH2n-2.
Príklady:
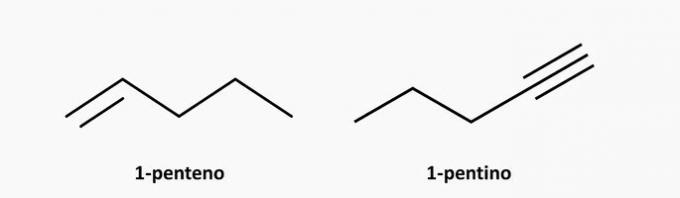
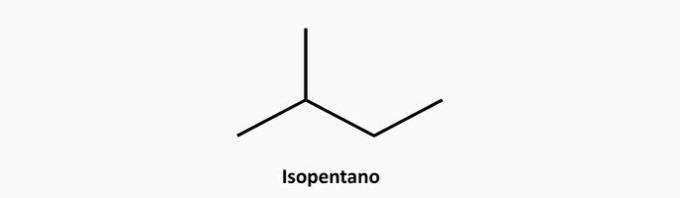
e) SPRÁVNE. Rozvetvenou zlúčeninou s otvoreným reťazcom je alkán, ktorého vzorec je CčH2n + 2. Zlúčeninou s 5 atómami uhlíka a 12 atómami vodíka môže byť izopentán.
Príklad:
3. (PUC) Alkyny sú uhľovodíky:
a) nasýtené alifatické látky.
b) nasýtené alicyklické skupiny.
c) nenasýtené alifatické látky s dvojnou väzbou.
d) nenasýtené alicyklické zlúčeniny s trojnou väzbou.
e) nenasýtené alifatické látky s trojnými väzbami.
Alternatíva e) nenasýtené alifatické látky s trojnou väzbou.
a) NESPRÁVNE. Zlúčeninami s otvoreným reťazcom a jednoduchými väzbami sú alkány.
Príklad:

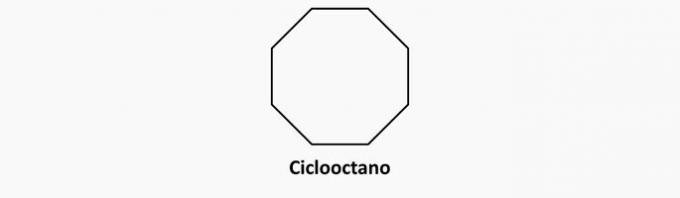
b) NESPRÁVNE. Cyklické zlúčeniny s jednoduchými väzbami sú cyklány.
Príklad:
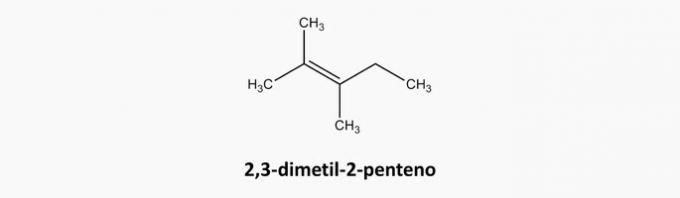
c) NESPRÁVNE. Zlúčeninami s otvoreným reťazcom a dvojne viazanými zlúčeninami sú alkény.
Príklad:
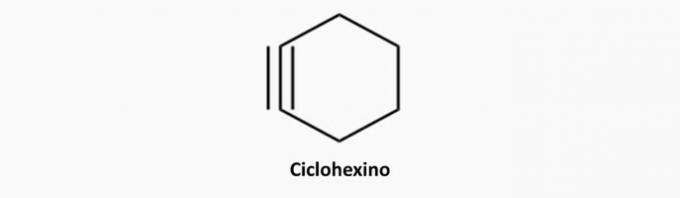
d) NESPRÁVNE. Cyklické a trojito viazané zlúčeniny sú cyklíny.
Príklad:
e) SPRÁVNE. Alkyny sú zlúčeniny s otvoreným reťazcom a trojité väzby.

Chcete si stále overovať svoje vedomosti? Nezabudnite si pozrieť tieto zoznamy:
- Cvičenia o uhľovodíkoch
- Cvičenia z organickej chémie
- Cvičenia o organických funkciách

