Čistá látka je tvorená jedným typom chemických látok, to znamená, že jej zloženie a vlastnosti sú nemenné. Mix obsahuje viac ako jeden typ komponentu, takže jeho organizácia sa líši.
Čistú látku od zmesi teda môžeme odlíšiť iba vtedy, keď poznáme jej zloženie.
Pri porovnaní pohára vody a pohára rozpusteného cukru si naše oči nevšimnú žiadny rozdiel. Ak však pohltíme obsah týchto dvoch pohárov, všimneme si, že jeden je čistá látka a druhý je zložený zo zmesi.
čisté látky
Čistá látka je sada iba jedného chemického druhu, to znamená, že nie je zmiešaná s ostatnými.
Ako príklad uvedieme vodu. Voda (H2O) je uznávaný pre svoje vlastnosti a špecifické vlastnosti tohto materiálu nám ho pomáhajú identifikovať. Hlavný vlastnosti vody oni sú:
| Hustota | 1,00 g / cm3 |
|---|---|
| Bod fúzie | 0 ° C |
| Bod varu | 100 ° C |
Keď má materiál po celú dobu fixné a nemenné vlastnosti, hovoríme, že je to čistá substancia.
Keď dáme kuchynskú soľ, chlorid sodný (NaCl), do pohára s vodou a miešame, dôjde k zmene.

Výsledkom je produkt so strednou hustotou medzi vodou a soľou. Je to preto, že voda už nie je čistou látkou a stala sa Zmiešať.
Pri pokuse o zmrazenie tejto zmesi si všimnete, že teplota topenia bude nižšia ako 0 ° C a to tiež táto zmes nebude vrieť pri 100 ° C, na jej odparenie bude potrebné viac tepla výrobok.
Čisté jednoduché a zložené látky
Čisté látky sa klasifikujú ako jednoduché, ak v ich zložení sú atómy iba jedného chemického prvku.
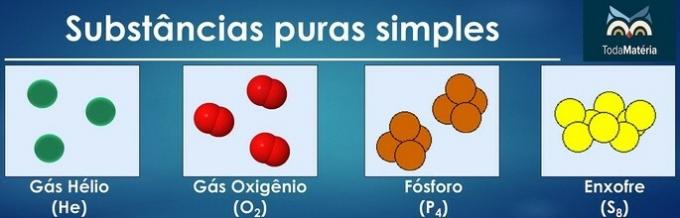
Usporiadanie atómov dvoch alebo viacerých chemických prvkov vytvára čisté zložené látky.

Zmesi
Zmes zodpovedá spojeniu dvoch alebo viacerých čistých látok, ktoré sa nazývajú zložky.
Na rozdiel od čistých látok nie sú jeho vlastnosti stále, pretože závisia od podielu zložiek v zmesi.
Zistite, ako sa hustota, fyzikálna vlastnosť, líši podľa množstva soli zmiešanej s vodou.
| Percento soli v celková hmotnosť zmesi |
Hustota zmesi (g / cm3) pri 20 ° C |
|---|---|
| 1 | 1,005 |
| 8 | 1,056 |
| 12 | 1,086 |
| 16 | 1,116 |
| 26 | 1,197 |
Zdroj: FURNISS, B. S. a kol. Vogelova učebnica praktickej organickej chémie. 4. vyd. London: Longman, 1987. P. 1.312.
Pridanie vody a soli v akomkoľvek pomere má preto premenlivú hustotu, a preto nemôžeme zmes klasifikovať ako vodu alebo soľ.
Homogénne a heterogénne zmesi
Homogénne zmesi sú tie, ktoré poskytujú zložky iba v jednej fáze, a preto majú vo všetkých bodoch rovnaké vlastnosti.

Keď vizuálne vnímame viac ako jednu fázu, potom je zmes klasifikovaná ako heterogénna.

Zhrnutie o čistých látkach a zmesiach
| Čisté látky a zmesi | |
|---|---|
|
homogénny systém (iba jedna fáza) |
čistá substancia (jedna zložka) |
|
homogénna zmes (viac ako jeden komponent v tej istej fáze) | |
|
heterogénny systém (viac ako jedna fáza) |
čistá substancia (zložka v rôznych fyzikálnych stavoch) |
|
heterogénna zmes (viac ako jedna zložka vo viac ako jednej fáze) |
Ak sa chcete dozvedieť viac, nezabudnite si prečítať tieto texty:
- Atómy
- Chemické prvky
- Oddelenie zmesí
Cvičenia s komentovanou spätnou väzbou
1. (UFMG) Vo vzorke čistej látky X boli stanovené niektoré jej vlastnosti. Všetky alternatívy majú vlastnosti užitočné pri identifikácii tejto látky, s výnimkou:
a) hustota.
b) hmotnosť vzorky.
c) rozpustnosť vo vode.
d) teplota varu.
e) teplota topenia.
Nesprávna alternatíva: b) hmotnosť vzorky.
a) SPRÁVNE. Hustota je množstvo hmoty v danom objeme. Ako vlastnosť špecifická pre materiál je užitočná na identifikáciu látky.
b) NESPRÁVNE. Hmotnosť je množstvo hmoty v tele. Pretože sa táto vlastnosť vzťahuje na akúkoľvek hmotu, bez ohľadu na jej zloženie, nie je možné ju použiť na identifikáciu látky.
c) SPRÁVNE. Rozpustnosť je schopnosť látky rozpustiť sa v danej kvapaline alebo nie. Ako vlastnosť špecifická pre materiál je užitočná na identifikáciu látky.
d) SPRÁVNE. Teplota varu zodpovedá teplote prechodu z kvapalného do plynného skupenstva. Ako vlastnosť špecifická pre materiál je užitočná na identifikáciu látky.
e) SPRÁVNE. Teplota topenia zodpovedá teplote prechodu z kvapalného do tuhého skupenstva. Ako vlastnosť špecifická pre materiál je užitočná na identifikáciu látky.
2. (Vunesp) Štítok fľaše minerálnej vody je uvedený nižšie.
| Pravdepodobné chemické zloženie: |
|---|
| Síran vápenatý 0,0038 mg / L |
| Hydrogenuhličitan vápenatý 0,0167 mg / l |
Na základe týchto informácií môžeme minerálnu vodu klasifikovať ako:
a) čistá látka.
b) jednoduchá látka.
c) heterogénna zmes.
d) homogénna zmes.
e) koloidná suspenzia.
Správna alternatíva: d) homogénna zmes.
a) NESPRÁVNE. Voda by bola čistá, keby jej zloženie malo iba molekuly H.2O.
b) NESPRÁVNE. Jednoduchá látka sa skladá z atómov iba jedného chemického prvku. Čistá voda tiež nie je jednoduchou látkou, pretože je tvorená atómami vodíka a kyslíka (H2O) je klasifikovaný ako kompozitný.
c) NESPRÁVNE. Heterogénna zmes má viac ako jednu fázu, v takom prípade môžeme pozorovať iba vodu.
d) SPRÁVNE. Pretože má iba jednu fázu, je systém homogénny. Pri pohľade na fľašu s vodou vidíme iba kvapalinu, pretože zlúčeniny síranu vápenatého a hydrogenuhličitanu vápenatého sú rozpustné vo vode, a preto sú rozpustené.
e) NESPRÁVNE. Koloidná suspenzia je heterogénna zmes, ktorej zložky sa diferencujú pomocou mikroskopu.
3. (UCDB) V chemickom laboratóriu sa pripravovali nasledujúce zmesi:
I. voda / benzín
II. voda / soľ
III. voda / piesok
IV. benzín / soľ
V. benzín / piesok
Ktoré z týchto zmesí sú homogénne?
a) Žiadne.
b) Iba II.
c) II a III.
d) I a II.
e) II a IV.
Správna alternatíva: b) Iba II.
a) NESPRÁVNE. Voda je anorganická zlúčenina a benzín organická zlúčenina. Tieto látky nemajú schopnosť vzájomného pôsobenia a pretože majú rôznu hustotu, vytvárajú heterogénnu zmes.
b) SPRÁVNE. Soľ, chlorid sodný, sa rozpúšťa vo vode za vzniku roztoku, ktorý je homogénnou zmesou.
c) NESPRÁVNE. Piesok, oxid kremičitý, vytvára s vodou heterogénnu zmes.
d) NESPRÁVNE. Soľ je anorganická zlúčenina a benzín ako organická zlúčenina. Tieto látky nemajú schopnosť vzájomného pôsobenia a pretože majú rôznu hustotu, vytvárajú heterogénnu zmes.
e) NESPRÁVNE. Piesok je anorganická zlúčenina a benzín je organická zlúčenina. Tieto látky nemajú schopnosť vzájomného pôsobenia, a preto tvoria heterogénnu zmes.
4. (Ufes) V dobre zmiešanom systéme pozostávajúcom z piesku, soli, cukru, vody a benzínu je počet fáz:
a) 2.
b) 3.
c) 4.
d) 5.
e) 6.
Správna alternatíva: b) 3.
FÁZA 1: Soľ a cukor sú schopné interagovať s vodou a prostredníctvom medzimolekulových síl sa molekuly viažu a vytvárajú roztok, ktorý je homogénnou zmesou.
FÁZA 2: Voda je anorganická zlúčenina a benzín organická zlúčenina. Tieto látky nemajú schopnosť vzájomného pôsobenia a pretože majú rôznu hustotu, vytvárajú heterogénnu zmes.
FÁZA 3: Piesok je kremičitan, ktorý nemá chemickú afinitu k vode a benzínu, a preto predstavuje fázu.
5. (Mackenzie) Zmes tvorená:
a) kocky ľadu a vodný roztok cukru (glukóza).
b) N plynov2 a CO2.
c) voda a acetón.
d) voda a egrešový sirup.
e) petrolej a nafta.
Správna alternatíva: a) kocky ľadu a vodný roztok cukru (glukóza).
a) SPRÁVNE. Je možné pozorovať dve fázy: kocky ľadu a roztok glukózy, ide teda o heterogénny systém.
b) NESPRÁVNE. Plyny sú vždy homogénna zmes.
c) NESPRÁVNE. Medzi karbonylom propanónu a molekulou vody sa tvoria vodíkové väzby. Pretože sú to polárne látky, je acetón schopný solubilizovať vo vode a vytvárať homogénnu zmes.
d) NESPRÁVNE. Tieto dve zložky sa zmiešajú a vytvoria homogénny systém, pretože z egrešového sirupu uvidíme iba červenú tekutinu, pretože k zriedeniu dôjde pridaním vody.
e) NESPRÁVNE. Obidve sú organické zlúčeniny a vďaka chemickej afinite tvoria jednu fázu, ktorá predstavuje homogénny systém.
Otestujte si svoje vedomosti na cvičeniach:
- Cvičenie na homogénne a heterogénne zmesi
- Cvičenie na separáciu zmesí
- Cvičenia z vlastností hmoty



