Povrchové napätie je jav, ktorý sa vyskytuje na povrchu tekutín, napríklad vody, a vytvára tenký film.
Keď voda v tekutom stave obsadí nádobu, môžeme vnímať oddelenie medzi kvapalinou a okolitým prostredím. Je to tak preto, lebo interakcia medzi molekulami vody na povrchu sa líši od interakcií vo vnútri kvapaliny.
Na povrchu molekula vody interaguje s molekulami po stranách a pod ňou. Vo vnútri je molekula obklopená ďalšími molekulami a dochádza k interakcii vo všetkých smeroch prostredníctvom vodíkových väzieb.
Práve kvôli tejto vlastnosti pozorujeme jav tvorby kvapôčky. Z tohto dôvodu je tiež možné, aby hmyz chodil po vode.
Čo je to povrchové napätie?
Je to tvorba tenkého filmu pod tekutinou v dôsledku nerovnosti príťažlivosti medzi molekulami, ktoré ho tvoria. Tento jav sa vyskytuje výraznejšie v tekutinách, ktoré majú medzimolekulové sily intenzívne, ako voda.
Interakcie medzi druhmi v kvapaline sa nazývajú kohézne sily. Zatiaľ čo molekuly vo vnútri kvapaliny sú priťahované k susedným molekulám vo všetkých smeroch, molekuly na povrchu interagujú s molekulami pod a vedľa nich.
Zistite, ako dochádza k povrchovému napätiu vo vode.
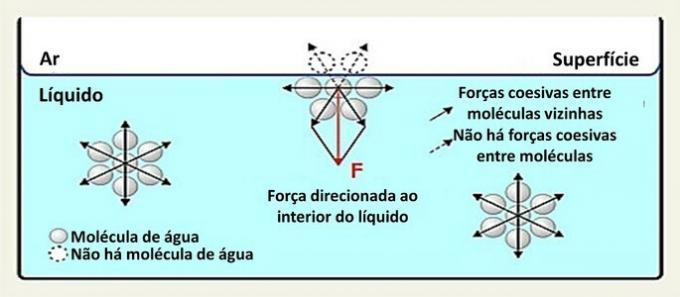
Voda (H2O) je polárna molekula tvorená 2 atómami vodíka (kladné póly) a jedným atómom kyslíka (záporný pól) spojeným spolu Kovalentné väzby. Kladný pól molekuly je priťahovaný k zápornému pólu susednej molekuly a vytvára vodíkové väzby.
Tento typ interakcie v kvapaline je distribuovaný vo všetkých smeroch. Na povrchu sú sily smerované nadol a do strán, pretože nad nimi nie sú molekuly vody. Vďaka tomu sú povrchové molekuly súdržnejšie a vytvára sa elastický film.
Jednotka povrchového napätia je daná kvocientom medzi jednotkou sily a jednotkou dĺžky, pričom najpoužívanejšie sú dyn / centimeter (dyn / cm) a newton / meter (N / m).
Voda má vysoké povrchové napätie, ktorého hodnota je 72,75 dynu / cm. Ortuť, tekutý kov, má však povrchové napätie približne 7-krát väčšie ako voda, 475 dynov / cm.
Chcete vedieť viac? Skontrolujte teda nasledujúce texty:
- Vlastnosti vody
- Polárne a nepolárne molekuly
- Chemické väzby
Javy spôsobené povrchovým napätím
Povrchové napätie je zodpovedné za niektoré javy, ktoré pozorujeme v každodennom živote. Hlavné sú:
Zvieratá, ktoré chodia po vode

Hmyz, pavúky a iné zvieratá môžu chodiť alebo odpočívať na Voda pretože na končatinách jeho labiek sú chĺpky potiahnuté mastnou látkou, a preto nemôžu preniknúť medzi molekuly vody spojené na povrchu.
Tvorba vodných kvapiek

Vodné kvapôčky sú sférické kvôli kontrakcii v molekuly povrchu spôsobeného povrchovým napätím. Guľa sa vyskytuje, pretože ide o geometrický tvar, v ktorom je najmenší vzťah medzi povrchovou plochou a objemom. Sférický tvar preto udržuje najmenší počet molekúl vody v kontakte so vzduchom.
Cvičenie povrchového napätia vody
1. Povrchovo aktívna látka je látka, ktorá na inú látku pôsobí:
a) osmolarita.
b) Povrchové napätie.
c) Elektroforéza.
d) Viskozita.
e) Osmotický tlak.
Správna alternatíva: b) Povrchové napätie.
a) NESPRÁVNE. Osmolarita súvisí s množstvom rozpustených častíc, ktoré sú obsiahnuté v danom objeme rozpúšťadla.
b) SPRÁVNE. Čistiace prostriedky aj mydlá znižujú povrchové napätie vody a všeobecne sa o nich hovorí povrchovo aktívne látky, pretože molekuly týchto materiálov sú umiestnené medzi molekulami vody a znižujú napätie povrchný.
c) NESPRÁVNE. Elektroforéza je technika separácie molekúl podľa ich nábojov.
d) NESPRÁVNE. Viskozita je fyzikálna vlastnosť, ktorá určuje odolnosť kvapaliny proti prúdeniu.
e) NESPRÁVNE. Osmotický tlak je koligatívna vlastnosť, ktorá zodpovedá tlaku, ktorý musí byť vyvíjaný na systém, aby sa zabránilo spontánnemu výskytu osmózy.
Získajte viac informácií o problémoch uvedených v tomto vydaní:
- Vlastnosti hmoty
- Koligatívne vlastnosti
- Osmotický tlak
2. Povrchové napätie kvapalín priamo závisí od interakčných procesov medzi molekulami, ako je napríklad vodíková väzba. Ktorá z látok uvedených nižšie má najvyššie povrchové napätie?
a) benzén
b) oktán
c) etylalkohol
d) chlorid uhličitý
e) kyselina etánová
Správna alternatíva: e) kyselina etánová.
a) NESPRÁVNE. Benzén je uhľovodík, nepolárna molekula a nevytvára vodíkové väzby.
b) NESPRÁVNE. Oktán je uhľovodík, a preto je to nepolárna molekula, ktorá nevytvára vodíkové väzby.
c) NESPRÁVNE. Etylalkohol je mierne polárna zlúčenina, ktorá môže vytvárať vodíkové väzby, ale interakcia medzi molekulami je obmedzená.
d) NESPRÁVNE. Chlorid uhličitý je nepolárna organická zlúčenina, a preto nevytvára vodíkové väzby.
e) SPRÁVNE. Funkčná skupina karboxylovej kyseliny (-COOH) môže vytvárať vodíkové väzby buď s kyslíkom, alebo s hydroxylovým vodíkom.

Získajte viac informácií o problémoch uvedených v tomto vydaní:
- Polarita molekúl
- Organické funkcie
- Uhľovodíky
experiment povrchového napätia
Sledujte video nižšie s experimentom, ktorý demonštruje povrchové napätie vody.