Organické reakcie sú reakcie, ktoré prebiehajú medzi organickými zlúčeninami. Existuje niekoľko typov reakcií, ktoré nastávajú rozbitím molekúl a vznikom nových väzieb.
Z nich sa v širokej miere využívajú v priemysle a práve z nich sa dajú vyrábať okrem iných vecí aj lieky a kozmetické výrobky, plasty.
hlavný typy organických reakcií oni sú:
- adičná reakcia
- náhradná reakcia
- eliminačná reakcia
- Oxidačná reakcia
Adičná reakcia
Adičná reakcia prebieha, keď sa väzby organickej molekuly zlomia a pridá sa k nej činidlo.
Stáva sa to hlavne v zlúčeninách, ktorých reťazce sú otvorené a ktoré majú nenasýtenia, ako sú alkény () a alkíny (
).
Príklady adičných reakcií
Príklad 1: hydrogenácia (pridanie vodíka)
Hydrogenáciou alkénu sa získa alkán.
Príklad 2: halogenácia (pridanie halogénov)
Halogenáciou alkénu sa získa halogenid.
Príklad 3: hydratácia (pridanie vody)
Hydratáciou alkénu vzniká alkohol.
Prečítajte si tiež: Organické zlúčeniny
Náhradná reakcia
K substitučnej reakcii dochádza, keď existujú väzobné atómy (alebo skupina), ktoré sú nahradené inými.
Stáva sa to hlavne medzi alkánmi, cyklami a aromatickými látkami.
Príklady substitučných reakcií
Príklad 1: halogenácia (výmena halogénu)
Halogenáciou alkánu sa získa halogenid.
Príklad 2: nitrácia (substitúcia nitro)
Nitráciou alkánu sa získa nitrozlúčenina.
Príklad 3: sulfonácia (substitúcia sulfonikami)
Sulfonáciou alkánu vzniká kyselina.
Prečítajte si tiež: Organické funkcie
Eliminačná reakcia
K eliminačnej reakcii dochádza, keď sa z organickej molekuly odstráni uhlíkový ligand.
Táto reakcia je v rozpore s adičnou reakciou.
Príklady eliminačných reakcií
Príklad 1: eliminácia vodíka (dehydrogenácia)
Odstránením vodíka z alkánu sa získa alkén.
Príklad 2: eliminácia halogénov (dehalogenácia)
Elimináciou halogénov z dihalogenidu sa získa alkén.
Príklad 3: eliminácia halogenidov
Odstránením halogenidu z halogenidu sa získa alkén.
Príklad 4: vylučovanie vody (dehydratácia alkoholom)
Odstránením vody z alkoholu vzniká alkén.
Pozri tiež: Esterifikácia
Oxidačná reakcia
Oxidačná reakcia, nazývaná tiež redox, prebieha, keď dôjde k zisku alebo strate elektrónov.
Príklady oxidačných reakcií
Príklad 1: energetická oxidácia alkénov
Energetická oxidácia alkénu produkuje karboxylové kyseliny.
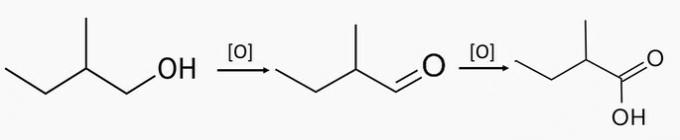
Príklad 2: oxidácia primárneho alkoholu
Energetická oxidácia primárneho alkoholu produkuje karboxylovú kyselinu a vodu.
Príklad 3: sekundárna oxidácia alkoholu
Oxidáciou sekundárneho alkoholu vzniká ketón a voda.
Prečítajte si tiež: Karboxylové kyseliny
Cvičenia z organických reakcií
Otázka 1
(Unifesp / 2002) Mnoho alkoholov sa dá získať kyselinou katalyzovanou hydratáciou alkénov.
V tejto adičnej reakcii sa H vo vode pridá k uhlíku, ktorý má na seba viazaných viac vodíkov a hydroxylová skupina je pripojená k menej hydrogenovanému uhlíku (Markovnikovovo pravidlo).
Ak vieme, že alkoholy vzniknuté pri hydratácii dvoch alkénov sú 2-metyl-2-pentanol a 1-etylcyklopentanol, aké sú názvy zodpovedajúcich alkénov, ktoré ich spôsobili?
a) 2-metyl-2-pentén a 2-etylcyklopentén.
b) 2-metyl-2-pentén a 1-etylcyklopentén.
c) 2-metyl-3-pentén a 1-etylcyklopentén.
d) 2-metyl-1-pentén a 2-etylcyklopentén.
e) 3-metyl-2-pentén a 2-etylcyklopentén.
Správna alternatíva: b) 2-metyl-2-pentén a 1-etylcyklopentén.
2-Metyl-2-pentanolový alkohol sa vyrába hydratáciou 2-metyl-2-penténalkénu.
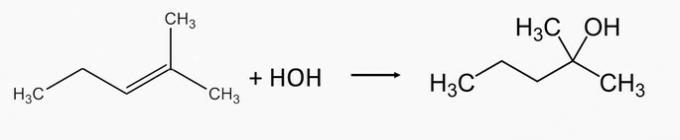
1-etylcyklopentanolový alkohol sa generuje hydratáciou 1-etylcyklopenténalkénu.
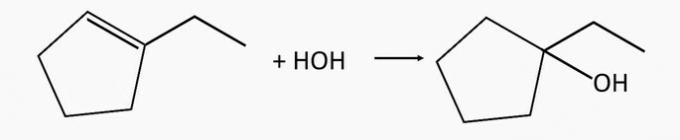
otázka 2
(Ufal / 2000) Pri štúdiu chémie uhlíkových zlúčenín sa zistilo, že BENZÉN:
() Je to uhľovodík.
() Možno získať z acetylénu.
() V oleji je to zložka s väčším hmotnostným podielom.
() Môže podstúpiť substitučnú reakciu.
() Je to príklad molekulárnej štruktúry, ktorá predstavuje rezonanciu.
(PRAVDA) Benzén je aromatický uhľovodík. Táto zlúčenina je tvorená iba atómami uhlíka a vodíka, ktorých vzorec je C6H6.
(SKUTOČNÉ) Benzén sa môže vyrábať z acetylénu nasledujúcou reakciou:
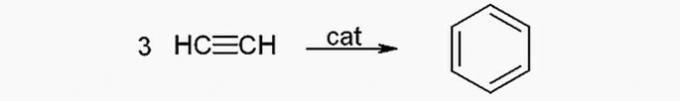
(FALSE) Ropa je zmes uhľovodíkov a hmotnosť zložiek závisí od veľkosti reťazca. Preto majú väčšie uhlíkové reťazce väčšiu hmotnosť. Ťažšie frakcie ropy, ako je asfalt, majú reťazce s viac ako 36 atómami uhlíka.
(PRAVDA) Substitučné reakcie, pri ktorých sa ako reakčné činidlo používa benzén, majú mnoho priemyselných aplikácií, hlavne na výrobu liečiv a rozpúšťadiel.
V tomto procese môže byť atóm vodíka nahradený halogénmi, nitroskupinou (-NO2), sulfónová skupina (—SO3H), okrem iných.
Pozrite si príklad tohto typu reakcie.
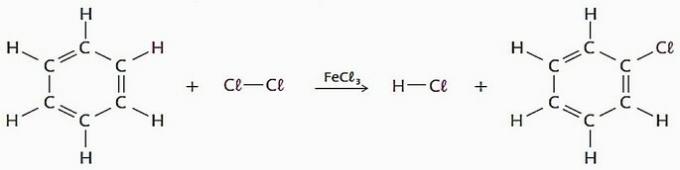
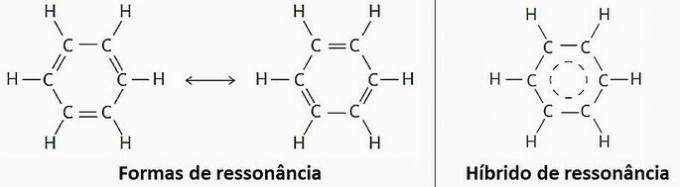
(PRAVDA) Z dôvodu rezonancie možno benzén predstavovať dvoma štruktúrnymi vzorcami.
V praxi sa však pozorovalo, že dĺžka a energia väzieb vytvorených medzi atómami uhlíka sú rovnaké. Preto je rezonančný hybrid najbližšie k skutočnej štruktúre.
otázka 3
(UFV / 2002) Oxidačná reakcia alkoholu s molekulárnym vzorcom C.5H12O, s KMnO4 poskytla zlúčenina molekulárneho vzorca C5H10O.
Začiarknite možnosť, ktorá zobrazuje SPRÁVNU koreláciu medzi názvom alkoholu a názvom vytvoreného produktu.
a) 3-metylbután-2-ol, 3-metylbutanal
b) pentán-3-ol, pentán-3-ón
c) pentán-1-ol, pentán-1-ón
d) pentán-2-ol, pentanal
e) 2-metylbután-1-ol, 2-metylbután-1-ón
Správna alternatíva: b) pentán-3-ol, pentán-3-ón.
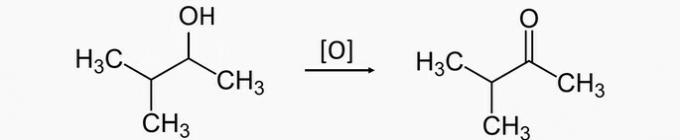
a) NESPRÁVNE. Oxidáciou sekundárneho alkoholu sa získa ketón. Správnym produktom na oxidáciu 3-metylbután-2-olu je preto 3-metylbután-2-ón.
b) SPRÁVNE. Oxidáciou sekundárneho alkoholu pentán-3-olu sa získa ketón pentán-3-ón.

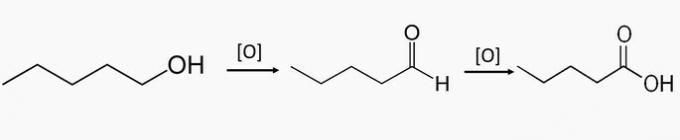
c) NESPRÁVNE. Tieto zlúčeniny sú súčasťou oxidácie primárnych alkoholov, pri ktorých sa vytvára aldehyd alebo karboxylová kyselina.
Pentan-1-ol je primárny alkohol a čiastočnou oxidáciou zlúčeniny môže vzniknúť pentanal a úplnou oxidáciou sa vytvorí kyselina pentánová.
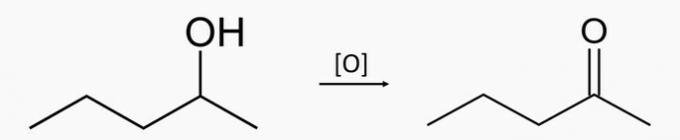
d) NESPRÁVNE. Oxidáciou sekundárneho alkoholu pentán-2-olu sa získa ketón pentán-2-ón.
e) NESPRÁVNE. Primárny alkohol 2-metylbután-1-ol produkuje aldehyd 2-metylbutanal v čiastočnej oxidácii a kyselinu 2-metylbutánovú v celkovej oxidácii.
otázka 4
(Mackenzie / 97) Pri eliminačnej reakcii, ktorá sa uskutočňuje v 2-brómbutáne s hydroxidom draselným v alkoholovom prostredí, sa získa zmes dvoch organických zlúčenín, ktoré sú pozičnými izomérmi.
Jedným z nich, ktorý sa tvorí v menšom množstve, je 1-butén. Druhou je:
a) metylpropén.
b) 1-butanol.
c) bután.
d) cyklobután.
e) 2-butén.
Správna alternatíva: e) 2-butén.
Alkény sa vyrábajú reakciou organického halogenidu HBr s hydroxidom draselným KOH v prítomnosti etylalkoholu ako rozpúšťadla.

Vďaka tomu, že atóm halogénu je uprostred uhlíkového reťazca, vznikli rôzne zlúčeniny, ktoré generovali viac ako jednu možnosť eliminácie.
Aj keď existujú dve možnosti výrobkov, nebudú mať rovnaké množstvo.
2-Butén pre túto reakciu bude tvorený vo väčšom množstve, pretože pochádza z eliminácie terciárneho uhlíka. 1-butén sa vytvoril elimináciou primárneho uhlíka, a preto sa vytvorilo menšie množstvo.

