Rovnováhatermálny je stav, v ktorom sa telo nachádza v to istéteplota než ich okolie. Pozorovalo sa, že všetky telá, ktoré majú vyššiu teplotu ako susedia, majú tendenciu spontánne im dodávať teplo, kým obidva nezačnú vykazovať rovnakú teplotu.
Pozritiež:Základy termológie
Tepelná rovnováha a nulový zákon termodynamiky
Tepelná rovnováha je ústredným pojmom za nulovým zákonom termodynamiky. Takýto zákon ustanovuje, že v prípade, že dva termodynamické systémy, THE a B, sú v tepelnej rovnováhe s tretím termodynamickým systémom, Çpotom THE a B budú tiež v tepelnej rovnováhe.
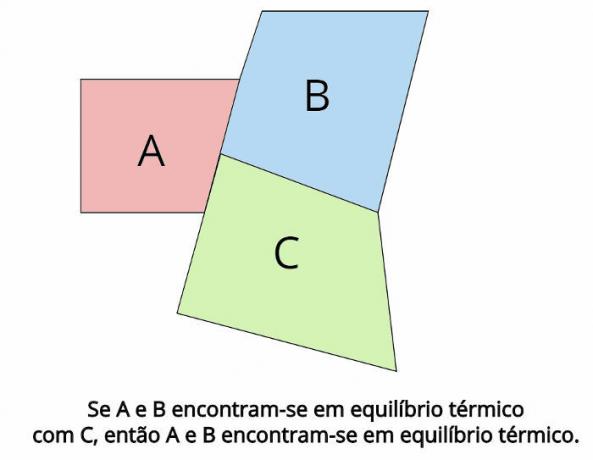
V tepelnej rovnováhe musia byť konečné teploty každého telesa rovnaké: TTHE = TB = TÇ
Zistite, čo ustanovuje nulový zákon termodynamiky:
“Ak sú dve telesá v tepelnej rovnováhe s tretím telesom, potom budú tieto telesá navzájom v tepelnej rovnováhe. “
Iný spôsob chápania tepelnej rovnováhy je založený na vnútornej energii telies. Vnútorná energia alebo jednoducho tepelná energia je fyzikálna veličina priamoproporcionálny à teplota
tela. Preto, ak existujú telá s rôznymi teplotami v rovnakom termodynamickom systéme, budú mať rôzne moduly vnútorná energia, a preto bude medzi nimi prenášať časť tejto energie, kým medzi ich energiami nebude žiadny rozdiel. interné. Chcete vedieť viac o tom, čo je to vnútorná energia a aké má vlastnosti? Prístup k článku: Vnútorná energia.Teraz neprestávajte... Po reklame je toho viac;)
tepelná a tepelná rovnováha
K prenosu tepla dochádza vždy spontánne, z tela s najvyššou teplotou do tela s najnižšou teplotou. K tomuto prenosu energie vo forme tepla môže dochádzať prostredníctvom procesov ako napr šoférovanie, konvekcia a žiarenie.
Vedenie vozidla: Jedná sa o prenos tepla medzi telesami, ktorý sa vyskytuje najmä v pevných látkach. Pri tomto type vedenia nedochádza k hromadným prenosom. Tento typ prenosu tepla vysvetľuje, ako napríklad v kovoch dochádza k tepelnej rovnováhe.
Konvekcia: Jedná sa o prenos tepla, ktorý prebieha v tekutinách. V tomto režime prenosu tepla dochádza k prenosu hmoty, keď sa ohriata tekutina pohybuje, pričom vytvára konvekčné prúdy, kým všetka tekutina nedosiahne tepelnú rovnováhu.
Žiarenie: Je to prenos tepla elektromagnetickými vlnami, takže k tomuto procesu dochádza, aj keď medzi telom a iným telom pri rôznych teplotách nie je žiadne fyzické médium. Teplo, ktoré sa prenáša, je v tomto prípade ekvivalentom elektromagnetických vĺn s menšou energiou ako viditeľné svetlo, teda tepelné žiarenie, ktoré sa nachádza v oblasti infračervená.
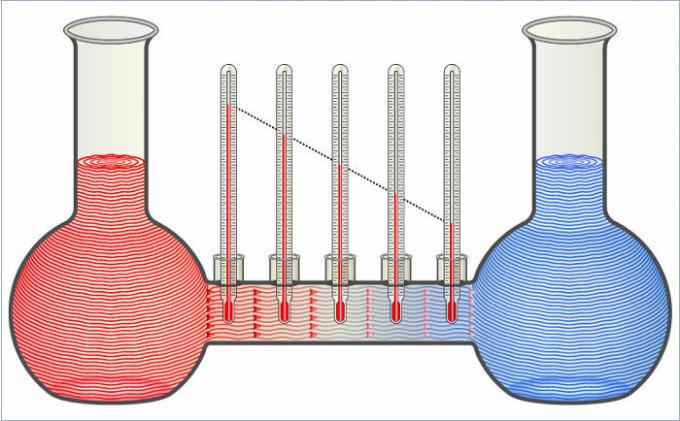
Dve kvapaliny na obrázku prenášajú navzájom teplo, kým sa ich teploty nevyrovnajú.
Chcete vedieť viac o tom, ako prebieha každý z procesov prenosu tepla? Prístup k článku: Procesy šírenia tepla.
citeľné teplo
keď je rozdielvteplota medzi dvoma telami alebo medzi telom a jeho okolím dôjde k spontánnej výmene tepla medzi nimi, takže telo s vyššou teplotou ochladzuje a telesá s nižšou teplotou sa zahrievajú, kým nedosiahnu teplotu v rovnováhatermálny.
Nazýva sa množstvo tepla, ktoré sa vymieňa medzi telesami pri rôznych teplotách citeľné teplo a túto sumu je možné vypočítať zo vzorca uvedeného na obrázku nižšie:
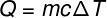
Q - teplo (vápno alebo J)
m - hmotnosť (g alebo kg)
ç - špecifické teplo (kal / g ° C alebo J / kg. K)
ΔT - kolísanie teploty (° C alebo K)
Vo vyššie uvedenom vzorci je dôležité zdôrazniť veľkosť mena špecifické teplo. takáto veľkosť meria množstvo energie na hmotnosť, ktoré látka potrebuje na získanie alebo absorpciu, aby sa jej teplota zmenila o 1 ° C. Napríklad v prípade čistej vody a za normálnych tlakových podmienok je na zmenu jej teploty o 1 ° C potrebných 1,0 kalórie na každý gram vody.
Všetky látky, ktoré navzájom nadviazali tepelný kontakt, majú teda tendenciu dosiahnuť stav rovnováhatermálny v priebehu času však spontánne niektorí potrebujú na to väčšie množstvo energie a to priamo ovplyvňuje teplotu na dosiahnutie tepelnej rovnováhy.
čítaťtiež:Čo je to teplota?
latentné teplo
Je možné, že počas tepelných výmen s okolím telo predstavuje tlak, teplotu a objem, ktoré spôsobujú, že prechádza zmenami vo svojom fyzickom stave. Tieto zmeny sa vyskytujú v teplotakonštantný (pre telesá zložené z jednej látky bez nečistôt), to znamená, že napriek prijímaniu alebo poskytovaniu tepla do vonkajšieho prostredia sa teplota týchto telies nemení.
To je možné len preto, že všetka vymenená energia sa v tomto prípade používa na zmenu konformácie vašich molekúl. Od okamihu, keď je energetická bariéra „prekonaná“ a všetok obsah tela je v inom fyzickom stave, tj Telo pokračuje vo výmene tepla so svojím okolím, pokiaľ sa jeho teplota samozrejme nerovná teplote vonku.
O latentné teplo sa dá vypočítať zo vzorca zobrazeného na obrázku nižšie, skontrolujte to:
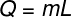
Q - latentné teplo (vápno alebo J)
m - hmotnosť (g alebo kg)
Ľ - špecifické latentné teplo (kal / g alebo J / kg)
Vzorec tepelnej rovnováhy
V prípade, že chceme zistiť, čo je to teplotavrovnováha niektorého termodynamického systému je potrebné, aby sme daný systém považovali za a systémizolovaný, to znamená, že musíme predpokladať, že so susednými časťami tohto systému sa nevymieňa žiadne množstvo tepla.
Z tejto podmienky môžeme povedať, že celé množstvo vymeneného tepla sa vymieňa iba medzi orgánmi, ktoré tvoria tento systém, bez ohľadu na tepelné straty napríklad na steny nádoby. V takom prípade hovoríme, že kontajner má tepelná kapacita zanedbateľné, tj. neabsorbuje žiadne teplo.
Predstavte si nasledujúcu situáciu: do šálky horúceho čaju so zanedbateľnou tepelnou kapacitou nalejte nejaké kocky ľadu. Aby sme mohli určiť tepelnú rovnovážnu teplotu, musíme okrem znalosti počiatočných podmienok systému urobiť niekoľko úvah:
Celé množstvo tepla, ktoré horúci čaj dáva ľadu, bude ním úplne absorbované, pretože šálka má zanedbateľnú tepelnú kapacitu.
Musíme ignorovať tepelné straty vzduchu a iného okolia, aby sme túto šálku čaju mohli chápať ako uzavretý termodynamický systém.
Týmto spôsobom môžeme zistiť, že celé množstvo tepla prijatého ľadom sa vzdal horúci čaj. Týmto sme napísali náš vzorec na výpočet tepelnej rovnováhy:
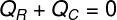
QR - Prijaté teplo
QÇ - teplo uvedené v
Teplo uvedené v (QÇ) sa vzťahuje na množstvo tepla, ktoré horúci čaj preniesol na kocky ľadu, ktoré sú doň vložené. Už bolo prijaté teplo (QR) je množstvo tepla, ktoré tieto kocky ľadu prijali. Toto množstvo tepla bude mať dve povahy: teplo citlivý a horúce latentný, pretože pri vstupe do tepelnej rovnováhy sa pravdepodobne kocky ľadu roztavia.
Stanovenie tepelnej rovnovážnej teploty
Určme teplotu tepelnej rovnováhy z nasledujúcej situácie:
Do šálky so zanedbateľnou tepelnou kapacitou, ktorá obsahuje 200 ml (200 g) čaju pri počiatočnej teplote 70 ° C, sa dá 10 g ľadu pri teplote -10 ° C. Určte tepelnú rovnovážnu teplotu systému (predpokladajte, že merné teplo čaju sa rovná mernému teplu vody):
Údaje:
çVODA = 1,0 kal / g ° C
çICE = 0,5 kal / g ° C
ĽICE = 80 kcal / g
Najprv si myslíme, že všetko teplo prijaté ľadom bolo rozdané čajom:

Ďalej je potrebné podrobne uviesť, ktoré formy tepla boli dané a prijaté:
Čaj: Čaj dodával iba citeľné teplo (Qs), pretože jeho fyzický stav sa nezmenil.
Ľad: Ľad mal pôvodne teplotu -10 ° C, takže prijímal citeľné teplo (Qs) až do teploty 0 ° C, potom prijalo latentné teplo (QĽ) skvapalniť. Potom, čo sa stal tekutým, prijal latentné teplo (Qs), kým sa nedostane do tepelnej rovnováhy (TF) s čajom.
Ak preložíme to, čo sme analyzovali vyššie, vo forme rovnice, budeme musieť vyriešiť nasledujúci výpočet:
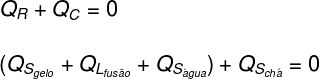
Ak nahradíme údaje poskytnuté cvičením vo vyššie uvedenej rovnici, budeme musieť vyriešiť nasledujúci výpočet:
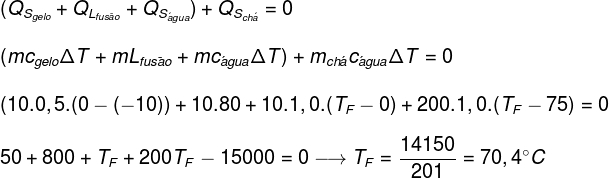
Podľa vyššie uvedeného výpočtu by rovnovážna teplota systému čaj + ľad mala byť približne 70,4 ° C.
Experiment s tepelnou rovnováhou
Na otestovanie tepelnej rovnováhy medzi dvoma telesami môžeme vykonať niekoľko experimentov. Najjednoduchšie z nich však zahŕňa použitie a kalorimeter to je a teplomer. Kalorimeter je adiabatická nádoba (ktorá neumožňuje prechod tepla) s tepelnou kapacitou ozanedbateľný, ako napríklad hrniec s polystyrénom, ktorý je dobrým tepelným izolátorom.

Kalorimeter sa používa na meranie kolísania teploty systému vo vnútri.
Tepelná rovnováha a život na Zemi
O rovnováhatermálny hrá zásadnú úlohu v pozemskom živote. Bez prítomnosti skleníkových plynov v zemskej atmosfére je väčšina tepelné žiarenie planéta by ju opustila a šírila by sa do vesmíru. To by časom spôsobilo obrovské ochladenie na celej planéte, čo by spôsobilo, že oceány časom zamrzli.
Oceány navyše zohrávajú kľúčovú úlohu v rovnováhatermálny planéty. Z dôvodu svojej veľkej cestoviny a teplokonkrétne, oceány sú obdarené obrovským kapacitatermálne, to znamená, že na zmenu teploty musia prijímať obrovské množstvo tepla. Z tohto dôvodu sú schopní veľmi efektívne regulovať teplotu planéty. Regióny ďaleko od oceánov a s malým množstvom vody bývajú veľké teplotné rozsahy, ako v prípade púští, ktoré sú cez deň mimoriadne horúce a v noci mrznú.
Preto rovnováhatermálny je to proces zásadného významu pre udržanie fyzikálnych, chemických a biologických procesov na planéte, a preto je nevyhnutný pre existenciu života na Zemi.
Podľa mňa.Rafael Helerbrock