Môže sa stať, že existujú kyseliny toho istého prvku a tento prvok má rovnaké oxidačné číslo (NOX), rozdiel je však v stupňoch hydratácie.
Napríklad nižšie máme tri kyseliny tvorené prvkom fosfor (P):
H3PRACH4 H4P2O7 HPO3
Všimnite si, že vo všetkých troch kyselinách je oxidačné číslo fosforu +5; rozdiel je v stupni hydratácie.
Na základe toho sa tieto kyseliny rozlišujú v nomenklatúre pomocou predpôn orto, pyro a meta.
Najviac hydratovaná kyselina sa nazýva orto. V uvedenom príklade prvý (H3PRACH4) sa volá kyselina ortofosforečný, pretože je najviac hydratovaný z týchto troch. Orto predpona je spotrebná, takže väčšinu času sa táto kyselina bude iba volať kyselina fosforečná.
Predpony pyro a meta sa používajú s kyselinou orto ako referenčným bodom:
Teraz neprestávajte... Po reklame je toho viac;)
- Pyrus: 2 molekuly orto mínus 1 molekula H2O
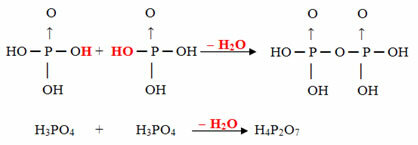
Príklad: H4P2O7 sa volá kyselina pirofosforečný pretože sa rovná dvom molekulám kyseliny ortofosforečnej (H3PRACH4) mínus jedna molekula vody.
2. H3PRACH4 = H6P2O8
H6P2O8 - H2O = H4P2O7
Tento proces je a intermolekulárna dehydratácia:
- Cieľ: 1 molekula orto mínus 1 molekula H2O
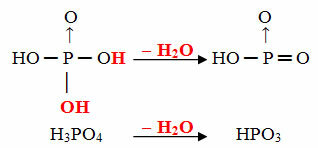
Príklad: HPO3 sa volá kyselina cieľfosforečný pretože sa rovná molekule kyseliny ortofosforečnej (H3PRACH4) mínus jedna molekula vody.
H3PRACH4 - H2O = HPO3
Tento proces je a intramolekulárna dehydratácia:
Autor: Jennifer Fogaça
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. „Stupeň hydratácie kyselín“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/grau-hidratacao-dos-acidos.htm. Prístup k 28. júnu 2021.
Kyselina ortofosforečná má nasledujúci molekulový vzorec: H3PRACH4. Odtiaľ označte alternatívu, ktorá označuje kyselinu pyrofosforečnú, respektíve kyselinu metafosforečnú:
Stupeň ionizácie, kyselina chlorovodíková, prchavosť, kyselina octová, Svante Arrehenius, kyseliny vedú elektrinu, neutralizačné reakcie, reakcia s uhličitanmi a hydrogenuhličitanmi, červený roztok fenolftaleínu, lakmusový papierik Modrá.
