Katalyzátor účinkuje v zásade na urýchlenie vývoja určitej reakcie. Je to možné, pretože katalyzátor mení mechanizmus, ktorým reakcia prebieha, čo vedie k „alternatívnej ceste“, ktorá vyžaduje menej aktivačnej energie na to, aby sa reakcia mohla spustiť a dostať sa k aktivovanému komplexu.
Existuje niekoľko druhov katalýzy, z ktorých jeden je heterogénna katalýza, ktoré možno definovať ako to, čo nastane, keď má systém viac ako jednu fázu, to znamená, že reaktanty a produkty sú vo fyzikálnom stave odlišnom od fyzikálneho stavu katalyzátora.
Ako príklad môžeme uviesť medzistupeň tvorby kyseliny sírovej (H2IBA4 (aq)). Tento krok spočíva v tvorbe oxidu siričitého (SO3 (g)) spaľovacou reakciou oxidu siričitého (SO2 písm. G)):
2 SO2 písm. G) + O.2 písm. G) → 2 OS3 (g)
Pretože táto reakcia prebieha tak pomaly, na jej urýchlenie sa použije katalyzátor. Katalyzátorom, ktorý je možné v tomto prípade použiť, je oxid diváničitý (V2O5 (S)), ktorý je tuhý. Pretože reaktanty a reakčný produkt sú plynné, budeme mať heterogénny systém.
Ako však môže oxid diváničitý urýchliť reakciu?
Čo sa stane, je to, že molekuly kyslíkového činidla sú adsorbované, to znamená, že sú zadržané na povrchu oxidu divanáditého. To spôsobuje, že väzby molekúl tohto plynu časom slabnú, čo uľahčuje tvorbu komplexu aktivovaná a následne znižuje aktivačnú energiu reakcie a zvyšuje jej rýchlosť vývoja, to znamená jej rýchlosť.
Teraz neprestávajte... Po reklame je toho viac;)
Ako sa to deje, uvidíte na nasledujúcom diagrame:
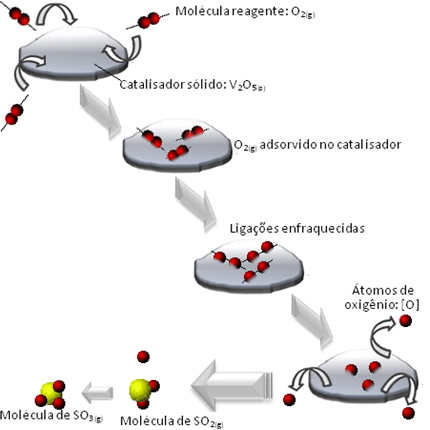
Ďalšie príklady heterogénnej katalýzy sú uvedené nižšie. Upozorňujeme, že v obidvoch prípadoch sú reaktanty a produkty v plynnom, vodnom alebo kvapalnom stave, zatiaľ čo katalyzátory sú v tuhom stave:
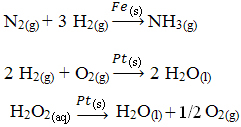
Príkladom heterogénnej katalýzy, ktorá sa vyskytuje v našom každodennom živote, je konvertor auto katalytické, známejšie ako katalyzátory. Tieto zariadenia proti znečisťovaniu sú potiahnuté látkami, ktoré pôsobia ako katalyzátory zvyčajne zliatina paládia a ródia (pre benzínové motory) a paládia a molybdénu (pre benzínové motory). alkohol).
V tomto katalyzátore prebiehajú chemické reakcie, pri ktorých sa plyny z nedokonalého spaľovania, ktoré sú škodlivejšie pre človeka, premieňajú na netoxické plyny. Reaktanty a produkty sú všetko plyny, zatiaľ čo katalyzátory sú pevné látky.
Ak chcete získať viac informácií o operačnom systéme tohto zariadenia, prečítajte si text: "Katalyzátor”.
Autor: Jennifer Fogaça
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. „Heterogénna katalýza“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/catalise-heterogenea.htm. Sprístupnené 27. júna 2021.


