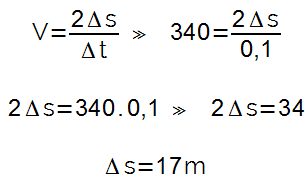THE Elektrochémia je odbor fyzikálnej chémie, ktorý študuje reakcie, pri ktorých dochádza k prenosu elektrónov (oxi-redukčné reakcie) a k nim premena na elektrickú energiu, ako aj opačný proces, to znamená premena elektrickej energie na energiu chémia.
Prvý proces je to, čo sa deje v Batérie. Batérie sú zariadenia tvorené dvoma elektródami (kladným pólom, ktorým je katóda, a záporným pólom, ktorým je anóda), navyše s elektrolytom (vodivý roztok). Elektróny sú prenášané vonkajším vodičom z anódy na katódu a vytvárajú elektrický prúd, ktorý sa používa na zapnutie niektorého zariadenia. Batérie pozostávajú z niekoľkých článkov zapojených do série alebo paralelne.
Toto je spontánny proces a energia sa dodáva až do vyčerpania chemickej reakcie (ako je to v prípade primárnych článkov a batérií, napríklad suchého článku Leclanché a batérie alkalické), alebo v prípade reverzibilných reakcií možno použiť potenciálny rozdiel a reakciu zvrátiť, čím sa reaktanty znova vytvoria a batéria sa dobije je pripravený na ďalšie použitie (to je prípad batérií a sekundárnych batérií, ako sú olovo, ktoré sa používajú v automobiloch, a lítium-ión, ktoré sa používajú v prístrojoch mobilné telefóny).

Primárne články a batérie v popredí a druhé dobíjanie sekundárnych batérií (olovené a lítium-iónové)
Teraz neprestávajte... Po reklame je toho viac;)
Opačný proces nie je spontánny a je vyvolaný elektrolýza. Elektrolýza je prechod elektrického prúdu prichádzajúceho z generátora, ako je napríklad článok alebo batéria, cez iónovú kvapalinu. Ak je kvapalinou nejaká roztavená látka, máme a magmatická elektrolýza, ale ak ide o vodný roztok, máme a vodná elektrolýza.
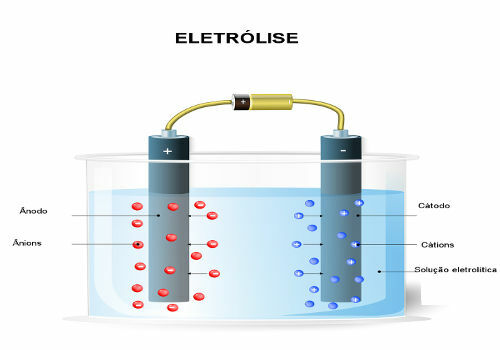
Pri prechode elektrického prúdu cez kvapalné médium generátor „ťahá“ elektróny z kladného pólu (anóda - je to opak oproti batéria) elektrolytického článku a prenáša ich na záporný pól (katódu), to znamená, že katóda prechádza redukciou a anóda oxidácia. Elektrická energia dodávaná generátorom sa teda transformuje na redoxné reakcie (chemická energia). Nižšie je uvedená schéma elektrolýzy vody:
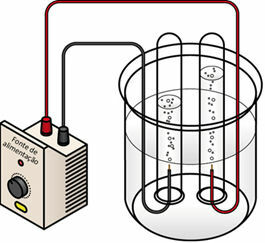
Schéma elektrolýzy vody
Elektrolýza sa široko priemyselne používa pri výrobe dôležitých látok, ako je hliník, plynný chlór, kovový sodík, a na čistenie alebo ochranu rôznych kovov, ako pri galvanickom pokovovaní alebo procesoch galvanického pokovovania, ktoré spočívajú v potiahnutí nejakého predmetu kovom, ako je postriebrenie, pokovovanie meďou, pokovovanie niklom, pozlátenie chromátovanie; keď je oceľ potiahnutá zinkom, nazýva sa to galvanizácia.
V časti Elektrochémia na našom webe nájdete viac podrobností o všetkých aspektoch týkajúcich sa článkov a batérií, ako aj elektrolýzy.
Autor: Jennifer Fogaça
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. „Čo je to elektrochémia?“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-eletroquimica.htm. Sprístupnené 27. júna 2021.
Chémia
Elektrolýza, roztoky elektrolytov, elektrický prúd, oxidačno-redukčné reakcie, spontánny chemický proces, chemický proces spontánne, transformátor, umelá transformácia, priemyselné odvetvia, alkalické kovy, kovy alkalických zemín, plynný vodík, plyn kl