O teplo je to tepelná energia, ktorá prechádza z tela s vyššou teplotou do iného s nižšou teplotou. Ak nie je rozdiel v teplote medzi dvoma telesami, nie je ani teplo.
Obrázok vyššie zobrazuje prechod tepla z telesa s teplotou T do iného telesa s nižšou teplotou zodpovedajúcou T '. Keď sa telesné teploty vyrovnajú, hovoríme, že tepelná bilancia bolo dosiahnuté a v tom okamihu, pretože nebude teplotný rozdiel, teplo prestane prúdiť.
Tu je niekoľko dôležitých bodov týkajúcich sa tepla:
1) KALORICKÉ: Až do začiatku 19. storočia sa verilo, že teplo súvisí s prítomnosťou tzv. Neviditeľnej a beztiažovej tekutiny kalorický. Čím vyššia je teplota tela, tým väčšie je množstvo tejto látky v jeho vnútri. Na základe pozorovaní Benjamina Thompsona, známeho ako Earl of Rumford (1753-1814), boli vykonané experimenty, ktoré mali dokázať, že teplo je energia. Experiment s najväčším významom v tomto dôkaze patrí Prescottovi Jouleovi (1818-1889).
Myšlienková mapa: Teplo
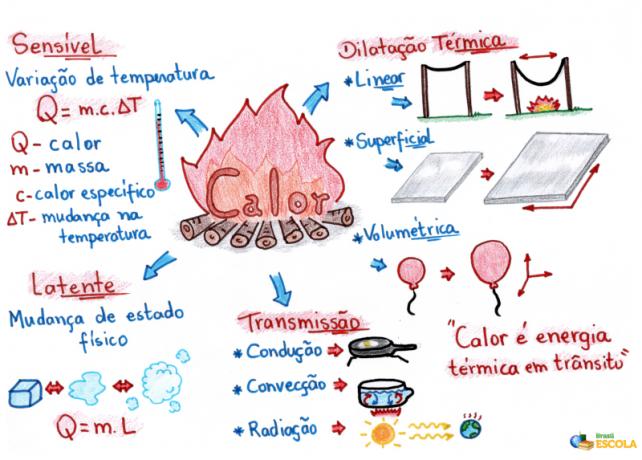
* Ak si chcete stiahnuť myšlienkovú mapu v PDF, Kliknite tu!
2) Merná jednotka: Podľa Medzinárodný systém jednotiek (SI), jednotka merania tepla je joule, ale jednotka kalórií (kal) sa často používa.
1 kal = 4,18 J
Kalória je množstvo tepla potrebné na zvýšenie teploty 1 g vody o 1 ° C.
3) Zdroje tepla:Zdrojom tepla je akýkoľvek prvok schopný vyvolať zvýšenie teploty v inom tele. Ako príklad môžeme uviesť plameň kachlí, pecí, krbov a pod.
4) Prenos tepla: Existujú tri možné spôsoby prestup tepla:
- Šoférovanie: Keď teplo prechádza z molekuly na molekulu materiálu;
- Konvekcia: Prenos tepla v tekutine, ku ktorému dochádza v dôsledku hromadného posunu samotnej tekutiny;
-
Žiarenie: Prevod tepla elektromagnetickými vlnami.
5) Druhy tepla: Keď dodáte množstvo tepla, ktoré je schopné iba generovať teplotné zmeny v tele, toto množstvo energie sa nazýva citeľné teplo. Keď množstvo preneseného tepla spôsobí zmenu fyzikálneho stavu, dôjde k jeho vzniku latentné teplo.
Joab Silas
Vyštudoval fyziku
* Moja mentálna mapa. Rafael Helerbrock
Zdroj: Brazílska škola - https://brasilescola.uol.com.br/o-que-e/fisica/o-que-e-calor.htm

