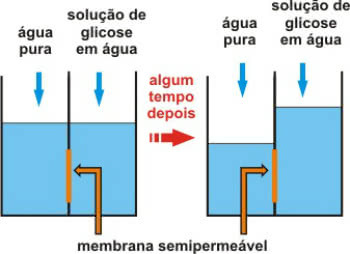
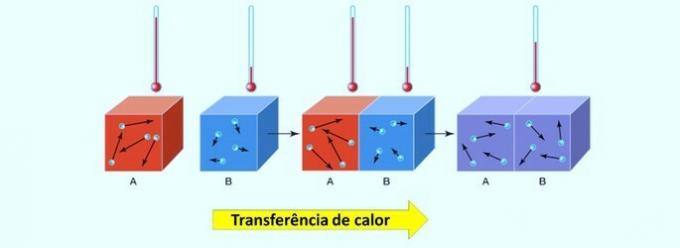
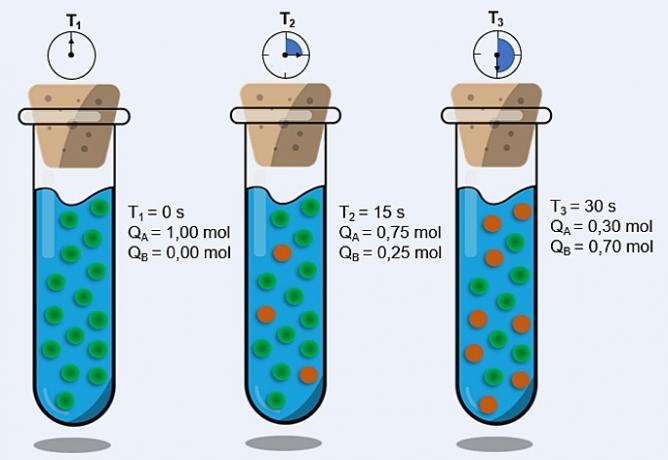
Vedec Friedrich Kohlrausch (1840-1910) ako prvý navrhol, že čistá voda vedie elektrinu, aj keď v malom rozsahu. Je to tak preto, lebo voda sa chová amfotérne; to znamená, že pri určitých príležitostiach pôsobí ako kyselina a daruje protóny (H.+); a v iných sa správa ako základňa a prijíma protóny.
To znamená, že voda vykonáva svoju vlastnú ionizáciu podľa chemickej rovnice uvedenej nižšie:
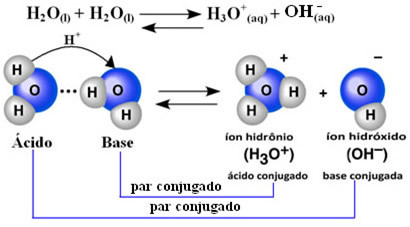
Tento proces sa nazýva autoionizácia vody a vyskytuje sa vo veľmi malom rozsahu, to znamená, že voda je veľmi slabý elektrolyt s nízkymi hodnotami stupňa ionizácie a ionizačnej konštanty v rovnovážnom stave (Kç). Presne preto má voda takú nízku vodivosť.
Pre predstavu, pri teplote okolia 25 ° C je možné určiť, že koncentrácie hydroxidových a hydróniových iónov produkovaných pri samoionizácii čistej vody sú rovné 1. 10-7 mol. Ľ-1. To znamená, že z miliardy molekúl vody sa ionizujú iba dve.
Konštanta iónovej rovnováhy vody sa nazýva çdisociačná konštanta vody,konštanta autoprotolýzyalebo iónový produkt vody.Túto konštantu predstavuje Kw, pretože w odkazuje na slovo voda, čo v angličtine znamená voda.
Teraz neprestávajte... Po reklame je toho viac;)
Jeho výpočet sa vykonáva rovnakým spôsobom ako ostatné rovnovážné konštanty, pričom treba pamätať na to, že ako je uvedené v texte „Konštanty Balance Kc a Kp “, v tomto prípade sa vo výraze objavia iba produkty, pretože voda v tekutom stave má rovnakú aktivitu do 1. Čisté kvapalné alebo tuhé látky sa nevkladajú do disociačného konštantného výrazu, pretože sa nemenia. Umiestnia sa iba vodné a plynné roztoky. Takže máme:
Kw = [H3O+]. [oh-]
Kw = (1. 10-7). (1. 10-7)
Kw = 10-14
Rovnako ako u ostatných rovnovážnych konštánt, Okw mení sa len so zmenou teploty. So zvyšovaním teploty vody sa zvyšuje aj jej ionizácia, čo znamená, že samoionizácia vody je endotermický proces, to znamená, že absorbuje teplo.
Je to vidieť na hodnotách iónového produktu vody (K.w) uvedené v nasledujúcej tabuľke pri rôznych teplotách:
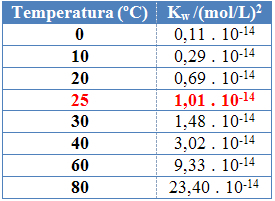
Iónový produkt vody bude mať vždy pevnú hodnotu pri každej teplote, či už v čistej vode alebo v roztoku. Aj keď má roztok koncentrácie iónov H3O+ a oh- rôzne, produkt medzi nimi zostane konštantný.
Autor: Jennifer Fogaça
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. „Iónový vodný produkt (Kw)“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/produto-ionico-Agua-kw.htm. Prístup k 28. júnu 2021.