Plyn a para
Rozdiel medzi plynom a parou je daný kritickou teplotou. Para je hmota v plynnom stave, ktorá sa dá skvapalniť pri zvyšujúcom sa tlaku. Plyn nie je to isté. Je to tekutina, ktorá sa nedá skvapalniť jednoduchým zvýšením tlaku. Tým sa plyn líši od pary.
Správanie plynov
Daná látka v plynnom stave je plyn, ak je jeho teplota vyššia ako kritická teplota, ak je rovnaká alebo nižšia ako kritická teplota, pri ktorej je látkou para.
Skutočné plyny, ktoré bežne poznáme, ako napríklad hélium, dusík a kyslík, majú rozdielne a konkrétne molekulárne charakteristiky. Ak ich však všetky vystavíme vysokým teplotám a nízkym tlakom, začnú sa prejavovať veľmi podobne. Pri štúdiu plynov sa prijíma jednoduchý teoretický model, ktorý v praxi neexistuje, s chovaním podobným chovaniu skutočných plynov. Táto aproximácia je lepšia, čím nižší je tlak a tým vyššia je teplota. Tento plynový model sa nazýva perfektný plyn.
Okolo 17. a 19. storočia traja vedci (Jacques Charles, Louis J. Gay-Lussac a Paul E. Clayperon) po štúdiu správania plynov vypracoval zákony upravujúce správanie dokonalých plynov, ktoré sa tiež nazývajú ideálne plyny. Nimi stanovené zákony ustanovujú pravidlá „vonkajšieho“ správania dokonalého plynu, ktoré vedie k počíta iba fyzikálne veličiny, ktoré sú s nimi spojené, a to: objem, teplota a tlak.
Všeobecný zákon dokonalých plynov
Výraz, ktorý určuje všeobecný zákon pre dokonalé plyny, možno vidieť nasledovne:
Teraz neprestávajte... Po reklame je toho viac;)
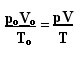
kde pO, VO a TO sú počiatočný tlak, počiatočný objem a počiatočná teplota. Toto je výraz, ktorý sa používa, keď sa premenné plynu líšia.
Boyleov zákon
Robert Boyle, fyzik a chemik, bol ten, kto určil zákon, ktorý riadi transformácie, ktorými plyn prechádza, keď je jeho teplota udržiavaná na konštantnej hodnote. Jeho zákon hovorí, že keď plyn prechádza izotermickou premenou, je jeho tlak nepriamo úmerný jeho obsadenému objemu. Z tohto zákona získame toto ako TO = T Musíme:
POV.O = pV
Karolov zákon
Charlesov zákon je zákon, ktorý riadi premeny dokonalého plynu na konštantný objem. Tieto transformácie sa nazývajú izochorické alebo izometrické transformácie. Podľa tohto zákona, keď ideálna plynová hmota prechádza izochorickou premenou, je jej tlak priamo úmerný jej absolútnej teplote. Matematicky možno tento zákon vyjadriť nasledovne:

kde pO a TO sú počiatočný tlak a počiatočná teplota.
Zákon Gay-Lussac
Zákon Gay-Lussac je zákon, ktorý riadi premeny dokonalého plynu pri konštantnom tlaku. Tento zákon, napriek tomu, že nesie meno Gay-Lussac, už objavil fyzik a chemik A.C. Charles. Podľa zákona, keď plyn prechádza izobarickou premenou, je objem plynu priamo úmerný jeho absolútnej teplote. Matematicky možno tento zákon vyjadriť nasledovne:

Kde VO a TO zodpovedajú počiatočnému objemu a počiatočnej teplote.
Autor: Marco Aurélio da Silva
Pozrieť viac!!
Transformácie plynu
Vedzte, čo sú transformácie plynov.
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
SANTOS, Marco Aurélio da Silva. „Štúdium plynov“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/fisica/estudo-dos-gases.htm. Sprístupnené 27. júna 2021.
