osmoskopia je spoločné vlastníctvo (ostatní sú tonoskopia, ebullioskopia a kryoskopia), ktorý skúma výskyt osmóza medzi dvoma roztokmi rôznych koncentrácií, z ktorých jeden je koncentrovanejší ako druhý.
Poznámka: Ak sa do rozpúšťadla pridá neprchavá rozpustená látka, dôjde ku koligatívnym vlastnostiam.
Ako napr osmoskopia študovať osmózu, je nevyhnutné vedieť Čo je tento jav. K tomu použijeme nižšie uvedené riešenia, ktoré sú oddelené polopriepustnou membránou:
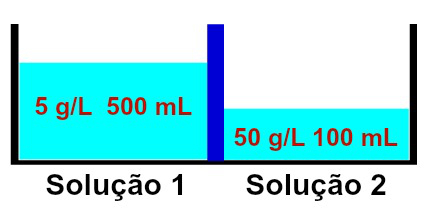
Reprezentácia roztokov, ktoré majú rôzne koncentrácie
Pozorovalo sa, že roztok 1 obsahuje koncentráciu 5 g / l a objem 500 ml, zatiaľ čo roztok 2 má koncentráciu 50 g / l a objem 100 ml, oddelený membránou polopriepustný. Roztok 2 je koncentrovanejší ako roztok 1, a preto medzi nimi musí dôjsť k osmóze.
Osmóza sa musí nevyhnutne vyskytnúť od roztoku 1 po roztok 2, pretože roztok 1 je menej koncentrovaný. Počas tohto výskytu časť rozpúšťadla prechádza semipermeabilnou membránou, čím sa vytvorí objem roztoku 2 narastá a objem roztoku 1 klesá, až kým obidva roztoky nezačnú mať rovnakú koncentráciu, tj. izotonia.

Úprava výšky roztokov 1 a 2 v dôsledku výskytu osmózy
Poznámka: Izotonické médiá sú médiá, ktorých koncentrácia je rovnaká.
Podľa osmoskopia, dochádza k osmóze, pretože maximálny tlak pár rozpúšťadla v menej koncentrovanom roztoku je vyšší ako tlak rozpúšťadla v koncentrovanejšom roztoku. Teraz, ak chceme zabrániť výskytu osmózy, stačí vyvinúť tlak na najkoncentrovanejšie riešenie:
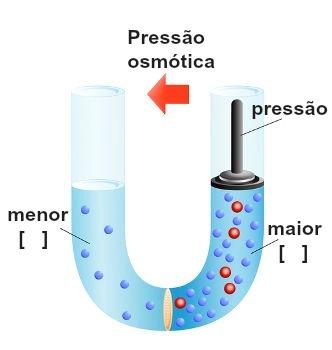
Reprezentácia vykonania tlaku na najkoncentrovanejšie riešenie
Tento tlak, ktorý je vyvíjaný na najkoncentrovanejší roztok na blokovanie alebo dokonca reverznú osmózu, sa nazýva osmotický tlak a je reprezentovaná symbolom π. Malo by to byť priamo úmerné koncentrácii roztoku.
Možné interpretácie osmotického tlaku
Podľa záverov osmoskopia, každé riešenie má osmotický tlak, pretože to súvisí s koncentráciou, charakteristikou prítomnou v každom roztoku.
Teraz neprestávajte... Po reklame je toho viac;)
Pri porovnaní jedného média alebo jedného riešenia s druhým môžeme použiť nasledujúce výrazy:
Hypertonické: keď jedno médium predstavuje osmotický tlak väčší ako druhé;
hypotonický: keď má jedno médium osmotický tlak nižší ako druhé;
Izotonický: keď majú dve médiá alebo riešenia rovnaký osmotický tlak.
Teda pri porovnaní osmotických tlakov dvoch roztokov A a B, predstavovaných πTHE a πB, môžeme povedať, že:
Ak sú osmotický tlak A a B rovnaké, prostriedky alebo riešenia budú izotonické:
πTHE = πB
Ak je osmotický tlak A väčší ako osmotický tlak B, bude médium A vo vzťahu k B hypertonické:
πTHE> πB
Ak je osmotický tlak B nižší ako osmotický tlak A, bude médium B vo vzťahu k B hypotonické:
πB< πTHE
Vzorec na výpočet osmotického tlaku
π = M.R.T.
V tomto vzorci:
π = je osmotický tlak
M = je koncentrácia v mol / L
R = je všeobecná plynová konštanta (0,082 pre tlak v atm; 62,3 pre tlak v mmHg)
T = teplota v Kelvinoch
Pretože koncentrácia v mol / L má konkrétny vzorec, ako je uvedené nižšie:
M = m1
M1.V
Môžeme ho nahradiť vo vzorci osmotického tlaku:
π = m1.R.T
M1.V
Poznámka: Ak je rozpustná látka prítomná v roztoku iónová, musíme použiť Van't Hoffov korekčný faktor i) vo vyjadrení výpočtu osmotického tlaku:
π = M.R.T.i.
Príklad výpočtu osmotického tlaku
Príklad: (UF-PA) Roztok obsahujúci 2 mg nového antibiotika v 10 ml vody pri 25 ° C vytvára osmotický tlak 0,298 mmHg. Molekulová hmotnosť tohto antibiotika je teda približne:
a) 3 000
b) 5200
c) 7500
d) 12500
e) 15300
Údaje poskytnuté cvičením boli:
n = 0,298 mmHg
T = 25 OC alebo 298 K (po pridaní 273)
m1 = 2 mg alebo 0,002 g (po vydelení 1000)
V = 10 ml alebo 0,01 l (po vydelení 1000)
R = 62,3 mmHg
Ak chcete vyriešiť toto cvičenie, jednoducho použite dostupné údaje vo výraze na výpočet osmotického tlaku nasledovne:
π = m1.R.T
M1.V
0,298 = 0,002.62,3.298
M1.0,01
0,298 M.1.0,01 = 37,1308
0,00298 M.1 = 37,1308
M1 = 37,1308
0,00298
M1 = 12460 u
Podľa mňa. Diogo Lopes Dias
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
DNI, Diogo Lopes. „Čo je to osmoskopia?“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-osmoscopia.htm. Prístup k 28. júnu 2021.