Organické zlúčeniny môžu byť reprezentované rôznymi spôsobmi, napríklad plochým štruktúrnym vzorcom, zjednodušeným alebo kondenzovaným štruktúrnym vzorcom alebo pomlčkovým vzorcom. Najjednoduchšie je však znázornenie pomocou molekulárneho vzorca.

Pozrime sa teda, ako určiť molekulárny vzorec organických zlúčenín na základe ďalších vyššie uvedených vzorcov.
1. Prostredníctvom plochého štruktúrneho vzorca:tento vzorec ukazuje usporiadanie alebo usporiadanie atómov v molekule. Napríklad nižšie je uvedený plochý štruktúrny vzorec jedného z uhľovodíkov prítomných v benzíne.

Upozorňujeme, že v tomto vzorci sú zobrazené všetky atómy a všetky existujúce väzby medzi nimi. Teraz, aby ste určili molekulárny vzorec tejto zlúčeniny, stačí spočítať počet atómov každého prvku a umiestniť index na pravú dolnú stranu príslušného prvku.
Dôležitým aspektom, ktorý je potrebné zdôrazniť, je to molekulárny vzorec organických zlúčenín začíname vždy od prvku uhlík, pretože je hlavnou zložkou týchto látok. Pozrite si príklad:
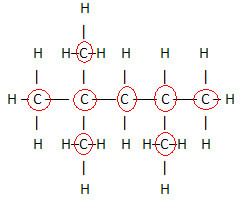
Pretože má 8 uhlíkov, začneme písať molekulárny vzorec takto: Ç8
Na dokončenie tohto vzorca počítame množstvo vodíkov:
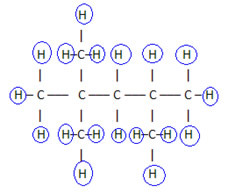
Takže vaše molekulárny vzorec é Ç8H18.
2. Prostredníctvom zjednodušeného alebo zhusteného štruktúrneho vzorca: v tomto type vzorca je množstvo vodíkov skrátené. Napríklad sa pozrite na rovnaký vzorec pre molekulu, ktorá sa nachádza v benzíne, teraz v kondenzovanej forme:
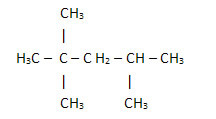
Teraz neprestávajte... Po reklame je toho viac;)
Takto je ešte jednoduchšie spočítať množstvo vodíkov, stačí pridať indexy (3 +3+ 3 +2 +1 +3 +3 = 18).
Teraz sa však pozrime na kondenzovaný štruktúrny vzorec kyseliny linolovej, ktorý existuje v zelenine, ako je bavlna, sója, slnečnica atď. a ktorý sa používa vo farbách a lakoch:
H3C─CH2CH2CH2CH2CH═CH─CH2CH═CH─CH2CH2CH2CH2CH2CH2CH2─COOH
Počítaním množstva uhlíkov, vodíkov a kyslíkov máme nasledujúce molekulárny vzorec kyseliny linolovej: Ç18H32O2.
3. Prostredníctvom vzorca mŕtvice: tento vzorec ďalej zjednodušuje spôsob predstavovania organických zlúčenín, pretože vynecháva skupiny C, CH, CH2 a CH3.
Príkladom je linolová molekula, pozrite sa, ako to vyzerá:

Najprv spočítajme množstvo uhlíkov, nezabúdajme, že v tomto vzorci je každá väzba medzi uhlíkmi predstavovaná pomlčkou. Končeky teda rovnako ako dva inflexné body zodpovedajú atómom uhlíka.
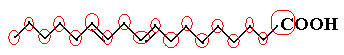
Takže máme: Ç18
Teraz, aby sme spočítali množstvo vodíkov, si musíme uvedomiť, že väzby medzi uhlíkmi a vodíkmi sú implikované, pretože je známe, že uhlík vytvára štyri väzby; teda množstvo chýbajúcich väzieb je množstvo vodíka naviazaného na tento prvok.
Prečítajte si vysvetlenie nižšie:
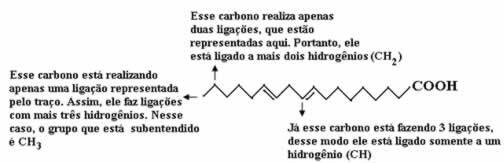
Množstvo vodíka bude teda: 32.

Množstvo kyslíka sa dá spočítať celkom jednoducho, pretože sú iba dva. Keďže molekulárny vzorec é: Ç18H32O2.
Autor: Jennifer Fogaça
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. "Molekulárne vzorce organických zlúčenín"; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/formulas-moleculares-compostos-organicos.htm. Prístup k 28. júnu 2021.
Uhlíkový priestorový vzorec, Lewisov elektronový vzorec, rovinná štruktúra, elektronické páry, väzba kovalentná, valenčná vrstva, vývoj atómového modelu, molekulárny vzorec, štruktúrny vzorec, vzorce trojrozmerný.
Chemické vzorce, plochý štruktúrny vzorec, Couperov štruktúrny vzorec, trojitá väzba, plyn dusík, elektronický vzorec, Lewisov vzorec, molekulárny vzorec, jednoduchá väzba, dvojitá väzba, plyn uhličitý.