O chlorid sodný (kuchynská soľ) je soľ, ktorú používame v každodennom živote na solenie ručne vyrábaných alebo spracovaných (industrializovaných) potravín. Je to látka, ktorá je tiež prítomná v rôznych prírodných potravinách, ktoré denne konzumujeme, ako sú ovocie, zelenina, strukoviny, semená atď.
V tomto texte budete vedieť všetko o tejto dôležitej látke pre každodenný život človeka:
definícia
Chlorid sodný patrí k anorganickej funkcii solí a je tvorený asociáciou katiónu sodného (Na+) je to anión ctamoreto (Cl-) prostredníctvom a iónová väzba.
b) Chemické vlastnosti
Chlorid sodný tvoria dva chemické prvky:
→ Sodík (Na):
patrí do skupiny kovov (schopné ľahko vytvárať katióny) alkalické (AI);
má elektrón vo valenčnom obale;
má atómové číslo rovné 11;
má vysokú elektropozitivitu (schopnosť strácať elektróny).
→ chlór (Cl)
patrí do rodiny halogénov (VIIA);
je to nekov (preto sa tak ľahko stane aniónom);
má vo valenčnej škrupine sedem elektrónov;
má atómové číslo rovné 17;
má vysokú elektronegativitu (schopnosť získavať elektróny).
Ako dva chemické prvky, ktoré tvoria chlorid sodný, sú prítomné, respektíve, vysoká elektropozitivita a vysoká elektronegativita, medzi nimi je iónová väzba (založená medzi atómami s tendenciou strácať a získavať elektróny).
Chemická štruktúra chloridu sodného sa skladá z jedného chloridového aniónu (zelená guľa), ktorý interaguje so šiestimi katiónmi sodíka (modré guľôčky), ako je zrejmé z nasledujúcej štruktúry:
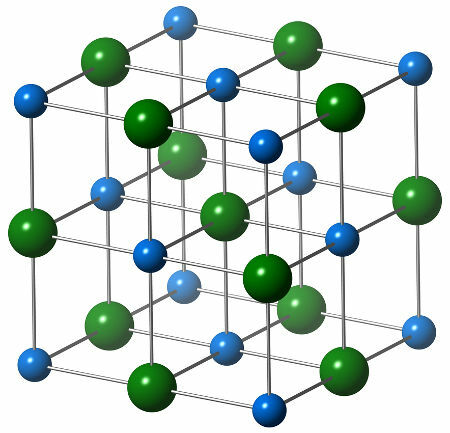
Reprezentácia kryštalickej štruktúry chloridu sodného
c) Fyzikálne vlastnosti
Bod tavenia:
Chlorid sodný sa môže transformovať z pevného stavu do tekutého stavu pri teplote 801 OÇ.
Bod varu:
Chlorid sodný sa môže transformovať z kvapalného do plynného stavu pri teplote 1465 OÇ.
Polarita
Pretože ide o látku vzniknutú iónovou väzbou, to znamená, že ide o iónovú zlúčeninu, je chlorid sodný polárny.
Rozpustnosť vo vode
Môžeme rozpustiť v 1 L vody, pri 25 ° C OC, až 359 gramov chloridu sodného.
Rozpustnosť v iných rozpúšťadlách:
Pretože chlorid sodný je polárna zlúčenina, nemôže sa rozpustiť v žiadnom nepolárnom rozpúšťadle, napríklad v oleji.
Hustota:
Hustota chloridu sodného je 2,165 g / ml, preto je hustejšia ako voda, ktorá má hustotu 1 g / ml.
Elektrická vodivosť:
Pretože je to iónová zlúčenina, chlorid sodný je schopný viesť elektrický prúd, iba ak:
Je v roztavenom stave, to znamená v tekutom stave;
Rozpustený vo vode.
d) Metódy získavania
Chlorid sodný sa dá získať fyzicky alebo chemicky:
1O) Získanie fyzickej hodnoty:
frakčná kryštalizácia
Chlorid sodný sa získava odparením vody z oceánov.
podzemné bane
Extrahuje sa v baniach pomocou banských techník.
podzemné ložiská
Extrahuje sa z hlbokých podzemných ložísk rozpustením vo vode (soľ prítomná v ložisku sa rozpúšťa) a následným čerpaním.
2O) Získanie chemicky
syntézna reakcia
Chlorid sodný sa dá získať chemickou reakciou syntézy (jednoduché látky vedú k zloženiu látky) medzi plynným chlórom a kovovým sodíkom:
2 vstupys + Cl2 písm. G) → 2 NaCls
Neutralizačná reakcia:
Ďalším spôsobom, ako chemicky získať chlorid sodný, je neutralizačná reakcia medzi kyselinou chlorovodíkovou a hydroxidom sodným, pri ktorej vzniká soľ a voda:
HCl(1) + NaOH(tu) → NaCl(tu) + H2O(1)
e) Dôležitosť pre ľudí
Samotný chlorid sodný nemá v ľudskom tele žiadnu funkciu, ale keď sa disociuje na katióny sodíka (Na+) a chloridové anióny (Cl-), každý z týchto dvoch iónov má pre naše telo niekoľko dôležitých funkcií. Pozrite si niektoré z týchto funkcií:
→ Funkcie katiónu sodného (Na+)
Zabraňuje zrážaniu krvi;
Bojuje proti tvorbe obličiek a žlčových kameňov;
Podieľa sa na regulácii telesných tekutín;
Podieľa sa na regulácii krvného tlaku.
→ Funkcie chloridového aniónu (Cl-)
Účasť na tvorbe a tvorbe žalúdočnej šťavy (kyselina chlorovodíková - HCl);
Účasť na tvorbe pankreatickej šťavy.
f) Poškodenie ľudského tela
Nadmerná konzumácia chloridu sodného môže spôsobiť ľuďom nasledujúce škody:
→ Poškodenie spôsobené nadmerným obsahom katiónov sodíka v tele:
Predĺžený čas hojenia rán;
Zvýšený výskyt kŕče;
Zvýšený krvný tlak;
Preťaženie obličiek;
Zvýšená retencia tekutín v tele.
→ Poškodenie spôsobené nadmerným obsahom chloridových aniónov v tele:
zničenie vitamín E.;
Zníženie produkcie jódu v tele.
g) Ostatné aplikácie
Okrem toho, že sa chlorid sodný používa na solenie jedál, môže sa použiť aj v nasledujúcich situáciách:
Výroba šampónov;
Výroba papiera;
Výroba Hydroxid sodný (NaOH);
Výroba čistiacich prostriedkov;
Výroba mydla;
Topenie snehu na miestach, ktoré trpia snehovými búrkami;
Výroba kovového sodíka;
Výroba chlóru;
V izotonike na náhradu telesného elektrolytu;
V roztokoch na prekrvenie nosa;
Výroba soľného roztoku; okrem iných aplikácií.
Podľa mňa. Diogo Lopes Dias

